被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内的离子“流过”水和氧化锌组成的电解液。电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH)。下列说法正确的是
| A.该电池的正极为锌 |
| B.电池正极反应式为:MnO2 + e-+H2O =" MnO(OH)" + OH- |
| C.该电池反应中二氧化锰起催化剂作用 |
| D.当 0.l mol Zn 完全溶解时,流经电解液的电子数目为 1.204×l023 |
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH + 3O2 + 4OH— =2CO32— + 6H2O,则下列说法错误的是
| A.放电时CH3OH参与反应的电极为正极 |
| B.充电时电解质溶液的pH逐渐增大 |
| C.放电时负极的电极反应为:CH3OH-6e-+8OH- = CO32— + 6H2O |
| D.充电时每生成1 mol CH3OH转移6 mol电子 |
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是: 。
。
总反应式为: 
 ,下列说法正确的是
,下列说法正确的是
| A.Zn为正极, Ag2O为负极 |
| B.电解质溶液中, OH-移向Ag2O极 |
| C.原电池工作时,正极区溶液pH值增大 |
| D.原电池工作时,负极区溶液pH值增大 |
用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示。下列说法正确的是
A.充电时,阴极的电极反应为: |
B.放电时,负极的电极反应为: |
| C.放电时,OH-移向镍电极 |
| D.充电时,将电池的碳电极与外电源的正极相连 |
近年来,科学家研制了一种新型的乙醇燃料电池,它用酸性电解质(H+)作溶剂。电池总反应为:C2H5OH+3O2=2CO2+3H2O,下列说法不正确的是
| A.乙醇在电池的负极上参加反应 |
| B.1mol CH3CH2OH被氧化转移6mol e- |
| C.随着反应的进行,正极附近的酸性减弱 |
| D.电池放电过程中化学能转化成电能 |
用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示。下列说法正确的是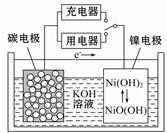
| A.充电时,阴极的电极反应为:Ni(OH)2+OH--e-===NiO(OH)+H2O |
| B.放电时,负极的电极反应为:H2-2e-+2OH-=== 2H2O |
| C.放电时,OH-移向镍电极 |
| D.充电时,将电池的碳电极与外电源的正极相连 |
某充电宝锂离子电池的总反应为:xLi + Li1-xMn2O4  LiMn2O4,某手机镍氢电池总反应为:NiOOH + MH
LiMn2O4,某手机镍氢电池总反应为:NiOOH + MH M+ Ni(OH)2(M为储氢金属或合金),有关上述两种电池的说法不正确的是:
M+ Ni(OH)2(M为储氢金属或合金),有关上述两种电池的说法不正确的是:
| A.锂离子电池放电时Li+向正极迁移 |
| B.镍氢电池放电时,正极的电极反应式:NiOOH+H2O+e-="=" Ni(OH)2+OH- |
| C.上图表示用锂离子电池给镍氢电池充电 |
| D.锂离子电池充电时,阴极的电极反应式:LiMn2O4—xe-="=" Li1-xMn2O4+ xLi+ |
一种新型的乙醇电池,它用磺酸类质子溶剂。电池总反应为:C2H5OH +3O2 → 2CO2 +3H2O,电池示意如图,下列说法正确的是
| A.a极为电池的正极 |
| B.电池工作时电流由a极沿导线经灯泡再到b极 |
| C.电池负极的电极反应为:4H+ + O2 + 4e-= 2H2O |
| D.电池工作时,1mol乙醇被氧化时就有12mol电子转移 |
科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,下列说法不正确的是
| A.通入N2的电极发生的电极反应式为:N2 + 6e- + 8H+="=" 2NH4+ |
| B.反应过程中溶液的pH会变大,故需要加入盐酸 |
| C.该电池外电路电流从通入H2的电极流向通入N2的电极 |
| D.通入H2的电极为负极,A为NH4Cl |
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为
Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列结论正确的是
| A.Pb 为正极被氧化 |
| B.溶液的pH不断减小 |
| C.放电时负极反应式是PbO2 +4H++ SO42-+2e-= PbSO4 +2H2O |
| D.溶液pH不断增大 |
科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入以磷酸为电解质的燃料电池发电。电池负极反应为:
| A.H2+2OH-=2H2O+2e- | B.O2+4H++4e-=2H2O |
| C.H2 -2e-=2H+ | D.O2+2H2O+4e-=4OH- |
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法正确的是
| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为O2+2H2O+4e-===4OH- |
| C.每转移0.2 mol电子,消耗标准状况下1.12 L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |
微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,负极反应为:Zn+2OH--—2e-==ZnO+H2O;正极反应为:Ag2O+H2O+2e-="=2Ag+2OH-" ,根据反应式,判断下列叙述正确的是
| A.在使用过程中,电池正极区溶液的pH增大 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn是正极,Ag2O是负极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为
下列叙述不正确的是
| A.放电时负极反应为:Zn—2e— +2OH—= Zn(OH)2 |
B.充电时阳极反应为:Fe(OH)3 —3e—+5 OH— = FeO +4H2O +4H2O |
| C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |