有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是
①每消耗1 mol CH4可以向外电路提供8 mol e-②负极上CH4失去电子,电极反应式为CH4+10OH--8e-=CO+7H2O ③负极上是O2获得电子,电极反应式为O2+2H2O+4e-=4OH-④电池放电后,溶液的pH不断升高
| A.①② | B.①③ | C.①④ | D.③④ |
固体氧化物燃料电池是以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。
下列判断正确的是
| A.有O2参加反应的a极为电池的负极 |
| B.电路中每转移2mole-,则消耗H2的体积为22.4L. |
| C.a极对应的电极反应式为O2+2H2O+4e-=4OH- |
D.该电池的总反应式为2H2+O2 2H2O 2H2O |
某航空站安装了一台燃料电池,该电池可同时提供电和水蒸气。所用燃料为氢气,电解质为熔融的碳酸钾。已知该电池的总反应为2H2+O2=2H2O,正极反应为O2+2CO2+4e-=2CO32-,则下列推断正确的是
| A.负极反应为H2+2OH--2e-=2H2O |
| B.该电池可在常温或高温时进行工作,对环境具有较强的适应性 |
| C.该电池供应2 mol水蒸气,同时转移2 mol电子 |
| D.放电时负极有CO2生成 |
科研人员设想用右图所示装置生产硫酸,下列说法正确的是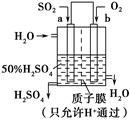
| A.a为正极,b为负极 |
| B.负极反应式为2H2O+SO2-2e-=SO42-+4H+ |
| C.电子从b极向a极移动 |
| D.生产过程中H+向a电极区域运动 |
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-。总反应式为:Ag2O+Zn=2Ag+ZnO,下列说法正确的是
| A.Zn为正极,Ag2O为负极 |
| B.Zn为负极,Ag2O为正极 |
| C.原电池工作时,正极区溶液pH值减小 |
| D.原电池工作时,负极区溶液pH值增大 |
“嫦娥一号”探测器所用的镍氢蓄电池,其负极板材料M为能吸收氢原子的合金。充电时电极反应分别为:M + H2O + e-=" MH" + OH-,Ni(OH)2 + OH-- e-=" NiOOH" + H2O。
下列有关镍氢蓄电池的说法正确的是
| A.放电时,正极附近的pH减小 |
| B.放电时,总反应为MH + NiOOH =" M" + Ni(OH)2 |
| C.充电时,电极M应与充电电源正极相连 |
| D.充电后,负极板材料M变成了MH,MH中H元素显-1价 |
液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池以空气中的氧气为氧化剂,以KOH溶液为电解质溶液。下列关于该电池的叙述错误的是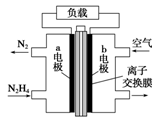
| A.b极发生还原反应 |
| B.a极的反应式为N2H4 - 4e-===N2↑+4H+ |
| C.放电时,电流从b极经过负载流向a极 |
| D.其中的离子交换膜需选用阴离子交换膜 |
一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是
A.反应CH4+H2O 3H2+CO,每消耗1molCH4转移12mol电子 3H2+CO,每消耗1molCH4转移12mol电子 |
| B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O |
| C.电池工作时,CO32-向电极B移动 |
| D.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- |
TESLA电动汽车的电池采用了松下提供的NCA系列(镍钴铝体系)的18650A型钴酸锂(LiCoO2)锂离子电池。电池正极材料为钴酸锂(LiCoO2),负极材料是石墨(C6)。电池反应为:
LiCoO2+C6 C6Lix+Li1-xCoO2。下列有关说法不正确的是
C6Lix+Li1-xCoO2。下列有关说法不正确的是
| A.锂离子电池与传统铅蓄电池相比,具有高比能量(比能量指的是单位重量或单位体积的能量)的特点 |
| B.废旧锂离子电池先进行“放电处理”让Li+进入石墨(C6)中而利于回收 |
| C.放电时,正极锂的化合价未发生改变 |
| D.充电时电池标有(+)的极上发生的反应为:LiCoO2—x e-=== Li1-x CoO2+xLi+ |
右图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是
| A.分子组成为Cm(H2O)n的物质一定是糖类 |
| B.微生物所在电极区放电时发生还原反应 |
| C.放电过程中,H+从正极区移向负极区 |
| D.正极反应式为:MnO2+4H++2e—=Mn2++2H2O |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为 CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法正确的是
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4mol电子转移,则消耗氧气的体积2.24L |
| C.电池反应的化学方程式为:CH3CHO+O2=CH3COOH+H2O |
| D.正极上发生的反应是:O+4e-+2H2O=4OH- |
全钒液流电池是一种新型的绿色环保储能电池。其电池总反应为:
V3++ VO2++H2O VO2++2H++V2+ 下列说法正确的是
VO2++2H++V2+ 下列说法正确的是
| A.放电时每转移2mol电子时,消耗1mol氧化剂 |
| B.放电时正极反应为:VO+2+2H++e—=VO2++H2O |
| C.放电过程中电子由负极经外电路移向正极,再由正极经电解质溶液移向负极 |
| D.充电过程中,H+由阴极区移向阳极区迁移 |
一种碳纳米管能够吸附氢气,用这种材料吸氢后制备的二次电池(充放电电池)工作原理如下图所示,该电池的电解质为6 mol·L-1KOH溶液,下列说法中正确的是
| A.放电时K+移向碳电极 |
| B.放电时电池负极的电极反应为H2-2e-= 2H+ |
| C.充电时镍电极的电极反应为Ni(OH)2 + OH――e-= NiO(OH) + H2O |
| D.该电池充电时将碳电极与电源的正极相连,发生氧化反应 |
热激活电池可用作火箭、导弹的工作电。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池的总反应方程式为:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是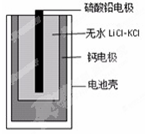
| A.正极反应式:Ca +2Cl--2e-=CaCl2 |
| B.放电过程中,Li+向负极移动 |
| C.每转移0.1mol电子,理论上生成20.7gPb |
| D.常温时,在正负极间接上电流表或检流计,指针不偏转 |