我国在青藏高原发现了名为“可燃冰”的环保型新能源。
(1)“可燃冰”属于化石燃料,主要成分是CH4。另外还有两种化石燃料,它们的名称分别是 ________和 。
(2)CH4可与Cl2反应,反应历程如下
则CH4与Cl2反应生成CH3-Cl(g)的热化学方程式为 。
(3) CH4可用于设计燃料电池。甲烷燃料电池的工作原理如下图所示:
CH4可用于设计燃料电池。甲烷燃料电池的工作原理如下图所示:
则通入CH4的一极为原电池的 (填“正极”或“负极”),正极的电极反应式为 。
(4)在25℃时,将两个铂电极插入一定量的饱和Na2SO4溶液中进行电解,通电一段时间后在阳极逸出a mol气体,同时析山w g Na2SO4·10H2O晶体,若温度不变,此时剩余溶液的质量分数是 。
(14分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)目前工业上有一种方法是用CO2来生产燃料甲醇。
为探究反应原理,现进行如下实验,在体积为1 L的 密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。
①从反应开始到平衡,氢气的平均反应速率υ(H2)=__________mol/(L·mi n)。
n)。
②该反应的平衡常数表达式为K=__________。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1277 kJ·mol-1
ΔH=-1277 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
③C(s)+ O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
④H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
则,CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH=________kJ·mol-1。
(3)2009年10月 ,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
①该电池工作时,b口通入的物质为___________,c口通入的物质为___________。
②该电池负极的电极反应式为:_________________。
③工作一段时间后,当外电路中有1.2NA个电子通过时,有 g甲醇参加反应。
(4)在下列选项中与甲醇互为同系物的是_______(填字母代号),该同系物与相对分子质量相同的羧酸反应的化学方程式为______________,该反应的反应类型是____________。
试写出一种与D选项互为同分异构体且含有苯环的物质_______________。
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)利用反应6NO2+ 8NH3 7N2+12 H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N2+12 H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=—196.6 kJ·mol-1
2SO3(g) ΔH=—196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=—113.0 kJ·mol-1
2NO2(g) ΔH=—113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH= kJ·mol-1。
SO3(g)+NO(g)的ΔH= kJ·mol-1。
(3)铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O= Fe(OH)2+2Ni(OH)2
当电池放电时,正极电极反应式为 。
一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通乙烷(C2H6)和氧气,其中某一电极反应为:C2H6+18OH――14e—=2CO32-+12H2O。有关此电池的推断错误的是
| A.通氧气的电极为正极 |
| B.参加反应的O2与C2H6的物质的量之比为7∶2 |
| C.放电一段时间后,KOH的物质的量浓度将下降 |
| D.放电一段时间后,正极区附近溶液的pH减小 |
锂电池用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)中形成的,该电池的总反应方程式为:8Li+3SOCl2=6LiCl+Li2SO3+2S,下列叙述中正确的是
| A.电解质溶液中混入水,对电池反应无影响 |
| B.上述过程中是电能转化成化学能 |
| C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3 |
| D.电池工作过程中,金属锂提供电子的物质的量与析出硫的物质的量之比为4 :1 |
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含 盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。下列“水” 电池在海水中放电时的有关说法正确的是
盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。下列“水” 电池在海水中放电时的有关说法正确的是
| A.正极反应式:Ag+Cl--e-=AgCl | B.每生成1 mol Na2Mn5O10转移2 mol电子 |
| C.Na+不断向“水”电池的负极移动 | D.AgCl是还原产物 |
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨和锂,含Li+ 导电固体为电解质。下列有关LiFePO4电池说法正
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨和锂,含Li+ 导电固体为电解质。下列有关LiFePO4电池说法正 确的是
确的是
| A.可加入硫酸以提高电解质的导电性 |
| B.充电过程中,电池正极材料LiFePO4的质量减少 |
| C.放电时电池内部Li+ 向负极移动 |
| D.放电时电池负极反应为:FePO4+Li++e-= LiFePO4 |
铅蓄电池的总反应为:PbO2(s)+Pb(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l)关于铅蓄电池的说法正确的是
2PbSO4(s)+2H2O(l)关于铅蓄电池的说法正确的是
| A.在放电时,正极发生的反应是Pb(s)+SO(aq) -2e-=PbSO4(s) |
| B.在放电时,该电池的负极材料是铅板 |
| C.在充电时,电池中硫酸的浓度不断变小 |
| D.在充电时,阳极发生的反应是PbSO4(s)+2e-=Pb(s)+SO(aq) |
.汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2 + Pb + 2H2SO4 = 2PbSO4↓+ 2H2O,根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb + SO42- - 2e - = PbSO4↓ |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
某经济开发区将钛冶炼厂与氯碱厂、甲醇厂组成了一个产业链(如图所示),大大地提高了资源利用率,减少了环境污染。
请填写下列空白:
(1)写出钛铁矿经氯化得到四氯化钛的化学方程式: ▲ 。
(2)由CO和H2合成甲醇的方程式是:CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
①已知该反应在300℃时的化学平衡常数为0.27,该温度下将2 mol CO、3 mol H2和2 mol CH3OH充入容积为2 L的密闭容器中,此时反应将 ▲ (填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
②若不考虑生产过程中物质的任何损失,该产业链中每合成19.2 t甲醇,至少需额外补充H2 ▲ t。
(3)用甲醇—空气碱性(KOH)燃料电池作电源电解精炼粗铜(右图),
在接通电路一段时间后纯Cu质量增加3.2 g。
①请写出燃料电池中的负极反应式: ▲ 。
②燃料电池正极消耗空气的体积是 ▲ (标准状况,
空气中O2体积分数以20%计算)。
铅蓄电池是一种二次电池,在现代生活中有广泛的应用。其电极材料是Pb和PbO2,
电解质溶液为30%H2SO4溶液。下列说法正确的是
| A.电池充电时,电池负极和电源的负极相连接 |
| B.电池充电时,阴极反应为:Pb - 2e- + SO42-=PbSO4 |
| C.电池放电时,电池负极周围溶液c(H+)不断增大 |
| D.电池放电时,每消耗1mol Pb,共生成1mol PbSO4 |
(16分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,
请回答:
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示)。
(2)负极反应式为 。
(3)电极表面镀铂粉的原因为
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2="2LiH " Ⅱ.LiH+H2O==LiOH+H2↑
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
③由②生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
关于铜锌原电池和电解CuCl2溶液的装置(如右图),下列说法正确的是 
| A.锌是负极,铜片上有气泡产生,电流从锌片经导线流向铜片 |
| B.铜片质量逐渐减少,氢离子在铜片表面被还原 |
| C.d为阳极,电极反应为:2Cl—-2e—=Cl2↑ |
| D.电解过程中, d电极质量增加 |
镁电池毒性低、污染小,电压高而平稳,它逐渐成为人们研制绿色电池的关注焦点。其中一种镁电池的反应原理为: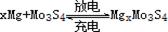 。下列说法不正确的是
。下列说法不正确的是
| A.放电时,Mo3S4发生氧化反应 |
| B.放电时,正极反应式:Mo3S4+2xe-→Mo3S42x- |
| C.充电时,Mg2+向阴极迁移 |
| D.充电时,阴极反应式:xMg2++2xe-→xMg |
(本题16分).哥本哈根气候变化峰会自2009年12月7日开幕以来,就被冠以“有史以来最重要的会议”、“改变地球命运的会议”等各种重量级头衔。纵然世界各国仍就减排问题进行着艰苦的角力,但低碳这个概念几乎得到了广泛认同。中国慈善首富陈光标2010年11月5号创作的低碳之歌——《让我们再回到从前》让低碳概念融入到每个人的生活之中,减碳是每个人的责任。新能源开发中的燃料电池是低碳研究的重要领域。
(1)可燃性的有机物和氧气在理论上都可以作为燃料电池中的反应物,现以CxHyOz表示燃料电池中的有机反应物,O2为正极反应物,40%的KOH溶液为电解质溶液,请写出CxHyOz-O2-KOH燃料电池的负极的电极反应式: 。
(2)日本茨城大学研制了一种新型的质子交换膜二甲醚燃料电池(DDFC),该电池有较高的安全性。电池总反应为:CH3OCH3 +3O2=2CO2 +3H2O ,电池示意如图,下列说法不正确的是:
A.a极为电池的负极
B.电池工作时电流由b极沿导线经灯泡再到a极
C.电池正极的电极反应为:O2 +2H2O+ 4e— = 4OH—
D.电池工作时,1mol二甲醚被氧化时有6mol电子转移
(3)若用C3H8-O2-KOH构成燃料电池,当有11克丙烷在电池的负极完全反应,则在电池的外电路上转移的电子的物质的量为 mol;此过程中放出的总能量为A KJ,并已知1molCO2与足量KOH溶液反应放出的热量为B KJ。写出表示丙烷燃烧热的热化学方程式。 。
(4)将一定数量的C3H8-O2-KOH燃料电池按一定方式进行串联或者并联组成电池组以满足电解需要的电压。现用该电池组电解500mL某CuSO4的稀溶液,电解后的溶液需要加入98克Cu(OH)2才能使溶液恢复到原硫酸铜溶液的浓度和质量。若忽略电池组在电解过程中的能量损失,其能量全部用来电解CuSO4溶液,计算:
①原CuSO4的溶液的浓度。
②该电池组消耗的丙烷在标准状况时的体积。