某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是
| A.a为CH4,b为CO2 |
| B.CO32-向负极移动 |
| C.此电池在常温时也能工作 |
| D.正极电极反应式为O2+2H2O+4e-="==" 4OH- |
(1)已知:①C3H8(g)+5O2(g)==3CO2(g)+4H2O(l) ΔH="-2220.0" kJ·mol-1
②H2O(l)==H2O(g) ΔH="+44.0" kJ·mol-1
写出丙烷燃烧生成CO2和气态水的热化学方程式:______________________。
(2)航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置,它可直接将化学能转化为电能。我国发射的“神舟五号”载人飞船是采用先进的甲烷电池为电能来源,该电池以KOH溶液为电解质。试回答:
①负极上的电极反应为________________________________;
②消耗标准状况下的5.6 L O2时,有________mol电子发生转移。
③开始放电时,正极附近溶液的pH________(填“增大”“减小”或“不变”)。
根据下图所示的装置,判断下列说法正确的是
| A.该装置中a极为负极 |
| B.该装置中b极的电极反应式是:2H++2e-= H2↑ |
| C.一段时间后,左边装置中溶液pH增大 |
| D.CuSO4溶液浓度保持不变 |
用酸性氢氧燃料电池为电源电解CuSO4溶液的实验装置如下图所示。下列说法中正确的是( )
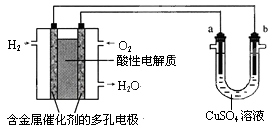
| A.燃料电池工作时,正极反应为:O2+2H2O+4e-=4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是
A.反应CH4+H2O 3H2+CO,每消耗1molCH4转移12mol电子 3H2+CO,每消耗1molCH4转移12mol电子 |
| B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O |
| C.电池工作时,CO32-向电极B移动 |
| D.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- |
聚合物锂离子电池以其良好的性能、低发热而广泛应用于手机的移动电源。某品牌聚合物锂离子电池的反应如下:LiCoO2+nC  Li1-xCoO2+LixCn。下列说法正确的是
Li1-xCoO2+LixCn。下列说法正确的是
| A.放电时,负极发生反应的物质是 Li1-xCoO2 |
| B.充电时,阴极发生氧化反应 |
| C.放电时,Li+由负极向正极迁移 |
| D.充电时,阳极的电极反应式为:xLi++nC+xe-= LixCn |
(1)写出下列化合物的结构简式
2,2,3,3,-四甲基戊烷:__________________________。
(2)①写出Na2CO3溶液与AlCl3溶液反应的离子方程__________________________。
②写出由甲苯制备TNT的化学方程式:__________________________。
③Na2CO3溶液显碱性,用离子方程式表示原因___________,其溶液中离子浓度大小顺序为___________。
(3)除去括号中的杂质,填上适宜的试剂和提纯方法
乙醇(水):__________、_________。
(4)甲烷燃料电池(在KOH环境中)的负极的电极反应式:___________________。
(5)将煤转化为煤气的主要化学反应为:C(s)+H2O(g)===CO(g)+H2(g)
C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
H2(g)+ O2(g)===H2O(g) ΔH=-242.0 kJ/mol
O2(g)===H2O(g) ΔH=-242.0 kJ/mol
CO(g)+ O2(g)===CO2(g) ΔH=-283.0 kJ/mol
O2(g)===CO2(g) ΔH=-283.0 kJ/mol
根据以上数据,写出C(s)与水蒸气反应的热化学方程______________________。
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时反应为
Pb+PbO2+2H2SO4 2PbSO4+2H2O,下列结论正确的是
2PbSO4+2H2O,下列结论正确的是
| A.Pb为正极,发生氧化反应 | B.SO42-只向正极移动 |
| C.电解质溶液密度不断减小 | D.溶液的pH不断减小 |
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢氧燃料电池的说法正确的是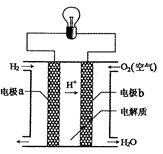
| A.该电池工作时电能转化为化学能 |
| B.该电池中电极a是正极 |
| C.外电路中电子由电极b通过导线流向电极a |
| D.该电池的总反应:2H2+O2 = 2H2O |
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2由此可知,该电池充电时在阳极上发生反应的是( )
Cd(OH)2+2Ni(OH)2由此可知,该电池充电时在阳极上发生反应的是( )
| A.Ni(OH)2 | B.Cd(OH)2 | C.Cd | D.NiOOH |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
| A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B.充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
| C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
锌银电池的负极是Zn,正极是Ag2O,以苛性钠溶液为电解质,电池放电时的总反应为Zn+Ag2O+H2O==Zn(OH)2 + 2Ag,下列判断正确的是( )
| A.放电时,OH-向负极方向移动 |
| B.放电时,正极反应式为Zn+2OH--2e-===ZnO+H2O |
| C.充电时,Zn发生氧化反应 |
| D.充电时, 阴极附近PH 减小 |
2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200oC左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2=2CO2 +3H2O,电池示意如图,下列说法不正确的是
| A.电池工作时,1mol乙醇被氧化时就有6mol电子转移 |
| B.a极为电池的负极 |
| C.电池工作时电流由b极沿导线经灯泡再到a极 |
| D.电池正极的电极反应为:4H+ + O2 + 4e—=2H2O |
纸电池是一种有广泛应用的“软电池”,右图这种碱性纸电池采用薄层纸片作为载体和传导体,纸的两面分别附着锌和二氧化锰。下列有关该纸电池说法不合理的是
| A.Zn为负极,进行氧化反应 |
| B.电池工作时,电子由MnO2流向Zn |
| C.正极反应:MnO2+e-+H2O=MnO(OH)+OH- |
| D.电池总反应:Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH) |