下列离子方程式正确的是( )
| A.沸水中滴入FeCl3饱和溶液:Fe3++3H2O(沸水)=Fe(OH)3(胶体)+3H+ |
| B.一小块钠投入水中:Na+2H2O=Na++2OH-+H2↑ |
| C.Ca(HCO3)2溶液中加入足量NaOH溶液:HCO3-+OH-=H2O+CO32- |
| D.Na2CO3溶液中加入醋酸:CO32-+2H+=CO2↑+H2O |
下列离子方程式中正确的是
| A.小苏打溶液中滴加足量石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
| B.向NH4Al(SO4) 2溶液中滴入Ba(OH)2恰好使SO42-反应完全: 2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O |
| C.次氯酸钠溶液中通入SO2气体:2ClO-+SO2+H2O=2HClO+SO32- |
| D.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |
下列有关Fe2(SO4)3溶液的叙述正确的是
| A.该溶液中K+、Fe2+、SCN-、Br-可以大量存在 |
| B.和KI溶液反应的离子方程式: Fe3++2I-=Fe2++I2 |
| C.和Ba(OH)2溶液反应离子方程式:Fe3++ SO42-+Ba2++3OH-=Fe(OH)3↓+BaSO4↓ |
| D.1 L0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2g Fe |
下列离子方程式书写正确的是( )
| A.NaClO溶液中通入少量的SO2气体:2ClO-+SO2+H2O=SO32-+2HClO |
| B.铜跟浓硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
| C.向Ca(HCO3)2溶液中滴加过量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| D.等体积等物质的量浓度的NH4HCO3与Ba(OH)2溶液混合后加热:NH4++OH-=NH3↑+H2O |
下列反应的离子方程式正确的是( )
| A.乙酸乙酯与氢氧化钠溶液反应:CH3COOCH2CH3+ OH-—→CH3COO- + CH3CH2O- + H2O |
| B.醋酸溶液与新制氢氧化铜反应:2H++Cu(OH)2—→Cu2++2H2O |
C.苯酚钠溶液中通入少量二氧化碳:2 +CO2+H2O +CO2+H2O 2 2 +CO +CO |
D.乙醛溶液与新制氢氧化铜悬浊液共热CH3CHO+2Cu(OH)2+OH_ CH3COO-+ Cu2O↓+ 3H2O CH3COO-+ Cu2O↓+ 3H2O |
下列相关离子方程式书写正确的是
| A.NaClO溶液与FeCl2溶液混合:6Fe2++3ClO-+3H2O===2Fe(OH)3↓+3Cl-+4Fe3+ |
| B.用食醋检验牙膏中的碳酸钙:CaCO3+2H+===Ca2++CO2↑+H2O |
| C.FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2===2Fe3++2H2O |
D.电解MgCl2水溶液的离子方程式:2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
下列化学用语表达正确的是
| A.苏打溶液与稀盐酸反应的离子反应方程式:HCO3-+H+=== CO2↑+H2O |
| B.氨气溶于水显碱性的原因:NH3+ H2O === NH3·H2O ===NH4++ OH- |
C.饱和FeCl3溶液滴入沸水中制备Fe(OH)3胶体的离子方程式:Fe3++3H2O Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
| D.CO2通入到纯碱饱和溶液中反应的化学方程式:Na2CO3+CO2+H2O === 2NaHCO3↓ |
能正确表示下列反应的离子方程式为
| A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S |
| B.NH4HCO3溶于过量的NaOH溶液中:HCO3−+OH−=CO32−+H2O |
| C.少量SO2通入苯酚钠溶液中:C6H5O−+SO2+H2O=C6H5OH+HSO3− |
| D.大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO−+CO2↑+H2O |
下列有关离子方程式判断正确的是( )
| A.足量铁屑溶于稀硝酸:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| B.硫化钠溶液中通入足量硫化氢:H2S + S2-=2HS- |
| C.碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-=CO32-+H2O |
D.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O  2C6H5OH+CO32- 2C6H5OH+CO32- |
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42—、CO32—等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法正确的是
| A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+ |
| B.原溶液中含有的Fe3+和Al3+的物质的量之比为1∶1 |
| C.原溶液中一定含有SO42—和Na+ |
| D.反应最后形成的溶液中溶质只有Na2SO4 |
下列各组中的两种物质相互反应时,无论哪种过量,都可以用同一个离子方程式表示的是:( )
①碳酸钠溶液与盐酸 ②偏铝酸钠溶液与盐酸 ③苯酚钠溶液与CO2
④硝酸银溶液与氨水 ⑤氯化铝溶液与氨水 ⑥碳酸氢钠溶液与澄清的石灰水
| A.③⑤ | B.①③⑥ | C.仅有⑤ | D.②④ |
已知电离平衡常数:H2CO3>HClO>HCO3—,下列有关叙述中,正确的是:
①若KI溶液中混有Br-,加入足量FeCl3溶液,用CCl4萃取后,取无色的水层并加入AgNO3溶液,有淡黄色沉淀生成。
②向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2===2Fe3++2Cl-
③向NaClO溶液中通入少量二氧化碳的离子反应方程式:
2ClO-+CO2+H2O===2HClO+CO32—
④海水提溴过程中,用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为
3 Br2+6 CO32-+3H2O="5" Br-+ BrO3-+6HCO3-
| A.②④ | B.①③ | C.②③ | D.①④ |
下列离子方程式中,正确的是( )
A.向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO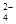 反应完全 反应完全2Ba2++ 4OH—+ Al3+ + 2SO 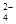 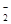 +2H2O +2H2O |
| B.向Mg(HCO3)2溶液中加入过量的NaOH溶液 Mg2++2HCO 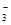 +4OH— +4OH—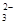 +2H2O +2H2O |
C.足量的CO2通入饱和碳酸钠溶液中:CO2+CO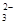 +H2O +H2O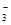 |
D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++2NO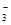 |
下列选项正确的是
| A.使pH试纸变成红色的溶液中,可能存在大量的:NH4+、Cu2+、ClO﹣、Cl﹣ |
| B.(NH4)2Fe(SO4)2溶液中,可能存在大量的:K+、Cu2+、Cl﹣、MnO4﹣ |
| C.硫酸酸化的淀粉KI溶液在空气中变成蓝色:4I﹣+O2+2H2O=2I2+4OH﹣ |
| D.NaHCO3溶液中滴加少量澄清石灰水:2HCO3﹣+Ca2++2OH﹣=CaCO3↓+2H2O+CO32﹣ |