下列离子方程式书写不正确的是
| A.过量铁粉与稀HNO3反应:3Fe+8H++2NO3-= 3Fe2++2NO↑+4H2O |
| B.向氧化铁中加入氢碘酸发生反应: Fe2O3+6H++2I- = 2Fe2++I2+3H2O |
| C.用稀HNO3溶解FeS固体:FeS+2H+===Fe2++H2S↑ |
| D.向溴化亚铁溶液中通入过量氯气:2Fe2++4Br-+3Cl2=2Fe3+ + 2Br2+ 6Cl- |
下列有关NaClO和NaCl混合溶液的叙述正确的是
| A.该溶液中,H+、NH4+、SO42-、Br-可以大量共存 |
| B.该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存 |
| C.向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+=== Cl-+2Fe3++H2O[Z |
| D.向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
下列离子方程式书写正确的是
| A.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O |
| B.过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑ |
| C.NH4HCO3溶液与过量的NaOH溶液反应:NH4++OH-=NH3↑+H2O |
| D.用氨水检验氯化钠溶液中混有氯化铝杂质:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
下列离子方程式书写正确的是
| A.Fe(NO3)3溶液中加入过量的HI溶液:3Fe3++2I-=3Fe2++I2 |
| B.NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
| C.漂白粉溶液中通入过量CO2气体:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
| D.向NH4Al(SO4)2溶液中不断滴加Ba(OH)2至溶液中SO42-完全沉淀; |
2Ba2-+4OH-+Al3++2SO42=2BaSO4↓+AlO2-+2H2O
下列解释实验事实的方程式不正确的是( )
A.0.1 /L /L 溶液的pH>1: 溶液的pH>1:  CHCOO-+H+ CHCOO-+H+ |
B.“ 球”浸泡在冷水中,颜色变浅2 球”浸泡在冷水中,颜色变浅2 (g) (红棕色) (g) (红棕色) N2O4 (g) (无色),△H<0 N2O4 (g) (无色),△H<0 |
C.铁溶于稀硝酸,溶液变黄:3Fe+8H++2N  3Fe2++2NO↑+4H2O 3Fe2++2NO↑+4H2O |
D.向Na2CO3溶液中滴入酚酞溶液,溶液变红:CO32— + H2O H CO3— + OH— H CO3— + OH— |
下列表示对应化学反应的离子方程式正确的是
| A.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性: 2MnO 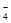 + 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O + 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O |
| B.Na2O2与H2O反应制备O2:Na2O2 + H2O= 2Na+ + 2OH- + O2↑ |
| C.NO2与水的反应:3NO2+H2O=2NO3-+NO+2H+ |
D.向NaAlO2溶液中通入过量CO2:2AlO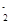 +CO2+3H2O=2Al(OH)3↓+CO2 +CO2+3H2O=2Al(OH)3↓+CO2 |
以下化学反应的离子方程式书写正确的是( )
| A.碳酸钠溶液中通入少量SO2:2CO32-+SO2+H2O=2HCO3-+SO32- |
| B.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I- |
| C.少量氯气通入溴化亚铁溶液中3Cl2+2Fe2++4Br- |
| D.NaHCO3溶液水解:HCO3-+ H2O=H2CO3 + OH- |
下列离子方程式书写正确的是
| A.Ba(OH)2溶液与过量的NaHCO3溶液混合:Ba2++2OH—+2HCO3-=BaCO3↓+CO32—+2H2O |
| B.在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入适量盐酸: 3Fe2++4H++NO3—=3Fe3++NO↑+2H2O |
| C.少量的氯气通入溴化亚铁溶液:3Cl2+2Fe2++4Br—=6Cl—+2Fe3++2Br2 |
| D.氧化铁粉末投入氢碘酸溶液中:Fe2O3+6H+=2Fe3++3H2O |
下列表示对应化学反应的离子方程式正确的是 ( )
| A.FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ |
| B.NO2与水的反应:3NO2+H2O=2NO3-+NO+2H+ |
| C.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
下列离子方程式与所述事实相符且正确的是
A.用惰性电极电解熔融氯化钠:2Cl—+2H2O Cl2↑+H2↑+2OH— Cl2↑+H2↑+2OH— |
| B.向偏铝酸钠溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| C.用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+=Cu2++2H2O |
| D.向碳酸氢钙溶液中加入足量的氢氧化钠溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O |
下列离子方程式与所述事实相符且正确的是
| A.用食醋和淀粉—KI试纸检验碘盐中的KIO3:IO3-+5I-+6H+=== 3I2+3H2O |
| B.稀HNO3溶液与难溶于水的FeS固体:FeS+2H+===Fe2++H2S↑ |
| C.碳酸氢钙与少量的NaOH溶液反应 Ca2++HCO3- +OH-=== CaCO3↓+ H2O |
| D.Na与水的反应Na + H2O=== Na++OH-+ H2↑ |
已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I━、Br━的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。横、纵坐标的单位均为mol。有关说法不正确的是
| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中c(FeBr2)= 6 mol/L |
| C.当通入Cl22mol时,溶液中已发生的反应可表示为2Fe2++2I━+2Cl2=2Fe3++I2+4Cl━ |
| D.原溶液中n (Fe2+): n (I-): n(Br-)=2:1:3 |
下列离子方程式正确的是:
| A.浓烧碱溶液中加入铝片:Al + 2OH-=AlO2-+H2↑ |
| B.向明矾溶液中滴加Ba(OH)2溶液,使SO42-全部沉淀: 2Al3+ + 6OH- +3SO42- +3Ba2+ = 2Al(OH)3↓+ 3BaSO4↓ |
| C.在2mol/L FeBr2溶液80mL中通入4.48L氯气(标况下),充分反应: 4Fe2+ +6Br- +5Cl2 = 4Fe3+ + 3Br2 + 10Cl- |
| D.用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+==H2↑+ Cl2↑ |
下列离子方程式不正确的是( )
| A.用稀硫酸除去铜绿:4H++Cu2(OH)2CO3===2Cu2++CO2↑+3H2O |
| B.将Na2O2固体投入H218O中:2H218O+2Na2O2===4OH-+4Na++18O2↑ |
| C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42—完全沉淀: 2Ba2++NH4++Al3++2SO42—+4OH-===Al(OH)3↓+NH3·H2O+2BaSO4↓ |
| D.向Na2FeO4溶液中加入稀硫酸产生氧气:4FeO42—+20 H+===4Fe3++3O2↑+10H2O |