下列离子方程式不正确的是
| A.用稀硫酸除去铜绿:4H++Cu2(OH)2CO3===2Cu2++CO2↑+3H2O |
| B.将Na2O2固体投入H218O中:2H218O+2Na2O2===4OH-+4Na++18O2↑ |
| C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO完全沉淀:2Ba2++NH+Al3++2SO+4OH-===Al(OH)3↓+NH3·H2O+2BaSO4↓ |
| D.向Na2FeO4溶液中加入稀硫酸产生氧气:4FeO+20 H+===4Fe3++3O2↑+10H2O |
下列反应的离子方程式正确的是( )
| A.铝粉投入到NaOH溶液中:2Al +2OH- = 2AlO2- + H2↑ |
| B.铁粉加入三氯化铁溶液中:2Fe +Fe3+ = 3Fe2+ |
| C.AlCl3溶液中加入足量的氨水:Al3+ + 3OH- = Al(OH)3↓ |
| D.FeCl2溶液中加入氯水:Cl2 +2 Fe2+ ="2" Fe3+ + 2Cl- |
下列离子方程式不正确的是( )
A.石英与烧碱溶液反应:SiO2+2OH-=== +H2O +H2O |
B.硅与烧碱溶液反应:Si+2OH-+H2O=== +2H2↑ +2H2↑ |
C.向小苏打溶液中加入过量的石灰水:2HCO+Ca2++2OH-===CaCO3↓+2H2O+ |
D.往水玻璃中加入盐酸:2H++ ===H2SiO3↓ ===H2SiO3↓ |
能正确表示下列反应的离子方程式是 ( )
| A.向KHSO4溶液中加入Ba(OH)2溶液至恰好沉淀完全 Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B.铁跟稀硫酸反应:2Fe + 6H+ ═ 2Fe3+ + 3H2 ↑ |
| C.碳酸钙与醋酸反应:CaCO3+2H+ ═ Ca2+ + CO2↑ + H2O |
| D.硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4 |
下列化学反应可用离子方程式CO+2H+===CO2↑+H2O表示的是( )
| A.石灰水和盐酸反应 |
| B.难溶的碳酸盐和难电离的酸反应生成CO2和H2O |
| C.可溶性碳酸盐与强酸反应生成CO2和H2O |
| D.可溶性碳酸盐与任何酸反应生成CO2和H2O |
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如下图所示,由此确定,原溶液中含有的阳离子是( )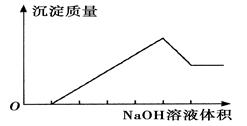
| A.H+、Al3+、Fe2+ | B.H+、Mg2+、Al3+ |
| C.H+、Ba2+、Al3+ | D.只有Mg2+、Al3+ |
下列离子方程式表达正确的是( )
A.Ca(HCO3)2溶液与足量盐酸混合:Ca(HCO3)2+2H+ Ca2++2CO2↑+2H2O Ca2++2CO2↑+2H2O |
B.Na2CO3溶液中通入CO2气体:CO32-+CO2+H2O 2HCO3- 2HCO3- |
C.实验室用NH4Cl固体与Ca(OH)2固体混合制NH3:NH4++OH- NH3↑+H2O NH3↑+H2O |
| D.将SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO32-+2HclO |
下列反应的离子方程式, 正确的是
| A.碳酸镁溶于浓硝酸中MgCO3+2H+=Mg2++H2O+CO2↑ |
| B.氧化铁溶于氢碘酸Fe2O3+6H+=2Fe3++3H2O |
| C.向漂白粉溶液中通入少量SO2气体H2O+Ca2++SO2+2ClO-=CaSO3+2HClO |
| D.FeBr2溶液中通入足量的Cl2:2Cl2+2Fe2++2Br-=4Cl-+2Fe 3++Br2 |
下列离子方程式正确的是
| A.在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7 :Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B.将少量SO2气体通入NaClO溶液中 :SO2+2ClO-+H2O=SO32-+2HClO |
| C.向碳酸氢钠溶液中滴入过量石灰水:HCO3- + Ca2+ + OH-=CaCO3↓+ H2O |
| D.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++ 3SO42-+ 3Ba2+ + 6OH-=2Al(OH)3↓+ 3BaSO4↓ |
下列有关离子方程式与所述事实相符且正确的是( )
A.用惰性电极电解CuCl2溶液:2Cu2++2H2O 4H++O2↑+2Cu 4H++O2↑+2Cu |
B.Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO ===BaSO4↓+2H2O ===BaSO4↓+2H2O |
| C.用氯化铁溶液和沸水反应制取氢氧化铁胶体:Fe3++3H2O(沸水) ===Fe(OH)3(胶体)+3H+ |
D.漂白粉溶液在空气中失效:ClO-+CO2+H2O===HClO+HCO |
下列离子方程式书写正确的是( )
A.铜片插入硝酸银溶液中 Cu + Ag+ Cu2++Ag Cu2++Ag |
B.铁溶于盐酸中: Fe+6H+ Fe3++3H2↑ Fe3++3H2↑ |
C.氯化铝溶液和氨水反应 Al3++NH3·H2O Al (OH) 3↓+NH4+ Al (OH) 3↓+NH4+ |
| D.NaHCO3溶液与HCl溶液反应:H++HCO3-=CO2↑+H2O |
下列解释实验事实的反应方程式不正确的是
| A.盛放烧碱的试剂瓶不能用玻璃塞:SiO2+2NaOH=Na2SiO3+H2O |
| B.用烧碱溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O |
C.用KSCN溶液检验Fe3+:Fe3++3SCN- Fe(SCN)3 Fe(SCN)3 |
| D.酸性KI淀粉溶液久置后变蓝:4I-+O2+2H2O=2I2+4OH- |
下列反应的离子方程式书写正确的是:
| A.用硫氰化钾溶液检验Fe3+:Fe3++3SCN- = Fe(SCN)3↓ |
| B.向海带灰浸出液中加入稀硫酸、双氧水:2I- + 2H+ + H2O2= I2 + 2H2O |
| C.磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH- = Na2SiO3↓+H2O |
| D.NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3- + OH-+ Ba2+ = H2O + BaCO3↓ |
将一定量的二氧化碳通入100毫升某浓度的氢氧化钠溶液中得到溶液X,若向X中逐渐加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示,则下列分析与判断不正确的是(不计二氧化碳溶解)
| A.若OA=AB,则溶液X为碳酸钠溶液 |
| B.若OA=0,则形成溶液X所发生反应的离子方程式为OH-+CO2=HCO3- |
| C.若OA>AB,则溶液X中大量存在的阴离子为碳酸根离子和碳酸氢根离子 |
| D.若3OA=AB,则溶液X中c(NaHCO3)=2c(Na2CO3) |
下列离子方程式书写不正确的是
| A.硫酸铜溶液和氢氧化钠溶液反应:Cu2﹣+2OH﹣═Cu(OH)2↓ |
| B.盐酸和氢氧化钠溶液反应:H++OH﹣═H2O |
| C.碳酸钙和盐酸溶液:CO32﹣+2H+═H2O+CO2↑ |
| D.氢氧化钡和硫酸的反应:Ba2++2OH﹣+2H++SO42﹣═2H2O+BaSO4↓ |