下列反应的离子方程式书写正确的是
| A.钠和冷水反应: Na+2H2O=Na++2OH-+H2↑ |
| B.金属铝溶于氢氧化钠溶液: Al+2OH-=AlO2-+H2 |
| C.铁跟稀硫酸反应:2Fe+6H+=2Fe3++3H2 |
| D.铜和硝酸银溶液反应: Cu + 2Ag+ =" 2Ag" + Cu2+ |
下列离子方程式正确的是
| A.铁粉撒入稀硫酸中2Fe + 6H+ →2Fe3+ + 3H2↑ |
| B.向AlCl3溶液中加入过量的氨水:Al3++4NH3·H2O→AlO2-+4NH4++2H2O |
| C.把金属钠放入冷水中:Na+H2O→Na++OH-+H2↑ |
| D.用氢氧化钠溶液除去铝表面的氧化铝:Al2O3+2OH-→2AlO2-+H2O |
下列反应的离子方程式正确的是
| A.一定量的碳酸氢钠溶液中加入足量澄清石灰水 HCO3-+Ca2++OH-= CaCO3↓+H2O |
| B.漂白粉的稀溶液中通入过量SO2气体 Ca2++2ClO-+SO2+H2O = CaSO3↓+2HClO |
| C.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O=2HClO+CO32- |
| D.Ba(OH)2溶液加入过量NaHSO4溶液中:H++SO42—+Ba2++OH—=BaSO4↓+H2O |
下列方程式书写正确的是
A.CO32-的水解方程式:CO32-+2H2O H2CO3+2OH- H2CO3+2OH- |
B.H2SO3的电离方程式H2SO3 2H++SO32- 2H++SO32- |
C.HCO3- 在水溶液中的电离方程式:HCO3-+H2O H3O++CO32- H3O++CO32- |
D.CaCO3的电离方程式:CaCO3 Ca2++CO32- Ca2++CO32- |
下列离子方程式中,正确的是:
| A.稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
| B.氧化镁与稀盐酸混合:MgO + 2H+=Mg2++ H2O |
| C.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++ Ag |
| D.铁与稀硫酸反应2Fe + 6H+=2Fe3++3H2↑ |
下列电离方程式正确的是( )
A.H2SO4  2H+ + SO42 - 2H+ + SO42 - |
B.BaCl2= Ba2+ + 2Cl- |
| C.NH3 •H2O = NH4+ + OH- | D.Na2CO3= Na+ + CO32- |
将2.32 g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1 mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中错误的是( )

| A.OA段发生反应的离子方程式为:H++OH-===H2O CO+H+===HCO |
| B.当加入35 mL盐酸时,产生CO2的体积为224 mL(标准状况) |
| C.A点溶液中的溶质为NaCl、NaHCO3 |
| D.混合物中NaOH的质量0.60 g |
下列离子方程式正确的是( )
| A.Fe3O4与稀硝酸反应:Fe3O4+8H+2Fe3+十Fe2++4H2O |
| B.向硫酸铵溶液中加入氢氧化钡溶液:Ba2++So42-BaSO4↓ |
| C.氯化铝溶液中加入过量氨水:Al3++3OH—==Al(OH)3↓ |
| D.含0.4molFeBr2溶液与0.4molCl2恰好反应:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
下列表示对应化学反应的离子方程式正确的是
| A.醋酸除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B.碘水中通入足量的SO2:I2 +SO2+2H2O=2I-+SO42-+4H+ |
| C.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D.惰性电极电解MgCl2溶液:Cl-+2H2O = 2OH-+H2↑+Cl2↑ |
下列热化学方程式或离子方程式中,正确的是
| A.氯化镁溶液与氨水反应:Mg2+ + 2OH- = Mg(OH)2 ↓ |
| B.500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: N2(g) + 3H2(g)  2NH3(g)△H= -38.6kJ·mol-1 2NH3(g)△H= -38.6kJ·mol-1 |
| C.甲烷的标准燃烧热△H= -890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g) + 2O2(g) = CO2(g)+2H2O(g) △H= -890.3kJ·mol-1 |
| D.氧化铝溶于NaOH溶液:Al2O3 + 2OH- =2AlO2- + H2O |
下列电离方程式正确的是
A.NaHSO4 Na++H++SO42- Na++H++SO42- |
B.HCO3-+H2O=== H3O++CO32- |
| C.HClO===H++ClO- | D.H2S H++HS- H++HS- |
下列相关反应的离子方程式书写错误的是
| A.在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:3ClO—+4OH—+2Fe(OH)3=3Cl—+5H2O+2FeO42— |
| B.少量SO2通入苯酚钠溶液中:2C6H5O—+SO2+H2O=2C6H5OH+SO32— |
| C.用稀硫酸酸化的KMnO4溶液与H2O2反应:2MnO4—+6H++5H2O2=2Mn2++5O2↑+8H2O |
| D.少量SO2通入NaClO溶液中:SO2+ClO—+OH—=SO42—+Cl—+H+ |
金属铈(58Ce)常用于制作稀土磁性材料,可应用于制造玻璃、打火石、陶瓷和合金等。已知:Ce4++Fe2+=Ce3+ +Fe3+。下列说法正确的是
| A.可用电解熔融CeO2制取金属铈,铈在阳极生成 |
B.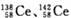 是同素异形体 是同素异形体 |
| C.铈能溶于HI溶液,发生反应的离子方程式为:Ce+4H+=Ce4++2H2 |
| D.铈的原子核外有58个电子 |
在以下各种情形下,下列电离方程式的书写正确的是 ( )。
| A.熔融状态下的NaHSO4电离:NaHSO4===Na++H++SO42- |
B.Fe(OH)3的电离:Fe(OH)3 Fe3++3OH- Fe3++3OH- |
C.H2CO3的电离:H2CO3 2H++CO32- 2H++CO32- |
| D.水溶液中的NaHSO4电离:NaHSO4===Na++HSO4- |