下列反应的离子方程式正确的是( )
| A.铝粉投入到NaOH溶液中:2Al +2OH- = 2AlO2- + H2↑ |
| B.铁粉加入三氯化铁溶液中:2Fe +Fe3+ = 3Fe2+ |
| C.AlCl3溶液中加入足量的氨水:Al3+ + 3OH- = Al(OH)3↓ |
| D.FeCl2溶液中加入氯水:Cl2 +2 Fe2+ ="2" Fe3+ + 2Cl- |
下列离子方程式正确的是( )
| A.澄清的石灰水与盐酸反应 Ca(OH) 2 + 2H+ = Ca2++ 2H2 O |
| B.钠与水的反应 Na + 2H2 O = Na++ 2OH- + H2↑ |
| C.铜片插入硝酸银溶液 Cu + Ag+ = Cu2+ + Ag |
| D.大理石溶于盐酸 CaCO3 + 2 H+ = Ca2+ + H2O + CO2↑ |
下列化学反应可用离子方程式CO+2H+===CO2↑+H2O表示的是( )
| A.石灰水和盐酸反应 |
| B.难溶的碳酸盐和难电离的酸反应生成CO2和H2O |
| C.可溶性碳酸盐与强酸反应生成CO2和H2O |
| D.可溶性碳酸盐与任何酸反应生成CO2和H2O |
下列反应的离子方程式书写正确的是
| A.Na2O 溶于水:Na20+ H2O=2Na+ + 20H— |
| B.向 Ca(C10)2 溶液中通入过量 C02 : 2C10-+H20+C02=2HC1O+CO32- |
| C.用FeC13溶液腐蚀铜板:Fe3十十Cu=Fe2十十Cu2十 |
| D.碳酸钙溶于稀醋酸:CaCO3+2H+=Ca2++CO2 +H20 |
下列离子方程式书写正确的是( )
| A.铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑ |
| B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓ |
C.三氯化铁溶液中加入铁粉 |
| D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
下列离子方程式书写正确的是
| A.铁溶于盐酸中2Fe + 6H+ = 2Fe3+ + 3H2↑ |
| B.碳酸钠与硫酸溶液反应 CO32ˉ + H+ = CO2↑+ H2O |
| C.二氧化硫被烧碱溶液吸收SO2 +2OHˉ= SO32ˉ + H2O |
| D.铜与稀硝酸反应 Cu + 8H+ + 2NO3ˉ= Cu2+ + 2NO↑ + 4H2O |
下列反应的离子方程式书写正确的是 ( )
| A.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| B.稀 H2SO4与铁粉反应: 2Fe+6H+=2Fe3++3H2↑ |
| C.氢氧化钡溶液与稀 H2SO4反应:Ba2++SO42-=BaSO4↓ |
| D.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
下列指定反应的离子方程式正确的是
| A.氯化铝溶液中加入过量的氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| B.NaClO溶液中通入少量SO2 :3ClO-+SO2+H2O=Cl-+SO42-+2HClO |
| C.向稀NH4HCO3溶液中加入过量NaOH溶液:NH4++OH-=NH3·H2O |
| D.10 mL 0.5 mol·L-1的KAl(SO4)2溶液与20 mL 0.5 mol·L-1的Ba(OH)2溶液混合反应: |
3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓
下列表示对应化学反应的离子方程式不正确的是
| A.FeCl3溶液与Cu的反应:Cu+2Fe3+=Cu2++2Fe2+ |
B.向NaClO溶液中加入浓盐酸:ClO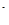 +Cl +Cl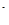 +2H+=Cl2↑+ H2O +2H+=Cl2↑+ H2O |
C.用氨水溶解Cu(OH)2:Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH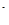 +4H2O +4H2O |
D.向NH4HCO3中滴加少量的NaOH溶液:NH +OH +OH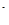 =NH3·H2O+H2O =NH3·H2O+H2O |
下列离子方程式书写正确的是
| A.氯气溶于水:Cl2+H2O═2H++Cl﹣+C1O﹣ |
| B.溴化钠溶液与氯气反应:2Br﹣+Cl2═2Cl﹣+Br2 |
| C.氢氧化钡溶液与稀硫酸反应:H++SO42﹣+Ba2++OH﹣═H2O+BaSO42﹣↓ |
| D.碳酸钙加入过量的盐酸中:CO32﹣+2H+═CO2↑+H2O |
下列叙述正确的是
| A.Na、Al、Fe金属单质在一定条件下与水反应都生成H2和对应的碱 |
| B.漂白粉和明矾都常用于自来水的处理,二者的作用原理不相同 |
| C.将SO2通入Ca(ClO)2溶液可生成CaSO3沉淀 |
| D.向FeCl2溶液中通入Cl2反应的离子方程式为:Fe2++Cl2═Fe3++2C1﹣ |
下列离子方程式正确的是( )
| A.硫酸铝溶液加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
| B.稀盐酸与碳酸钙反应:2H++CO32-=H2O+CO2↑ |
| C.硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ |
| D.稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑ |
常温下,取pH=2的 HA溶液与HB溶液各1 mL,分别加水稀释,测得pH变化与稀释倍数关系如图所示。下列叙述正确的是
A. 稀释前,c(HB) > c(HA)="0.01" mol·L-1
B. HB的电离方程式为HB=H++B-
C. NaA的水溶液中,离子浓度大小为:c(Na+)>c(A-)>c(OH-)>c(H+)
D. NaA、NaB的混合溶液中:2c(Na+)=c(A-)+c(B-)+c(HB)
下表是某铬酸(H2CrO4)溶液中离子浓度(mol.L-1)与pH的关系,下列说法不正确的是
| pH |
c(CrO42-) |
c(HCrO4-) |
c( Cr2O72-)] |
c(H2CrO4) |
| 4 |
0.0003 |
0.1040 |
0.4480 |
0 |
| 6 |
0.0319 |
0.0999 |
0.4370 |
0 |
| 7 |
0.2745 |
0.0860 |
0.3195 |
0 |
| 9 |
0.9960 |
0.0031 |
0.0004 |
0 |
A.铬酸的第一步电离是完全电离
B.铬酸的第二步电离是部分电离,且存在两种电离方式
C.当电离达到平衡时,2 (Cr2O72-)=
(Cr2O72-)= (HCrO4-)
(HCrO4-)
D.pH越大,电离出的CrO42-浓度越大
能正确表示下列化学反应的离子方程式的是
| A.氢氧化钡溶液与硫酸的反应 OH-+H+ = H2O |
| B.金属钠与热水反应 Na + H2O = Na++ OH- + H2 |
| C.铜片插入硝酸银溶液中 Cu +Ag+ = Cu2+ + Ag |
| D.碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2 |