目前,聚氯乙烯塑料(PVC)占塑料消费量的30%以上,BICM法用乙烯、氯气等为原料合成PVC,其工艺流程如下。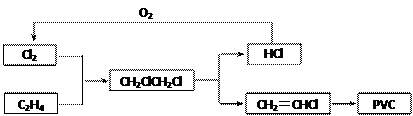
⑴一定条件下,HCl与O2反应制取Cl2的方法称为地康法,其热化学反应方程式为:
4HCl(g)+O2(g)  2Cl2(g)+2H2O(g) ΔH=-114.4kJ·mol-1。
2Cl2(g)+2H2O(g) ΔH=-114.4kJ·mol-1。
升高温度,该反应的化学平衡常数K会 ▲ 。
A.增大 B.减小 C.不变 D.无法确定
⑵一定温度下某体积可变的容器中充入4LHCl气体和6L空气(氧气占20%),充分反应后气体体积为9.2L。该反应中HCl气体的转化率为 ▲ 。
⑶假设BICM法中各步反应的转化率均为100%,计算生产1000吨PVC需要购得的氯气质量。
已知:①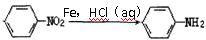 (弱碱性,易被氧化)
(弱碱性,易被氧化)
②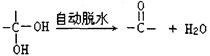
工业上以苯和C8H6O2Br2(显酸性)为原料合成一种产生电能的新型KEVLAR合成纤维,生产流程为: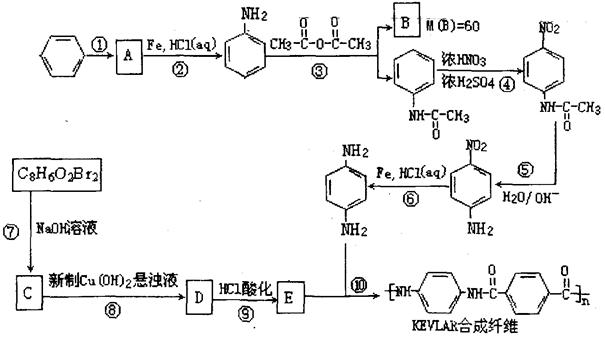
根据生产流程,回答下列问题:
(1)写出B的结构简式 ,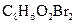 的结构简式 .
的结构简式 .
(2)写出反应①的化学方程式 .
(3)反应②④⑥⑧⑩中属于取代反应的是 ,设计反应③④⑤的目的是 .
(4)E与乙二醇发生聚合反应的化学方程式 .
由丙烯经下列反应可得到F、G两种高分子化合物,它们都是常用的塑料。
(1)聚合物F的结构简式是_____________________。
(2)D的结构简式是_____________________。
(3)B转化为C的化学方程式是__________________________________________。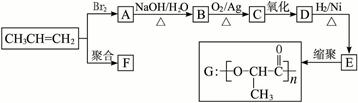
(4)在一定条件下,两分子E能脱去两分子水形成一种六元环化合物,该化合物的结构简式是_____________________。
(5)E有多种同分异构体,其中一种能发生银镜反应,1 mol 该同分异构体与足量的金属钠反应产生1 mol H2,则该同分异构体为_____________________。
 超细氧化铝是一种重要的功能陶瓷原料。
超细氧化铝是一种重要的功能陶瓷原料。
 (1)实验室常以
(1)实验室常以和
为原料,在一定条件下先反应生成沉淀
该沉淀高温分解即得超细
。
热分解的化学反应方程式。
 (2)
(2)的相对分子质量为453。欲配制100
为2、浓度约为0.1
的
溶液,配制过程为
 ①用托盘天平称量
①用托盘天平称量固体
;
 ②将上述固体置于烧杯中。
②将上述固体置于烧杯中。
 (3)在0.1
(3)在0.1溶液中,铝各形态的浓度(以
计)的对数(
)随溶液
变化的关系见下图


 ①用
①用溶液调节(2)中溶液
至7,该过程中发生反应的离子方程式有。
 ②请在答题卡的框图中,画出0.01
②请在答题卡的框图中,画出0.01溶液中铝各形态的浓度的对数
随溶液
变化的关系图,并进行必要的标注。
(1)化合物G 的相对分子质量为140,G 中含硅元素,其质量分数为60%,另有元素Y。
G 可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl 气体。
请推断:G 和E的化学式分别为______________、______________。
(2)粉末状G 能够与氧气反应,所得产物中有一种是空气中的主要成分,另一种是工业上生产玻璃的主要原料。请写出化合物G 与氧气反应的化学方程式
(3)常压下在G 中添加氧化铝,经高温烧结可制成一种高强度、超硬废、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表示为Si6-XAlXOXY8-X。在接近1700℃时x的极限值约为4.0,在1400℃时 x为2.0,以保持整个化合物呈电中性。推测:赛伦中以下元素的化合价:Si_______Y______,塞伦的晶体类型__________

 金属铝的生产是以
金属铝的生产是以为原料,在熔融状态下进行电解:

请回答下列问题:
 (1)冰品石(
(1)冰品石()的作用是。
 (2)电解生成的金属铝是在熔融液的(填"上层"或"下层")。
(2)电解生成的金属铝是在熔融液的(填"上层"或"下层")。
 (3)阴极和阳极均由材料做成;电解时所消耗的电极是(填"阳极"或"阴极")。
(3)阴极和阳极均由材料做成;电解时所消耗的电极是(填"阳极"或"阴极")。
 (4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成(填代号)。
(4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成(填代号)。
 a.冰品石 b.氧化铝 c.铝锭 d.硫酸铝
a.冰品石 b.氧化铝 c.铝锭 d.硫酸铝