电子工业使用的印刷线路板,是在敷有铜膜的塑料板上以涂料保护所需的线路,然后用FeCl3的溶液与未受保护的铜膜反应以去掉铜,腐蚀后的废液中含有大量的Cu2+。为了回收这一部分Cu2+并制成硫酸铜晶体(CuSO4·5H2O),常用如下步骤:
①向废液中加过量的铁屑,搅拌,静置;②滤出固体物质;③将滤出的固体物质加热煅烧;④把煅烧后的物质放在硫酸中溶解;⑤调节溶液的pH在3.4—4之间,使Fe(OH)3沉淀完全,过滤;⑥浓缩滤液,析出晶体;⑦将过滤得到的晶体溶解,再结晶。
(1)上述③步操作所得煅烧产物成分是_______________。
A.CuO B.CuO和FeO C.CuO和Fe2O3 D.CuO和Fe3O4
(2)上述第⑤步操作中,调节溶液的pH宜加入的物质是_______________。
A.氧化铜粉末 B.NaOH溶液 C.稀氨水 D.Na2CO3
(3)上述第⑥步操作中,用浓缩滤液而不用蒸干溶液的主要原因是_______________。
A.蒸干所得到的物质可能含有无水硫酸铜
B.温度升高CuSO4溶解度增大
C.温度升高Cu2+被还原为Cu
D.温度升高CuSO4分解
A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
A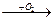 B
B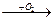 C
C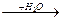 D
D
(1)若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,则A、D分别为(填写化学式)。
A.___________________,D.___________________。
写出A→B转化的化学方程式:___________________________________________________。
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红,则A为_______________。写出A→B转化的化学方程式:_______________________。
(3)若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,则A是_______________,B是_______________,C是_______________。C可作为呼吸面具的填充剂,C与二氧化碳发生反应的化学方程式为:______________________________________________________。A跟水发生反应的离子方程式为:________________________________________________。
(4)若A为常见的非金属单质,则A有多种情况,请填写下表,并完成相应的化学反应方程式。(可以不填满,也可以补充)
| 编号 |
A |
B→C化学方程式 |
| ① |
|
|
| ② |
|
|
| ③ |
|
|
下列制冷剂大量使用排放,会造成大气层中O3浓度下降的是( )
| A.干冰 | B.液态NH3 | C.液态N2 | D.氟氯烃(如CF2Cl2) |
下列离子方程式正确的是( )
| A.水中加入过氧化钠固体: 2H2O+2 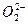 ====O2↑+4OH- ====O2↑+4OH- |
| B.等物质的量的氢氧化钡溶液与明矾溶液混合: 3Ba2++6OH-+2Al3++3 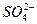 ====3BaSO4↓+2Al(OH)3↓ ====3BaSO4↓+2Al(OH)3↓ |
| C.氢氧化镁与稀硫酸反应: H++OH-====H2O |
| D.单质铜与稀硝酸反应: |
Cu+2H++2 ====Cu2++2NO↑+H2O
====Cu2++2NO↑+H2O
如右图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入一定量氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,对原来试管中盛装的气体判断不正确的是( )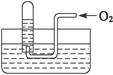
| A.可能是空气与NO2的混合气体 |
| B.可能是O2与NO2的混合气体 |
| C.可能是NO与NO2的混合气体 |
| D.可能是NO2一种气体 |
下列各组物质仅用水及物质间相互反应就能区别的一组是( )
| A.Na2O2 Al2(SO4)3 MgCl2 K2CO3 |
B.BaCl2 Na2SO4 CaCO3 KOH |
| C.AgNO3 NaCl KCl CuCl2 | |
| D.Fe2(SO4)3 K2CO3 K2SO4 BaCl2 |
为了测定某铜银合金的组成,将30.0 g合金溶于80 mL 13.5 mol·L-1的浓硝酸中,待合金完全溶解后,收集到气体6.72 L(标准状况),并测得溶液中H+的物质的量浓度为1 mol·L-1,假设反应后溶液的体积仍为80 mL,计算:
(1)被还原的硝酸的物质的量。
(2)合金中银的质量分数。
如右图所示,锥形瓶中盛有气体X,滴管内盛有液体Y。若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起。气体X和液体Y不可能是( )
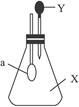
| A.X是NH3,Y是水 |
| B.X是SO2,Y是NaOH浓溶液 |
| C.X是CO2,Y是稀H2SO4 |
| D.X是HCl,Y是NaNO3稀溶液 |
已知硫氰(SCN)2、氰气(CN)2和Cl2性质相似。试完成下列反应:
(1)(CN)2+NaOH→___________________________________________________________。
(2)MnO2+HSCN→
_____________________________________________________________。
实验室里化学试剂的保存方法是不相同的,下图中A、B、C、D是常见的一些保存药品的试剂瓶。请把下列常见试剂的序号填写在各试剂瓶下面的括号内:①浓硫酸②碳酸钠溶液③大理石④酒精⑤氯水⑥浓硝酸
| A |
B |
C |
D |
 |
 |
 |
 |
| ( ) |
( ) |
( ) |
( ) |
下列溶液中加入氯化钡溶液生成白色沉淀,在加入稀硝酸震荡,白色沉淀不消失的是
| A.Na2SiO3 | B.Na2CO3 | C.Na2SO3 | D.Na3PO4 |
在一定条件下可实现下图所示物质之间的变化
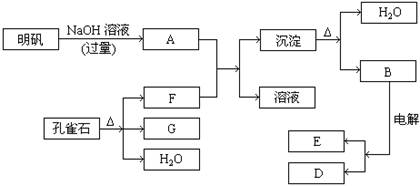
请填写以下空白:
(1)孔雀石的主要成份是CuCO3·Cu(OH)2(碱式碳酸铜)受热易分解。上图中的F是 。
(2)写出明矾溶液与过量的NaOH溶液反应的离子方程式
(3)图中所得G和D都为固体混合后在高温下可发生反应写出该反应化学方程式 。
(4)每生成1mol D同时生成 mol E。
某地有一池塘,生长着丰富的水生植物和多种鱼虾。后来,由于化工厂将大量污水排入池塘中,使水质恶化,各种水生生物先后死亡。根据题意回答下列问题:
(1)从生态平衡角度看,池塘这种变化说明了 。
(2)造成这种变化的原因是 。
(3)经检测,污水中含有0.012 mol·L-1的游离溴。可用亚硫酸钠除去污水中的溴,请写出其化学方程式 。
(4)处理这种污水5 L,需加入0.05 mol·L-1的亚硫酸钠__________L,才能将溴全部除去。
(5)要使池塘恢复本来面目.首先要解决的问题是__________.首先要恢复的生物是__________。