甲烷的氯化反应式为:
(1)在链增长的第二部反应中形成的化合物的电子式为 ;
(2)在反应机理的三个阶段破坏或形成的化学键类型均为 ;
(3)在短周期主族元素中,氯元素及与其相邻元素的电负性有大到小的顺序是 (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第 周期 族。
(4)链引发的反应为 ;链终止的反应为 (填“吸热”或“放热”)
(5)卤素单质及化合物在许多物质上都存在着递变规律。下列有关说法正确的是 。
a.相同条件下卤化银的Ksp按AgCl、AgBr、AgI 的顺序依次增大
b.卤化氢溶入水的酸性按HF、HCl、HBr、HI的顺序依次减弱
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质氧化性按F2、Cl2、Br2、I2的顺序依次减弱
(6)卤化氢的键能与键长大小如下表。
| |
HF |
HCl |
HBr |
HI |
| 键能/kJ·mol-1 |
568.6 |
431.8 |
365.7 |
298.7 |
| 键长/pm |
92 |
127.6 |
141.0 |
162 |
由上表数据可以推断:
①卤素单质非金属性越强,与氢化合生成的氢化物越 (填“稳定”或“不稳定”)。
②卤化氢的键长与卤离子的半径的关系是: 。
2009年12月7日~18日在丹麦首都哥本哈根召开了世界气候大会,商讨《京都议定书》一期承诺到期后的后续方案,即2012年至2020年的全球减排协议,大会倡导“节能减排” 和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。过渡排放CO2会造成“温室效应”,科学家正在研究如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应: CO2(g)+3H2(g)
CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化: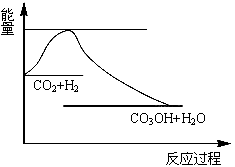
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),经测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),经测得CO2和CH3OH(g)的浓度随时间变化如图所示。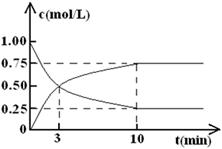
①从反应开始到平衡,CO2的平均反应速率v(CO2)= 。
②该反应的平衡常数表达式K= 。
③下列措施中能使化学平衡向正反应方向移动的是 (填字母)。
A.升高温度
B.将CH3OH(g)及时液化抽出
C.选择高效催化剂
D.再充入l molCO2和3 molH2
(3)25℃,1.01×105Pa时,16g液态甲醇完全燃烧,当恢复到原状态时,放出369.2kJ的热量,写出该反应的热化学方程式:___________________________________________。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极应加入或通入的物质有__________ _____;其正极的电极反应式是:_____________________________________。
为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究性学习:
【查阅资料】金属活泼性不同,其硝酸盐分解产物不同
(1)K→Na活泼金属的硝酸盐分解生成亚硝酸盐和氧气;
(2)Mg→Cu等较活泼金属的硝酸盐分解生成氧化物、NO2和O2;
(3)Hg以后不活泼金属的硝酸盐分解生成金属、NO2和O2。
2KNO3 2KNO2↑+O2↑ 2Cu(NO3)2
2KNO2↑+O2↑ 2Cu(NO3)2 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑
2AgNO3 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
【实验一】探究Fe(NO3)2热分解固体产物中Fe元素的价态。该小组甲同学将其溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验。
【提出猜想】
猜想一:Fe元素只显+2价;
猜想二:Fe元素只显______价;
猜想三:Fe元素_________。
【实验操作】①向一份溶液中滴入KSCN溶液;②稀酸性KMnO4溶液中滴入另一份溶液。
【实验现象】实验① ;实验② 。
【实验结论】猜想二成立,则Fe(NO3)2分解的化学方程式是 。
【实验二】探究Fe(NO3)2热分解气体产物的性质。小组乙、丙同学进行了如下图所示的实验(收集时操作恰当,几乎没有空气)
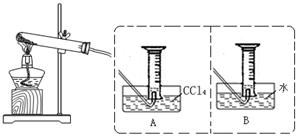
实验步骤:①连接仪器;②检查装置气密性;③取一定质量Fe(NO3)2装于大试管,并重新连接好仪器;④加热;⑤……
(1)乙同学使用A装置收集气体,恰好收集到27mL红棕色气体,要从水槽中取出量筒,乙同学的正确操作方法是 。
(2)乙同学用带火星木条检验量筒内气体时,发现木条燃烧,下列判断中正确的是 。
a.气体中只有NO2 b.气体是O2、NO2的混合物
c.支持燃烧的气体只有O2 d.NO2支持燃烧
(3)丙同学取等质量的Fe(NO3)2使用B装置收集气体,可收集到 mL气体。
【实验三】探究固体混合物的成分。小组丁同学取KNO3、Cu(NO3)2、Fe(NO3)2的混合粉末充分加热后用排水法未收集到任何气体,则KNO3、Cu(NO3)2、Fe(NO3)2的物质的量之比可能是 ( )
| A.1:2:2 | B.2:1:3 | C.1:2:3 | D.3:8:6 |
下列叙述正确的是( )
| A.向体积为Va的0.02mol·L-1CH3COOH溶液中加入体积为Vb的0.02mol·L-1NaOH溶液,Va>Vb时:c (CH3COOH)+c(CH3COO-)>c (Na+) |
| B.将0.2 mol·L-1的盐酸与0.1 mol·L-1的KAlO2溶液等体积混合,其溶液中离子浓度由小到大的顺序为:c(OH-)<c(Al3+)<c(H+)<c(K+)<c(Cl-) |
| C.pH=5的HCOOH溶液和pH=5的NH4NO3溶液中,c(H+)不相等 |
| D.25℃时,pH=4,浓度均为0.1mol·L-1的CH3COOH、CH3COONa混合溶液: |
c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)
下图所示物质(部分产物和反应条件未标出)中,只有A是单质,常温下B和C呈气态,且B是导致酸雨的大气污染物,D是氧化物,W是淡黄色固体。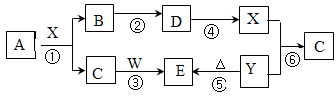
据此回答下列问题:
(1)B、C、D的化学式分别为:B 、C 、D ;从物质分类角度,上图所给物质中属于钠盐的是 (填写化学式)。
(2)上图所给物质在6个反应中只做还原剂的有 (填写化学式)。
(3)上图反应中不属于氧化还原反应的有 (填写序号)。
(4)写出A和X反应的化学方程式 ;若生成的B在标准状况下的体积为22.4L,则参加反应的A的物质的量为 ,反应中转移的电子数目为 。
(5)请写出C和W反应的化学方程式: 。
(6)请写出X和 Y反应的离子方程式: 。
物质A经下图所示的过程转化为含氧酸D,D为强酸,请回答下列问题:
(1)若A在常温下为气体单质则回答:
①A、C的化学式分别是:A________;C________。
②将C通入水溶液中,反应化学方程式为________________________。
(2)若仅A、B在常温下为气体且为化合物, 则回答:
①A的化学式是:A________。
②B生成C的化学方程式为________________________。
③一定条件下碳单质与D反应的方程式为________________________,该反应中D起到的作用是________________.
(3)若A在常温下为固体单质则回答:
①D的化学式是________;
②向含2mol D的浓溶液中加入足量的Cu加热,标准状况下产生的气体体积_______22.4L(填“大于”“等于”或“小于”),原因为_________________________________。
(10分)(1)物质的量各为1mol的钠、镁、铝与1mol·L-1的盐酸100mL反应,在相同条件下产生氢气的体积之比是______。等物质的量的Na2CO3和NaHCO3与足量的盐酸反应,在相同条件下产生二氧化碳的体积之比是__________。
(2)除去FeCl2溶液中少量的FeCl3最好加入_________物质,离子方程式为_____________。
除去SO2气体中少量的HCl最好加入_________物质,离子方程式为________________。
(3)鉴别Na2CO3和NaHCO3溶液可选用_________。(填序号)①CaCl2 ②Ca(OH)2 ③BaCl2
(4)下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是____________。(填序号)
① NaAlO2 ②(NH4)2CO3 ③Na2CO3 ④Al(OH)3 ⑤Ca(OH)2 ⑥NaHSO3
X、Y、Z是三种常见元素的单质,甲、乙是两种常见的化合物,这些单质和甲乙化合物之间存在如图所示的关系。下列说法一定正确的是
| A.X、Y、Z都是非金属单质 |
| B.X、Y、Z中至少有一种是金属单质 |
| C.若X、Y为金属单质,则Z必为非金属单质 |
| D.若X、Y为非金属单质,则Z必为金属单质 |
某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究。
[实验一]取样品0.100 g,用右图所示实验装置进行测定。(夹持装置省略)
(1)检查装置A气密性的方法是 。
(2)若在实验过程中共产生气体11.20 mL(已折算成标准状况),则样品中Na2O2的纯度为 。
[实验二]样品溶于水后用盐酸滴定
(3)取一定量样品溶于水并稀释至250 mL,配制时,所用到的玻璃仪器除了烧杯和玻璃棒外,还需用到 。
(4)取上述所配溶液各25.00 mL,用一定浓度的标准盐酸滴定,平行实验记录如下表:
| 实验次数 |
第一次 |
第二次 |
第三次 |
第四次 |
| 标准盐酸体积(mL) |
23.00 |
24.98 |
25.00 |
25.02 |
由表中数据可知,标准盐酸体积的平均值为 mL。若滴定前用上述所配溶液润洗锥形瓶,对测定盐酸体积产生的影响是 (填“偏高”、“偏低”或“无影响”)。
[实验分析]实验结果对比分析
(5)小组同学对比两个实验发现,实验一测得的Na2O2样品的纯度比理论值明显偏小。经过分析,小组同学认为,明显偏差不是由操作失误和装置缺陷引起的,可能是反应原理上的原因。查阅资料发现:
Na2O2与水反应产生的H2O2未完全分解。
①写出Na2O2与水生成H2O2的化学方程式 。
②若将实验一稍加改进,就能使测定结果接近理论值,写出改进方案: 。
镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害。某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下: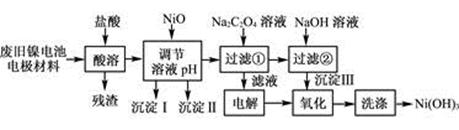
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②已知实验温度时的溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O
③某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如下表所示:
| M(OH)n |
Ksp |
开始沉淀pH |
沉淀完全pH |
| Al(OH)3 |
1.9×10-23 |
3.4 |
4.2 |
| Fe(OH)3 |
3.8×10-38 |
2.5 |
2.9 |
| Ni(OH)2 |
1.6×10-14 |
7.6 |
9.8 |
回答下列问题:
(1) 用NiO调节溶液的pH,依次析出沉淀Ⅰ________和沉淀Ⅱ__________(填化学式)。
(2) 写出加入Na2C2O4溶液的反应的化学方程式:
。
(3) 检验电解滤液时阳极产生的气体的方法:
。
(4) 写出“氧化”反应的离子方程式:
。
(5) 如何检验Ni(OH)3已洗涤干净?
。
现有某金属硝酸盐的化学式为M(NO3)2,为了探究其热分解产物,某化学小组开展探究性学习:
【查阅资料】金属活泼性不同,其硝酸盐分解产物不同。如,2KNO3 2KNO2+O2↑,
2KNO2+O2↑,
2Cu (NO3)2 2CuO+4NO2↑+O2↑, 4AgNO3
2CuO+4NO2↑+O2↑, 4AgNO3 4Ag+4NO2↑+2O2↑
4Ag+4NO2↑+2O2↑
【提出猜想】猜想1 M(NO3)2 M(NO2)2+O2↑
M(NO2)2+O2↑
猜想2 2 M(NO3)2 2MO+4NO2↑+O2↑
2MO+4NO2↑+O2↑
猜想3 。
【设计实验】为了探究上述猜想,设计如下实验装置:
【实验步骤】①连接仪器;②检查装置气密性;③取一定量样品装入大试管中,并重新连接好仪器;④加热;⑤……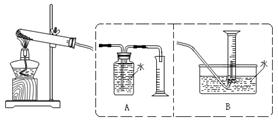
⑴写出猜想3的化学方程式: ;
⑵测定气体体积应选择 (填A或B);不选另一个装置的理由是
;
⑶实验收集到一定量气体是 ,量筒读数前应注意 ;
为了检验收集气体的成分,其操作方法是
;
⑷在实验后量筒里的水中加入适量碳酸氢钠粉末,溶液中产生大量气体,说明 正确(填“猜想1”、“猜想2”或“猜想3”);
⑸该小组测得两组数据:①实验前样品质量为Wg,收集到气体体积为V L;②实验前
样品质量为Wg,完全分解后测得固体产物质量为m g;
请你选择其中一组数据,计算元素M的相对原子质量为 。
芳香化合物A、B互为同分异构体B的结构简式是CH3COO- -COOCH2CH3,A经①、②两步反应得C、D和E,B经①、②两步反应得E、F和H。上述反应过程、产物性质及相互关系如下图所示:
-COOCH2CH3,A经①、②两步反应得C、D和E,B经①、②两步反应得E、F和H。上述反应过程、产物性质及相互关系如下图所示:
(1)B可以发生的反应类型有(填序号) 。
①加成反应 ②酯化反应 ③消去反应 ④取代反应 ⑤聚合反应
B的核磁共振氢谱中会出现_______个峰。
(2)E中含有官能团的名称是 。
(3)A有两种可能的结构,其对应的结构简式为 , 。
(4)B、C、D、F、G化合物中互为同系物的是 。
(5)F与H在浓硫酸作用下加热时发生反应的方程式为:
。
提示:某些金属氧化物跟熔融烧碱反应可生成盐。根据以下化学反应框图填空:
(1)单质F的化学式为 。 (2)溶液I中所含金属离子是 。
(3)由E生成G的反应类型为 , ;
A和B的混合物称为 。
(4)写出下列离子方程式: C+L ;
H转变成I ;
I转变成J ;
(5)由C→E+F若改用浓酸,则不能选用的浓酸是(写分子式) 。
下列反应的离子方程式正确的是( )
| A.向Ba(OH)2溶液加入等物质的量的硫酸:Ba2++2OH-+SO42-+2H+= BaSO4↓+2H2O |
| B.BaCO3溶于醋酸:BaCO3+2H+=Ba2++H2O+CO2↑ |
| C.将C12通入水中:C12+H2O=Cl-+2H++ClO - |
| D.向Na2CO3溶液中通入过量CO2气体:CO32-+CO2+H2O=HCO3- |
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)B的氢化物的分子空间构型是 。其中心原子采取 杂化。
(3)写出化合物AC2的电子式 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为 。
(4)E的核外电子排布式是 ,ECl3形成的配合物的化学式为 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 。