在一定温度下,在一体积固定的密闭容器中加入2 mol X和1 mol Y,发生如下反应:2X(g)+Y(g) aZ(g)+W(g) ΔH=-QkJ/mol(Q>0)
aZ(g)+W(g) ΔH=-QkJ/mol(Q>0)
当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;
平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)温度升高,平衡常数K的值是__________(填“增大”、“减小”或“不变”)。
(2)化学计量数a的值为__________。
(3)有同学认为,Q1一定小于Q,你认为该结论是否正确?__________,其理由是____________________。
(4)维持温度、体积不变,若起始时向容器中加入的物质的量如下列各项,反应达到平衡后放出的热量仍为Q1 kJ的是__________(稀有气体不参与反应)。
| A.2 mol X、1 mol Y、1 mol Ar | B.a mol Z、1 mol W |
| C.1 mol X、0.5 mol Y、0.5a mol Z、0.5 mol W | D.2 mol X、1 mol Y、1 mol Z |
中学化学中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡4种,且均符合平衡移动原理。请回答下列问题:
(1)现将4 mol SO2和2 mol O2充入固定容积为2 L的密闭容器中,500 ℃进行反应并保持温度不变,反应达到平衡。若在温度不变的条件下,再向平衡体系中加入2 mol SO2、2 mol O2与4 mol SO3,平衡将向________移动。
(2)常温下,取pH=2的盐酸和醋酸各100 mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸pH变化曲线的是________(填“A”或“B”)。设盐酸中加入的Zn粒质量为m1,醋酸中加入的Zn粒质量为m2。则m1________m2(填“<”、“=”或“>”)。
(3)难溶电解质在水溶液中存在溶解平衡。在常温下,溶液中各离子浓度以它们化学计量数为指数的乘积是一个常数,叫溶度积常数(Ksp)。当溶液中各离子浓度指数的乘积大于溶度积时,则产生沉淀,反之固体溶解。若某CuSO4溶液中c(Cu2+)=0.02 mol·L-1,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于________(已知Ksp=2.0×10-20)。
(4)常温下,向某纯碱溶液中滴入酚酞,溶液呈红色,则该溶液呈________性。在分析该溶液遇酚酞呈红色的原因时,甲同学认为是配制溶液时所用的纯碱样品中混有NaOH所致;乙同学认为是溶液中电离出的CO32-水解所致,请你设计一个简单的实验方案给甲和乙两位同学的说法进行评判(包括简要操作、现象和结论):_________________。
已知一个碳原子上连有两个羟基时,易发生下列转化: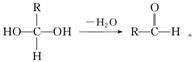
已知:A、B存在如图转化关系。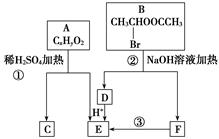
请据图回答:
(1)物质B能发生的反应类型是________。(填序号)
A.取代反应 B.水解反应 C.消去反应
(2)已知在相同情况下,等质量氢气的体积是A蒸气的81倍,16.2 g A在氧气中完全燃烧,生成44g CO2和9 g H2O,则A的化学式为________。
(3)C具有如下特点:能跟FeCl3溶液发生显色反应;能发生加聚反应;苯环上的一氯代物只有两种。写出反应①的化学方程式:______ 。
(4)化合物G是C的同分异构体,它属于芳香族化合物,能发生银镜反应。G有多种结构,写出其中只有一个取代基的同分异构体的结构简式:______ 。
(1)控制变量是科学研究中的重要研究方法,其基本思路是,在实验研究中人为只改变一个因素(调节变量),其他因素保持相同,观察测定因调节变量改变而改变的因素(因变量),从而分析得到研究结论。中学化学中应用控制变量的方法研究问题的例子很多。请分析或设计:
①在研究浓度对化学反应速率的影响时,教材安排了利用Na2S2O3与H2SO4反应的一组对照实验(Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O)
| 烧杯 编号 |
加3% Na2S2O3溶液体积(mL) |
加H2O体积(mL) |
加(体积之比为1∶2)H2SO4溶液体积(mL) |
所需时间(s) |
| 1 |
5 |
5 |
2 |
|
| 2 |
7 |
3 |
2 |
|
| 3 |
10 |
0 |
2 |
|
在三个烧杯(底部有黑色“十”字标记)内分别加入表中所示体积的三种液体,搅拌并开始计时,到出现浑浊使烧杯底部“十”字看不见时停止计时。比较所需时间,得出浓度对化学反应速率影响的结论。实验中,温度和反应体系中硫酸浓度是保持相同的因素,调节变量是____________________,因变量是______________。
②运用控制变量原理设计实验,利用纯碱溶液探究温度对盐的水解的影响,简述实验方法:________________________________________________________________________。
(2)373 K时,H2PO3-与OH-发生如下反应:
H2PO3-+OH-HPO32-+H2O
反应结果如表所示:
| H2PO3-起始浓度(mol/L) |
0.10 |
0.50 |
0.50 |
| OH-起始浓度(mol/L) |
1.00 |
1.00 |
4.00 |
| 反应速率[mol/(L·s)] |
3.2×10-5 |
1.60×10-4 |
2.56×10-3 |
如果用v=kcm(H2PO3-)·cn(OH-)表示反应速率(k为与浓度无关的常数)
①k=________,m=________,n=________。
②若c(H2PO3-)的起始浓度为0.20 mol/L,c(OH-)的起始浓度为1.50 mol/L,则反应速率v=________。
有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶液,且它们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用蘸有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其他五种溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化;F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1)能确定的溶液是(写出溶液标号与相应溶质的化学式):
_________________________________________________________________;
(2)不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:_________________________________________________________________。
常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1 CH3COOH溶液所得滴定曲线如下图。下列说法正确的是( )。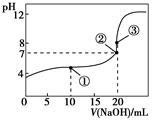
| A.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) |
| B.点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) |
| C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
淡黄色固体X和气体A存在如下转化关系:
请回答下列问题:
(1)固体X的名称 ;A的化学式 。
(2)写出反应①③的化学方程式,并指出氧化剂。
反应① , 。
反应③ , 。
(3)写出②④反应的离子方程式:
反应② 。
反应④ 。
从石油裂解中得到的1,3—丁二烯可进行以下多步反应,得到重要的合成橡胶和杀菌剂富马酸二甲酯。
(1)写出D的结构简式 。
(2)写出A的结构简式 。
(3)写出第⑦步反应的化学方程式 。
(4)写出富马酸的一种相邻同系物的结构简式 。
(5)写出第⑨步反应的化学方程式 。
(6)以上反应中属于消去反应的是 。(填入编号)
乳酸(CH3—CHOH—COOH)是人体生理活动的一种代谢产物,其聚合物(聚乳酸)是一种新型可生物降解的高分子材料,主要用于制造可降解纤维、可降解塑料和医用材料。下图是工业上用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物。
物质H的结构简式为 ,回答下列问题:
,回答下列问题:
(1)写出下列物质的结构简式:C ,F 。
(2)上述反应①~⑦中,②是 反应,⑥是 反应。(填反应类型)
(3)写出下列反应的化学方程式:
① 。
⑦ 。
(4)隐形眼镜的制作材料,应具有良好的光学性能、良好的透气性能和亲水性。一般采用G来制作隐形眼镜而不用H,其主要理由是 。
下表是不同温度下水的离子积数据:
| 温度 / ℃ |
25 |
t1 |
t2 |
| 水的离子积常数 |
1×10-14 |
α |
1×10-12 |
试回答下列问题:
(1)若25<t1<t2,则α________1×10-14(填“>”“<”或“=”),作出此判断的理由是________________________________________________________。
(2)已知25℃时饱和NaHCO3溶液的PH>7,则此温度下饱和NaHCO3溶液中各离子浓度关
系正确的是______________
A.c(Na+)>c(HCO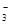 )>c(OH-)>c(H+)>c(CO
)>c(OH-)>c(H+)>c(CO )
)
B.c(Na+)+c(H+)=c(HCO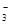 )+c(CO
)+c(CO )+c(OH-)
)+c(OH-)
C.c(Na+)=c(HCO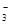 )+c(CO
)+c(CO )+c(H2CO3)
)+c(H2CO3)
D.c(OH-)=c(HCO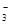 )+c(H2CO3)+c(H+)
)+c(H2CO3)+c(H+)
(3)t2℃下,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=___________。此溶液中各种离子的浓度由大到小的排列顺序是____________________。
已知可逆反应CO + H2O (g) CO2 + H2,在830K温度下达到平衡。
CO2 + H2,在830K温度下达到平衡。
(1)其化学平衡常数K的表达式为K= 。
(2)830K时,若起始时:c (CO) = 2 mol/L,c (H2O) = 3 mol/L,平衡时CO的转化率为60%,水蒸气的转化率为______________;K值为______________。
(3)830K,若只将起始时c (H2O)改为6 mol/L,则水蒸气的转化率为____________。
(4)若830K时,起始浓度c (CO)=a mol/L,c (H2O)=b mol/L,H2的平衡浓度c (H2)=c mol/L,
①a、b、c之间的关系式是____________________________________;
②当a = b时,a= ________c。
香豆素是用途广泛的香料,合成香豆素的路线如下(其他试剂、产物及反应条件均省略):
(1)Ⅰ的分子式为_____________;
(2)反应②的反应类型是_____________,反应④的反应类型是_____________。
(3)香豆素在过量NaOH溶液中完全水解的化学方程式为_______________________。
(4)Ⅴ是Ⅳ的同分异构体,Ⅴ的分子中含有苯环且无碳碳双键,苯环上含有两个邻位取代基,能发生银镜反应。Ⅴ的结构简式为_______________(任写一种)。
(5)一定条件下, 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为_____________。
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为_____________。
在容积固定不变的密闭容器中,可逆反应:A2(g)+B2(g) nC(g)符合下列图1所示关系。由此推断,对图Ⅱ的说法不正确的是( )
nC(g)符合下列图1所示关系。由此推断,对图Ⅱ的说法不正确的是( )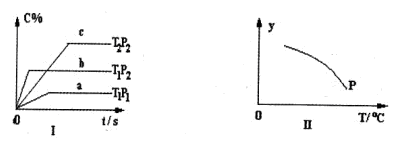
| A.Y轴表示A2的转化率 | B.Y轴表示C的浓度 |
| C.Y轴表示混合气体的密度 | D.Y轴表示混合气体的平均摩尔质量 |
B、D是常见金属单质,A是一种红棕色金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体。
(1)在E的溶液中加入氢氧化钠溶液,可以观察到的现象是________________________.
(2)按要求写化学方程式或离子方程式:
①A与B在高温条件下生成C和D的化学方程式:____________________________;
②在E的水溶液中通入氯气后的生成物和I溶液反应的离子方程式: 。
(3)由D和A组成的混合物与稀HCl作用,固体恰好溶解,所得溶液中滴加KSCN溶液不显红色,且生成的E与H2的物质的量之比为4:1。则反应物中A、D、HCl的物质的量之比为____。
Ⅰ:某些化学反应可表示为:A+B→C+D+H2O,请回答下列问题:
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,该反应离子方程式为 。
(2)若A为淡黄色固体,C为无色的气体,则该反应的离子方程式为 。
(3)若A、C、D均是铁的化合物,B是稀硫酸,则A与B反应的化学方程式为 。
Ⅱ:某些化学反应可表示为:A+B+H2O→C+D。请回答下列问题:
(1)若A为非金属单质,C为非金属单质,写出符合要求的化学反应方程式
(2)若A为金属单质,C为非金属单质,写出符合要求的离子方程式_____________________.