某化学课外活动小组设计实验探究氨气的化学性质,装置如下图所示(A装置未画出),其中A为气体发生装置。A中所用试剂,从下列固体物质中选取: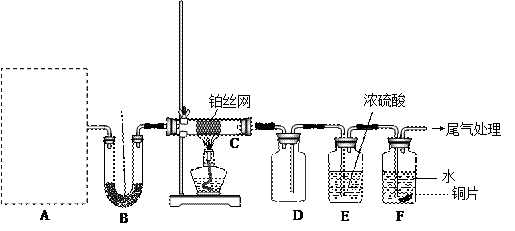
a. NH4HCO3 b. NH4Cl c. Ca(OH)2 d. NaOH 检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。
(1)实验室制取A中气体时若只用一种试剂,该试剂是_______(填代表备选试剂的字母);此时A中反应的化学方程式_______ ,A中主要的玻璃仪器有_______(填名称)。
(2)C中发生反应的化学方程式为_______,该反应是_________反应(填“吸热”或“放热”)。
(3)浓硫酸的作用____________________;铜片溶解的化学方程式_________________.
(4)待实验结束后,将B中固体混合物溶于500 mL 1 mol·L-1的盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是_______ mol。
m g铝镁合金与一定浓度的稀硝酸恰好完全反应(假定硝酸的还原产物只有NO)向反应后的混合溶液中滴加a mol/L NaOH溶液,当滴加到V mL时,得到沉淀质量恰好为最大值n g,则下列有关该实验的说法中正确的有 ( )
①沉淀中氢氧根的质量为(n—m)g
②恰好溶解后溶液中的NO 3-离子的物质的量为aVmol
③反应过程中转移的电子的物质的量为
④生成NO气体的体积室温下为
⑤与合金反应的硝酸的物质的量为
| A.2项 | B.3项 | C.4项 | D.5项 |
下列框图中的A—J是中学化学中常见的八种物质,所有物质均由短周期元素组成,已知常温、常压下D为无色液体, C、E、G均为气体单质,B为金属,I是由3个原子组成的一元含氧弱酸分子, A—J可发生如下转化: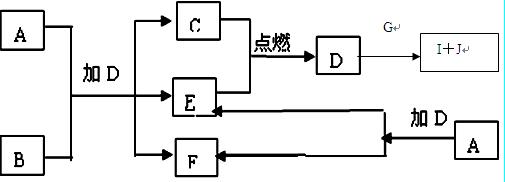
请填写下列空白:
⑴G的名称为 ,F的电子式为 。
⑵15.6gA与D完全反应,转移的电子的物质的量为 。
⑶常温下,A为一种 色的固体,它的一种重要用途是  。
。
⑷写出D、G反应转化为I和J的离子方 程式
程式  。
。
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代。处理有氰电镀的废水时,可在催化剂Ti O2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中
O2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中 用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。
用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。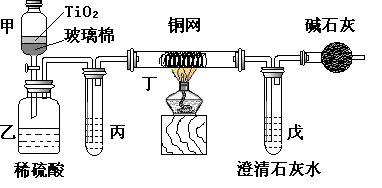
将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol·L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶 液全部放入乙中,关闭活塞。回答下列问题:
液全部放入乙中,关闭活塞。回答下列问题:
⑴乙中反应的离子方程式为______________ ___________。
⑵乙中生 成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是__ __(填字母)
成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是__ __(填字母)
a.饱和食盐水 b.饱和NaHCO3溶液 c.浓NaOH溶液 d.浓硫酸
⑶丁在实验中的作用是_____ __________________,
装有碱石灰的干燥管的作用是___________ ___________。
⑷戊中盛有含Ca(OH)20.02mol的石灰水,若实
 验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于___ _____,请说明该测得值与实际处理的百分率相比偏高还是偏低_ ___?简要说明可能的原因________________________ _________ _________。
验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于___ _____,请说明该测得值与实际处理的百分率相比偏高还是偏低_ ___?简要说明可能的原因________________________ _________ _________。
⑴某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应中还原产物是____;若反应过程中转移了0.3moL电子,则氧化产物的质量是__ g。
⑵将a mol Cl2 通入含b mol FeBr2的溶液中,
当0< a / b≤1/2 时,反应的离子方程式为: 2Fe2+ + Cl2 = 2Fe3+ + 2Cl- ,
写出另2个可能发生的离子方程式:
① 当 a / b =1时,_______________________ ______;
② 当a / b≥3/2时,________________ _____________。
⑶观察如下反应,总结规律,然后完成下列问题:
① Al(OH)3 +H2O Al(OH)4- + H+ ②NH3+H2O
Al(OH)4- + H+ ②NH3+H2O NH4+ + OH_
NH4+ + OH_
Ⅰ.已知B(OH)3是一元弱酸,试写出其电离方程式________________________ __
Ⅱ.N2H4是二元弱碱,试写出其第二步电离方程式___________ _________________
标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为ρ g/ml,质量分数为W,物质的量浓度为c mol/L,则下列关系中不正确的是 ( )
| A.W="17c/" (1000ρ) | B.ρ=(17V+22400)/(22.4+22.4V) |
| C.W="17V/(17V+22400)" | D.c=1000Vρ/(17V+22400) |
用Pt电极电解含有各0.1mol的Cu2-和X3+的溶液,阴极析出固体物质的质量m(g)与溶液中通过电子的物质的量n (mol)的关系见图示。
则离子的氧化能力由大到小排列正确的是: ( )
| A.Cu2+>X3+>H+ | B.Cu2+>H+>X3+ |
| C.X3+>H+>Cu2+ | D.H+>X3+>Cu2+ |
某强碱性溶液中可能含有的离子是K+、NH4+、Al3+、AlO2-、SO42-、SiO32-、CO32-、Cl-中的某几种离子,现进行如下实验:
①取少量的溶液用硝酸酸化后,加Ba(NO3)2溶液,无沉淀生成.
②另取少量溶液加入盐酸,其现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
(1)原溶液中肯定存在的离子是________________,肯定不存在的离子是____________
(2)已知一定量的原溶液中加入5 mL 0.2 mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187 g,则原溶液中是否含有Cl-?_________________.
(3)按照反应顺序逐步书写出②中发生反应的离子反应方程式①H++OH-=H2O
②
③
④HCO3-+H+=H2O+CO2
⑤
工业盐中含有NaNO2,外观和食盐相似,有咸味,人若误食会引起中毒,致死量为0.3g—0.5g.已知NaNO2能发生如下反应:aNO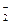 +xI—+yH+=bNO↑+cI2+zH2O,
+xI—+yH+=bNO↑+cI2+zH2O,
请回答下列问题:
(1)上述反应中,x、y、z的数值分别是 (全对才给分),
(2)根据上述反应,可用化学试纸和生活中常见物质进行实验来鉴别工业盐和食盐,现有碘化钾淀粉试纸,则还需选用的生活中常见物质的名称为 .
(3)某工厂废切削液中含有2%—5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2转化为不引起污染的N2,该物质是 ,
a.NaCl b.H2O2 c.NH4Cl d.浓H2SO4
所发生反应的离子方程式为: .
两种硫酸溶液,一种物质的量浓度为C1 mol/L,密度为ρ1 g/cm3,另一种物质的量浓度为C2 mol/L,密度为ρ2 g/cm3,当它们等体积混合后,溶液的密度为ρ3 g/cm3,则混合溶液的物质的量浓度为
( )
A. |
B. |
C. |
D.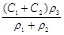 |
某含铬[Cr2O72-] 废水用硫酸亚铁铵[FeSO4·(NH4)2 SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀.该沉淀干燥后得到n molFeO·FeyCrxO3.不考虑处理过程中的实际损耗,下列叙述错误的是 ( )
| A.消耗硫酸亚铁铵的物质量为n(2-x)mol |
| B.处理废水中Cr2O72-的物质量为mol |
| C.反应中发生转移的电子数为3nx mol |
| D.在FeO·FeyCrxO3中3x=y |
NO2和N2O4混合气体的针管实验是高中化学的经典素材。理论估算和实测发现,混合气体体积由V压缩为V/2,温度由298K升至311K。已知这两个温度下N2O4(g)  2NO2(g)的压力平衡常数Kp分别为0.141和0.363。
2NO2(g)的压力平衡常数Kp分别为0.141和0.363。
6-1 通过计算回答,混合气体经上述压缩后,NO2的浓度比压缩前增加了多少倍。
6-2 动力学实验证明,上述混合气体几微秒内即可达成化学平衡。压缩后的混合气体在室温下放置,颜色如何变化?为什么?
固溶体BaInxCo1-xO3-δ是兼具电子导电性与离子导电性的功能材料,Co的氧化数随组成和制备条件而变化,In则保持+3价不变。为测定化合物BaIn0.55Co0.45O3-δ中Co的氧化数,确定化合物中的氧含量,进行了如下分析:称取0.2034 g样品,加入足量KI溶液和适量HCl溶液,与样品反应使其溶解。以淀粉为指示剂,用0.05000 mol/L Na2S2O3标准溶液滴定,消耗10.85 mL。
4-1 写出BaIn0.55Co0.45O3-δ与KI和HCl反应的离子方程式。
4-2 写出滴定反应的离子方程式。
4-3 计算BaIn0.55Co0.45O3-δ样品中Co的氧化数SCo和氧缺陷的量δ(保留到小数点后两位)。
(共12分)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(2)上述反应中的还原剂是 ,为了防止大气污染,反应产生的气体可用 吸收。
(3)As2S3和HNO3有如下反应:As2S3+ 10H++ 10 NO-3 = 2H3AsO4+ 3S↓+10NO2↑+ 2H2O
若生成1mol NO2,则反应中转移的电子数为 。若将该反应设计成一原电池,则NO2应该在 (填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量 (选填编号)。
a.等于0.5 mol b.小于0.5 mol c.大于0.5mol d.无法确定
如右下图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器。当其它条件相同时,在Ⅰ、Ⅱ分别加入2 mol X和2 mol Y,开始时容器的体积均为V L,发生如下反应并达到平衡状态(提示:物质X、Y的状态均未知,物质Z的状态为气态):2X(?)+ Y(?) a Z(g)此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是( )
a Z(g)此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是( )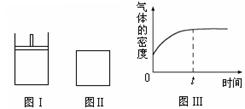
| A.物质Z的化学计量数a = 2 |
| B.若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ |
| C.若X、Y均为气态,则在平衡时X的转化率:Ⅱ>Ⅰ |
| D.若Ⅱ中气体的密度如图Ⅲ所示,则X、Y中只有一种为气态 |