设NA为阿伏加德罗常数的数值,下列说法错误的是
| A.一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA |
| B.256g S8分子中含S-S键为7NA个 |
| C.由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 |
| D.1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个 |
各种污染日趋严重,防止污染、改善水质的主要措施是对废气,废水进行处理.
Ⅰ.已知:汽车尾气处理的反应之一:2NO(g)+2CO(g)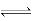 N2(g)+2CO2(g) △H<0
N2(g)+2CO2(g) △H<0
将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中发生上述反应,反应过程中部分物质的浓度变化如下左图所示.
①该反应第一次达到平衡时的平衡常数为__________。
②第12min时改变的条件是___________(填“升温”、“降温”),判断的依据是____________________。
③在第24min时,若保持温度不变,再向容器中充入CO和N2各0.060mol,平衡将_____移动(填“正向”、“逆向”或“不”).
Ⅱ.含有乙酸钠和对氯苯酚 的酸性废水,可利用微生物电池法除去,其原理如上右图所示
的酸性废水,可利用微生物电池法除去,其原理如上右图所示
①B是电池的______极(填“正”或“负”);
②酸性条件下,A极的电极反应式为______________________________。
③设电极两边溶液分别为1L,反应一段时间后,A极区溶液的pH从4变到1,此过程中处理的乙酸钠的质量为_________g 。
下列实验操作、现象和结论均正确的是
| 选项 |
操 作 |
可能的现象 |
结 论 |
| A |
向某溶液中先滴加少量氯水,再滴加KSCN溶液 |
溶液变为红色 |
溶液中一定含有Fe2+ |
| B |
向酚酞溶液中加入过量的Na2O2 |
溶液先变红后褪色 |
Na2O2与水生成的碱有漂白性 |
| C |
将表面氧化的铜丝从酒精灯的外焰慢慢移向内焰 |
黑色的铜丝变红 |
CuO被内焰中的乙醇蒸气还原 |
| D |
向饱和Na2CO3溶液中通入CO2 |
有晶体析出 |
溶解度:NaHCO3﹥Na2CO3 |
X、Y、Z、R、W是原子序数依次增大的五种短周期元素。Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同。25℃时,0.1mol/LX和W形成化合物的水溶液pH=1。下列说法正确的是
| A.Z与Y、Z与W形成的化合物的化学键完全相同 |
| B.Y、Z、W三种元素组成的化合物的水溶液可能显碱性 |
| C.简单离子的半径:Z﹥R﹥W﹥Y |
| D.因非金属Y﹥R,所以X与Y组成化合物的沸点低于X与R组成的化合物 |
物质A经下图所示的过程转化为含氧酸D,D为强酸,请回答下列问题:
(1)若A在常温下为气体单质则回答:
①A、C的化学式分别是:A________;C________。
②将C通入水溶液中,反应化学方程式为________________________。
(2)若仅A、B在常温下为气体且为化合物,则回答:
①A的化学式是:A________。
②B生成C的化学方程式为________________________。
③一定条件下碳单质与D反应的方程式为___________,该反应中D起到的作用是_________。
(3)若A在常温下为固体单质则回答:
①D的化学式是________;
②向含2mol D的浓溶液中加入足量的Cu加热,标准状况下产生的气体体积_______22.4L(填“大于”“等于”或“小于”),原因为_________________________________。
下图是实验室制取并收集Cl2的装置。A是Cl2发生装置,E是硬质玻璃管中装有细铁丝网;F为干燥的广口瓶,烧杯G为尾气吸收装置。
试回答:
(1)A中发生的化学反应方程式为 。
(2)C、D、G中各装的药品:C__________;D__________;G__________。
(3)E中的现象为 ;反应方程式为 。
(4)写出G中反应的离子方程式 。
(5)若将Cl2和SO2等物质的量混合漂白作用减弱,用化学方程式解释原因 。
将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是 g)
求:
(1)加入NaOH溶液0--20mL过程中反应方程式为:______。
160--180mL过程中反应方程式为_______________________。
(2)合金中Mg的质量为____________g。所用HCl 的物质的量浓度为____________mol/L。
将2.56 g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况),则反应中消耗HNO3的物质的量为
| A.0.05 mol | B.1 mol | C.1.05 mol | D.0.13 mol |
(B)【化学—有机化学基础】
请根据上述合成路线,回答下列问题:
(1)氢化阿托醛所含官能团的名称为 ;一定条件下,1 mol氢化阿托醛最多可跟 mol氢气加成。
(2)②的反应类型是 。
(3)写出反应③的化学方程式: 。
(4)④中所用试剂X为 。
(5)C与羧酸M在一定条件下可生成一种相对分子质量为178的酯类物质,则M的结构简式为 。
(6)氢化阿托醛具有多种同分异构体,写出符合下列特征的同分异构体的结构简式: (写出一种即可)。
①苯环上有两个取代基
②苯环上的一溴代物只有两种
③其水溶液遇FeCl3溶液呈特征颜色
④能发生加聚反应
目前机动车使用的电池品种不少,其中铅蓄电池的使用量最大。
I.铅蓄电池的电极材料分别是Pb和PbO2,电解质溶液为稀硫酸。铅蓄电池充放电的总反应方程式为:
PbO2+Pb+2H2SO4 2PbSO4+2H2O,
2PbSO4+2H2O,
请根据上述情况判断:
(1)电池的负极材料是 。
(2)充电时,铅蓄电池阳极的电极反应式为 。
Ⅱ.铅蓄电池使用量的急速增加引起铅污染日益严重,工业上从废铅蓄电池的铅膏回收铅的一种工艺流程如下:
请回答下列问题:
(3)为提高步骤①的化学反应速率,你认为可采取的措施是 (写一条即可)。
(4)写出步骤①中PbSO4转化为PbCO3反应的平衡常数表达式:K = 。
(5)步骤①中发生氧化还原反应的化学方程式为 。
(6)步骤③从母液可获得的副产品为 (写化学式)。
(7)已知:PbCO3在一定条件下可制得PbO,PbO通过进一步反应可制得Pb,写出一个由PbO生成Pb的化学方程式: 。
环境中氮氧化物的合理控制和治理是减少雾霾天气、优化生存环境的有效途径之一。请运用化学反应原理知识,回答下列问题:
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)="==" 4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) ="==" 2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 =" -1251" kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:
(2)用活性炭还原法也可处理氮氧化物。有关反应为:C(s)+2NO(g)  N2 (g)+CO2 (g)
N2 (g)+CO2 (g)
某研究小组向一个容积(3L)恒定的真空密闭容器中加人0.3mol NO和足量的活性炭与催化剂(固体试样的体积忽略不计),在恒温(T1℃)条件下发生反应,经10min反应达到平衡,测得N2的物质的量为0.09mol。
①0min~10min内以v(NO)表示的平均化学反应速率为 。
②下列各项能判断该反应达到平衡状态的是 。
| A.容器内压强保持不变 |
| B.速率关系:2v(NO)(正) =" v" (N2)(逆) |
| C.容器内CO2的体积分数不变 |
| D.混合气体的密度保持不变 |
③在相同条件下,若在容器中放入生石灰,则NO的平衡转化率 (填“增大”、“不变”或“减小”)。
短周期元素W、X、Y、Z在元素周期表中的位置如图所示。
其中Z的单质是一种重要半导体材料,广泛应用于电子工业的各个领域。
(1)W在元素周期表中的位置是 。
(2)Z的原子结构示意图为 。
(3)下列选项中,能证明元素非金属性X强于W的是 。
| A.原子序数:X>W |
| B.最低化合价:X>W |
| C.最简单氢化物的稳定性:X>W |
| D.最高价氧化物的水化物酸性:X>W |
(4)元素周期表中与Z同周期的某金属元素形成的单质A,可发生如下图所示的转化: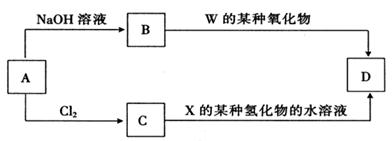
其中化合物D是一种白色沉淀,则B中溶质的化学式为 ;
C转化生成D的离子方程式为 。
(5)表中Y的最高价氧化物对应水化物的化学式为Y(OH)n ,在T℃时,其饱和溶液能使酚酞试液变红,原因是其溶液中的c(OH—) = mol·L—1 (填计算数值,已知:T℃,Ksp[Y(OH) n]=4.0×l0-12)。
常温下,电解质溶液的性质与变化是多样的,下列说法正确的是
| A.pH相同的①CH3COONa ②NaClO ③NaOH三种溶液c(Na+)大小:①>②>③ |
B.往稀氨水中加水, 的值变小 的值变小 |
| C.pH=4的H2S溶液与pH=10的NaOH溶液等体积混合,存在下列等式:c(Na+)+c(H+) = C(OH—)+2c(S2—) |
| D.Ca(ClO) 2溶液中通入少量CO2,ClO—水解程度增大,溶液碱性增强 |
某待测液中可能含有Ba2+、Fe3+、K+、Fe2+、CO32-、Cl-等离子,进行如下实验:
①取适量待测液于试管中,加入稀H2SO4,有白色沉淀生成;
②过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现;
③在步骤②中的溶液中,继续滴加氯水,溶液立即变红。
根据实验现象回答:
(1)待测液中一定含有的离子是 ,一定不含有的离子是 ;
(2)还有一种离子不能确定是否存在,要确认这种离子的实验方法和现象是 。
电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。用FeCl3溶液做腐蚀液与Cu反应生成CuCl2和FeCl2。
(1)写出该反应的化学方程式 。
(2)印刷电路的废腐蚀液含有大量CuCl2、FeCl2、FeCl3,任意排放会造成环境污染及资源的浪费。通过下列流程可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。
Ⅰ、步骤②需加入的试剂A是 (填化学式);
Ⅱ、步骤③通入的气体B是 (填化学式),写出该反应的离子方程式: