分类法在化学学科发展中起到了非常重要的作用,下列分类依据合理的是
①根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物和两性氧化物等
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否有丁达尔现象分为溶液、胶体和浊液
④根据组成元素的种类将纯净物分为单质和化合物
⑤根据电解质的水溶液导电能力的强弱将电解质分为强电解质和弱电解质
| A.②④⑤ | B.②③④ | C.①③⑤ | D.①②④ |
下列说法中正确的是
| A.干冰、液态氯化氢都是电解质 |
| B.有单质参加或生成的反应不一定属于氧化还原反应 |
| C.Na2O、Fe2O3、Al2O3既属于碱性氧化物,又属于离子化合物 |
| D.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
关于有机物的说法不正确的是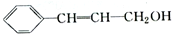
| A.lmol该有机物可以和4molH2反应 |
| B.该有机物分子中所有碳原子不可能共面 |
| C.该有机物可使溴的四氯化碳溶液褪色 |
| D.该有机物含有两种官能团 |
金属在人类社会的发展进程中起着重要的作用。下列有关金属及其化合物的说法正确的是
| A.Fe、Mg、Al均能与空气中的氧气反应在表面生成致密的氧化膜,对内层金属有保护作用 |
| B.Fe在高温下能与水蒸气反应,Fe被氧化生成Fe2O3,H2O被还原生成H2 |
| C.鉴别Na2CO3和NaHCO3溶液可向两种溶液中加入Ba(OH)2溶液,产生沉淀的就是Na2CO3 |
| D.Al与NaOH溶液的反应中,NaOH既不是氧化剂又不是还原剂 |
下列分子或离子在指定的分散系中能大量共存的一组是
| A.水溶液中:Na+、K+、NO3— |
| B.空气中:CO2、SO2、NO |
| C.氢氧化铁胶体中:H+、K+、I— |
| D.高锰酸钾溶液中:H+、SO42—、CH3CH2OH |
下列离子方程式的书写正确的是
| A.Ba(OH)2与H2SO4两稀溶液混合:Ba2++OH- +H++SO42—=BaSO4 ↓+H2O |
| B.AlCl3溶液中加入过量氨水:Al3++3NH3.HO=Al(OH)3↓ +3NH4+ |
| C.将Na投入到CuSO4溶液:2Na+Cu2+= 2Na++Cu |
| D.等物质的量的MgCl2、NaOH和HC1溶液混合:Mg2++2OH一=Mg(OH)2↓ |
用NA表示的值,下列说法正确的是
| A.24.5L氢气中所含氢原子数一定大于2NA |
| B.lmolCH3+电子数为9NA |
| C.l00g 60%CH3COOH水溶液中含有的分子数为NA |
| D.常温常压下0.lmol CO和NO的混合气体含氧原子数为0.lNA |
某学习小组为探究胶体的性质进行如下实验:
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,发生反应的化学方程式是:____________,反应后得到的溶液呈________色。
(2)取少量上述溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为______________________。
(3)在小烧杯中加入20 mL 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈__________色,即制得Fe(OH)3胶体。
(4)取上步实验烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀HI溶液,边滴加边振荡,会出现一系列变化。
①先出现红褐色沉淀,原因是________________________。
②随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式:________________________。
③最后溶液颜色加深,原因是_____________________________。(用离子方程式表示)。
④用稀盐酸代替稀HI溶液,能出现上述哪些相同的变化现象?________(写序号)。
已知常温下在溶液中可发生如下两个离子反应:Ce4++ Fe2+=Fe3++ Ce3+,Sn2++ 2Fe3+=2Fe2++ Sn4+,由此可以确定Fe2+、Ce3+、Sn2+三种离子的还原性由强到弱的顺序是
| A.Sn2+、Fe2+、Ce3+ |
| B.Sn2+、Ce3+、Fe2+ |
| C.Ce3+、Fe2+、Sn2+ |
| D.Fe2+、Sn2+、Ce3+ |
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是

| |
①中的物质 |
②中的物质 |
预测①的现象 |
| A |
淀粉KI溶液 |
浓硝酸 |
无明显变化 |
| B |
酚酞溶液 |
浓盐酸 |
无明显变化 |
| C |
AlCl3溶液 |
浓氨水 |
有白色沉淀 |
| D |
湿润红纸条 |
饱和氯水 |
红纸条褪色 |
N2O俗称“笑气”,曾用作可吸入性麻醉剂。以下反应能产生N2O:3CO+2NO2 3CO2+N2O。下列关于N2O的说法正确的是
3CO2+N2O。下列关于N2O的说法正确的是
| A.上述反应中每生成1 mol N2O,消耗1.5 mol CO |
| B.等物质的量的N2O和CO2含有相等的电子数 |
| C.N2O只具有氧化性,无还原性 |
| D.N2O会迅速与人体血红蛋白结合,使人中毒 |
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象如下:
| 金属 |
Ti |
Mg |
Cu |
| 金属表面现象 |
放出气泡速度缓慢 |
放出气泡速度快 |
无变化 |
下列有关三种金属的说法正确的是
A.三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu
B.若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C.用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D.Cu和稀盐酸不发生化学反应
火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2===Cu2S+2FeS+SO2,下列说法错误的是
| A.SO2既是氧化产物又是还原产物 |
| B.CuFeS2仅作还原剂,硫元素被氧化 |
| C.每生成1 mol Cu2S,有1 mol硫被氧化 |
| D.每转移1.2 mol电子,有0.2 mol硫被氧化 |
某溶液中可能含有Na+、NH4+、Ba2+、SO42-、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是
| A.Na+ | B.SO42- | C.Ba2+ | D.NH4+ |
下列变化或过程属于化学变化的是
| A.激光法蒸发石墨得C60 |
| B.丁达尔效应 |
| C.紫色石蕊试液通过活性炭变成无色 |
| D.用铂丝蘸取NaCl溶液进行焰色反应 |