分类是化学学习和研究的常用手段。下列分类依据和结论都正确的是( )
| A.N2O、Na2O2、CaO·SiO2均含有氧元素,都是氧化物 |
| B.HClO、浓硫酸、HNO3均具有氧化性,都是氧化性酸 |
| C.HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
| D.NaBr、MgO、AlCl3均由活泼金属和活泼非金属化合而成,都是离子化合物 |
下列叙述正确的是( )
| A.浊液均可用过滤的方法进行分离 |
| B.因为NH3·H2O是弱碱,所以不能用氨水与FeCl3溶液反应制取Fe(OH)3 |
| C.向一定体积的热浓硫酸中加入过量的铁粉,生成的气体不能完全被烧碱溶液吸收 |
| D.将某铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,说明该铝热剂中一定不含Fe2O3 |
北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子化合物,具有良好的超导性。下列有关分析正确的是( )
| A.K3C60中只有离子键 | B.K3C60中不含共价键 |
| C.该晶体在熔融状态下能导电 | D.C60与12C互为同素异形体 |
现有短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍。下列说法正确的是
| A.简单阳离子的氧化性:Y>X |
| B.气态氢化物的稳定性:Z>M |
| C.等浓度X2Z与Y2Z的溶液中,水的电离程度:X2Z>Y2Z |
| D.简单离子半径由大到小的顺序是:Z>M>Y |
强热硫酸亚铁固体可反应:FeSO4 FexOy + SO2↑+O2↑+SO3↑(未配平),则下列有关判断不正确的是( )
FexOy + SO2↑+O2↑+SO3↑(未配平),则下列有关判断不正确的是( )
| A.若所得气体中SO2与O2的体积比为2:1,则FexOy为氧化亚铁 |
| B.若所得FexOy为氧化铁,则气体中SO2与O2的体积比大于2:1 |
| C.若所得FexOy为Fe3O4,则气体中SO2与O2的体积比为3:2 |
| D.生成的混合气通入BaCl2溶液中,产生的沉淀为BaSO4 |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A.电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g |
| B.1 mol Na2O2固体中含离子总数为4NA |
| C.1mol羟基与17 g NH3所含电子数之比为9:10 |
| D.1mol Na2CO3晶体中含离子数小于1 NA |
下列说法正确的是
| 选项 |
实验 |
解释或结论 |
| A |
用洁净的Pt丝蘸取某溶液进行焰色反应,火焰呈黄色 |
该溶液中一定不含有K+ |
| B |
用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧 |
CO2、H2O与Na2O2反应是放热反应 |
| C |
利用一束强光照射明矾溶液,产生光亮的“通路” |
明矾一定发生了水解 |
| D |
向某溶液中滴加硝酸酸化的Ba(NO3)2溶液产生白色沉淀 |
该溶液中含有SO42- |
5—羟色胺对人体睡眠具有调节作用,其结构简式如图所示。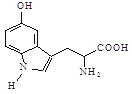
下列有关5—羟色胺说法错误的是
| A.该有机物分子式为C11H12N2O3 |
| B.该有机物分子中所有原子不可能共平面 |
| C.分子中含有1个手性碳原子 |
| D.1mol该物质最多可与4molH2或1molBr2发生反应 |
下列说法正确的是
| A.镀层破损后白铁(镀锌铁)比马口铁(镀锡铁)中的铁更易腐蚀 |
| B.SO2(g) + 2H2S(g) = 3S(s)+2H2O(l) 在常温下能自发进行,则该反应的△H>0 |
| C.0.1 mol·L-1CH3COOH溶液中加入少量水,CH3COOH电离程度和溶液pH均增大 |
D.在N2+3H2 2NH3平衡体系中加入少量催化剂,反应速率和平衡常数均增大 2NH3平衡体系中加入少量催化剂,反应速率和平衡常数均增大 |
室温下,将1mol的CuSO4•5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2,CuSO4•5H2O受热分解的化学方程式为:CuSO4•5H2O(s) CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是
CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是
| A.△H2>△H3 | B.△H1<△H3 | C.△H1+△H3=△H2 | D.△H1+△H2>△H3 |
X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是
| A.X与Y形成的化合物只有一种 |
| B.原子半径:r(Z)<r(R) |
| C.R的氢化物的热稳定性比W的强 |
| D.Y的最高价氧化物的水化物的酸性比W的强 |
物质a、b、c、d均为中学化学中的常见单质或化合物,它们之间的转化关系如右图所示(部分产物已略去),下列各组物质中,通过一步反应就能实现图示转化的是

| 选项 |
a |
b |
c |
d |
| A |
SO2 |
SO3 |
S |
H2SO4 |
| B |
Na2O |
Na2O2 |
Na |
NaOH |
| C |
CO |
CO2 |
C |
H2CO3 |
| D |
Al2O3 |
NaAlO2 |
Al |
Al(OH)3 |
下列表示对应化学反应的离子方程式正确的是
| A.Fe2O3溶于HI溶液中:Fe2O3 + 6H+=2Fe3++ 3H2O |
B.碳酸钠的水解:CO32-+ 2H2O H2CO3 + 2OH- H2CO3 + 2OH- |
C.硫酸铝溶液中滴加过量浓氨水:Al3++4NH3·H2O===AlO +4NH4++2H2O +4NH4++2H2O |
| D.用过氧化氢从酸化海带灰浸出液中提取碘:2I-+H2O2+2H+ =I2 +2H2O |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.0.1molN2与足量的H2反应,转移的电子数是0.6NA |
| B.常温下, 0.1 mol·L-1 NH4NO3溶液中含有的氮原子数是0.2NA |
| C.常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA |
| D.2.24 L CO和CO2的混合气体中所含的碳原子数为0.1 N A |