已知草酸(H2C2O4)在浓硫酸的催化作用下,加热能分解产生三种氧化物B、C、D,它们其它物质间的转化关系如下图所示,其中E是由两种元素组成的化合物,其相对分子质量为160,X、Y、Z均为单质。试解答下列问题:

(1)写出有关物质的化学式: B ;C ;E 。
(2)写出有关反应的化学方程式:反应① ;反应③ 。
(3)说出单质Y的用途 (一条即可)。
如图是铁丝在氧气中燃烧的实验,回答下列问题:

(1)铁丝在氧气中燃烧的现象是______________
(2)若将氧气换成空气,则该反应__________进行(填“能”或“不能”).
(3)该实验可以得出的结论是:①可燃物在氧气中燃烧通常比在空气中__________;②在空气中____ (填“易”或“不易 ”)燃烧的物质,在氧气中却_________燃烧。
(4)实验时,在集气瓶底部放少量水的目的是_____________
某同学用右图所示的装置测定空气中的含量,实验后发现所测定氧气的体积分数低于1/5,针对这一事实,你认为下列做法或想法不正确的是
| A.查看实验装置是否漏气 |
| B.将红磷改为蜡烛再重做实验 |
| C.实验中红磷的量可能不足,没有将瓶内的氧气消耗完全 |
| D.反应后未冷却至室温就打开止水夹,使进入瓶内的水的体积减少 |
根据铁丝在氧气中燃烧的实验,回答下列问题:
(1)该反应的文字表达式为 。
(2)集气瓶底事先要装少量水,目的是 ,在书上的演示实验中还有 (写一个)实验,集气瓶中也放少量水,其目的是 。
(3)铁丝燃烧实验若没有成功,你认为可能的操作原因会是 。(写一点)
为研究铁丝的粗细对铁在氧气中燃烧的影响,下列实验能达到目的的是:
| A.在两瓶相同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验 |
| B.在两瓶不同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验 |
| C.在同一瓶氧气中,先后进行不同粗、细铁丝的燃烧实验 |
| D.在两瓶不同浓度的氧气中,分别同时进行相同铁丝的燃烧实验 |
可以一次鉴别出空气、氧气、二氧化碳三瓶气体的最好方法是:
| A.将燃着的木条分别伸入瓶中 | B.将带火星的木条分别伸入瓶中 |
| C.分别加入适量澄清石灰水 | D.分别加入蒸馏水 |
空气中氧气含量测定的再认识。
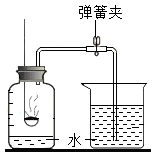
【实验回顾】如图是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。写出红磷燃烧的化学方程式_______________________。
步骤如下:
①用弹簧夹夹紧橡皮管。
②点燃燃烧匙内的红磷,立即伸入瓶中并塞紧塞子。
③_____________________________________。
④观察并记录水面的变化情况。
【实验反思】多次实验,发现集气瓶内上升的水的体积始终小于瓶内原空气体积的1/5。
【实验改进1】
I.根据铁在空气中生锈的原理(铁与氧气和水发生反应生成铁锈)设计右图实验装置,再次测定空气中氧气含量。装置中的食盐水和活性炭会加速铁生锈。
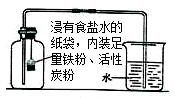
II.测得实验数据如表
| 测量项目 |
实验前 |
实验后 |
|
| 烧杯中水的体积 |
烧杯中剩余水的体积 |
集气瓶(扣除内容物)和导管的容积 |
|
| 体积/mL |
80.0 |
54.5 |
126.0 |
【交流表达】(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁,写出该反应的化学方程式____________________________________。
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是________。(消耗的水的体积忽略不计,计算结果保留一位小数)。
【猜想与假设】根据铁生锈的原理,某同学对最终生成的铁锈的主要成分作出猜想:
(Ⅰ)氧化铁(Ⅱ)碳酸铁,你认为猜想 (填序号)一定是错误的,理由是 。
【实验改进2】
使用右图装置进行实验。实验前应先进行的操作是______________________。

【实验过程】步骤1:在注射器中放入装有足量铁粉、活性炭粉的浸有食盐水的纸袋,封闭。
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹。
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化。
【数据处理】实验中需要记录的数据是___________________________________________。
计算得出氧气约占空气总体积的1/5。
【计算】铁的氧化物有多种,116g四氧化三铁与多少g氧化亚铁(FeO)中所含的氧元素质量相等。(写出计算过程)
【实验评价】与燃烧红磷法相比,用改进实验测定空气中氧气含量的优点是____________
____________________________________________。
现有A、B、C、D 4种物质,其中A和B是由同种元素组成的化合物,C、D是气态单质。它们之间的关系如图1所示:

(1)写出下列物质的化学式A______ __。
(2)B在通电条件下生成C和D的体积比为 ,该反应的类型为 。
(3)已知X3+与氖原子核外具有相同的电子层结构,则X与C在加热条件下反应的
化学方程式为:_ __。
有三个集气瓶,分别充满空气、氮气、氧气,用下列方法能最简单加以鉴别的是
| A.测密度 | B.带火星的木条 | C.燃着的木条 | D.澄清石灰水 |
分离混合物常用的方法有:①沉降;②过滤;③吸附;④蒸发;⑤蒸馏。
请选择合理的方法分离下列混合物 (填序号,可重复)。
(1)将茶水中的茶叶分离出来_________;(2)从海水中获取食盐_________;
(3)有颜色的水_________;(4)食盐和砂子_________。
已知A、B、C、D、E是初中化学中常见的五种物质。其中物质A是黑色固体单质,B、C、E是无色气体,A和E在不同条件下反应生成B、C两种产物,B、C是由相同元素组成的两种化合物,气体B易引起煤气中毒,D是无色液体,D在通电条件可生成E气体,C和D在常温下能发生化合反应。它们在一定条件下的转化关系如图所示(“—”表示相连物质间能反应,“→”表示物质间可转化)。试推断并回答相关问题:

(1) A化学式是 ;B化学式是 。
(2) 写出C、D发生化合反应的符号表达式: ;
C、D反应的生活实际应用为 。
(3) E→B的符号表达式:___________ ___;气体B的一种化学性质是 。
(4)实验室用加热紫黑色固体制取E气体的符号表达式是 。
A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,它们的转化关系如下图所示(部分生成物已省略):

(1)物质E的化学式为 。
(2)写出反应①的化学方程式 。
(3)写出反应②的化学方程式 ,该反应属于 (填
基本反应类型)反应。
区别空气、CO2、O2三种气体最简便的方法是
| A.将气体分别通入澄清的石灰水中 |
| B.观察气体的颜色 |
| C.将燃烧的木条分别伸入集气瓶中 |
| D.将气体分别通入水中 |
请根据下图实验内容回答下列问题。

A B C D
(1)A实验结束待集气瓶冷却后,进入集气瓶中水的体积小于集气瓶容积的五分之一,可能的原因是__________________(填一条即可)。该实验不能用蜡烛代替红磷,理由是___________________。
(2)B实验产生氧气与氢气的体积比约为___________。
(3)C实验观察到的现象是_______________________。
(4)D实验资料信息:白磷和红磷的着火点分别是40℃、240℃。铜片上的红磷不燃烧,是因为_______________。水中的白磷不燃烧,是因为_______________。如果要让水中的白磷在水下燃烧,应采取的措施是____________________。通过以上实验事实证明,燃烧一般需要同时具备下列条件:①物质具有可燃性;②可燃物与氧气接触;③_________________________。