如图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是( )

A.15℃时,甲和乙的饱和溶液中溶质质量相等
B.35℃时,30g甲加入50g水中,得到80g甲溶液
C.从乙溶液中获得乙晶体,常用蒸发结晶的方法
D.降低温度,甲溶液中溶质的质量分数一定减小
溶液与人类生产、生活密切相关。
(1)A、B、C三种固体物质的溶解度曲线如图所示。
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 。
②A、B、C三种物质中,溶解度随温度升高而减小的是 。
③t2℃时,完全溶解agA物质最少需要水的质量是 g。
④t2℃时,相同质量的A、B饱和溶液中,A的饱和溶液中所含水的质量 B的饱和溶液中所含水的质量(填“大于”、“等于”或“小于”)。
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、玻璃棒、 和滤纸。
(3)在实验室中,配制溶质质量分数为10%的氯化钠溶液45g,需要氯化钠固体的质量是 g.将45g10%的氯化钠溶液配成含氯化钠为0.9%的溶液,得到氯化钠溶液的质量是 g。

溶液与人们的生产生活密切相关。
(1)将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是 (填字母)
A.高锰酸钾 B.汽油 C.面粉 D.白糖
(2) 在盛有水的烧杯中加入以下某种物质, 形成溶液过程中,温度没有明显变化的是 (填字母)。
A.烧碱 B.硝酸铵 C.氯化钠 D.浓硫酸
(3)如图1为甲、乙两种固体物质的溶解度曲线。

①溶解度随温度升高而增大的物质是 (填“甲”或“乙”)。
②某同学按图2所示进行实验,得到相应温度下的A、B、C溶液,在A、B、C三种溶液中属于饱和溶液的是 (填字母)。 向溶液C中再加入25g甲,充分搅拌,恢复到t2℃时,所得溶液中溶质的质量分数为 (结果精确到0.1%)。
③ 将t2℃时的 甲、 乙两种物质的饱和溶液降温至t1℃, 所得溶液中溶质的质量分数甲 乙 (填“<”、“=”或“>“)。
利用溶解度曲线,可以获得许多有关物质溶解度的信息。如图是a、b 两物质的溶解度曲线。有关叙述正确的是( )

A.a的溶解度大于b的溶解度
B.当a物质中混有少量b物质时,可以用蒸发结晶的方法除去b
C.10℃时,取相同质量的a、b两物质分别配成饱和溶液所需水的质量是a大于b
D.将t℃时a、b的饱和溶液升温至40℃,其溶液中溶质的质量分数为 a大于b
如图是A、B、C三种固体物质的溶解度曲线,下列说法正确的是( )

A.t1℃时,三种物质的溶解度为B>A>C
B.t2℃时,三种物质的饱和溶液溶质质量分数为A=B>C
C.t3℃时,三种物质的饱和溶液降温至t1℃,仍为饱和溶液
D.t3℃时,三种物质各b g分别放入100g水中,所得溶液质量相等
如图是甲、乙两种固体物质的溶解度曲线。请回答:
(1)图中P点表示甲的溶液是 (填“饱和”或“不饱和”)的。
(2)要将t3℃时乙的饱和溶液变为不饱和溶液,可采用的方法是 (填一种即可)。
(3)将t2℃甲的饱和溶液降温至t1℃时,所得溶液的溶质质量分数 (填“变大”,“变小”或“不变”)。

如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是( )
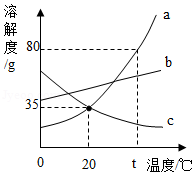
A.t℃时,将50g a物质加入到50g水中充分搅拌,可得到100g a的溶液
B.c物质微溶于水
C.a中含有少量b,可用恒温蒸发溶剂的方法提纯a
D.将20℃的三种物质的饱和溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a>c
下列关于溶液的说法错误的是( )
A.与乳化作用相比,溶解能使物质混合得更均匀
B.20℃时,50g水中溶解了15g的硝酸钾,则20℃时硝酸钾的溶解度是30g
C.一定温度下,固体物质的溶解度不随水的质量改变而改变
D.硝酸钾的饱和溶液恒温蒸发部分水后,剩余溶液溶质质量分数不变
如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线。下列叙述正确的是( )

A.t1℃时,a、c两种物质饱和溶液的溶质质量分数为20%
B.将接近饱和的c物质的溶液变成饱和溶液,可采用加溶质、降温等方法
C.将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为b>a=c
D.将150g a物质的饱和溶液从t3℃降温至t1℃,可析出30g a物质
如图1是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。回答下列问题:

(1)t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是 。
(2)P点表示,t2℃时,甲、丙两种物质的饱和溶液中,溶质与溶剂的质量比相等,均为 。
(3)t2℃时,取甲、乙两种固体各15g分别加入40g水中充分溶解,实验现象如图2所示,则烧杯a中溶解的物质是 (填“甲”或“乙”),所得溶液的质量为 g。
(4)当甲中含有少量的乙和丙(甲、乙、丙相互间均不发生化学反应)时,可采用 (填“降温”或“蒸发”)结晶的方法提纯甲物质。
(5)下列说法正确的是 (填字母序号)。
A.将甲物质的溶液由t3℃降温到t2℃,一定有晶体析出
B.将甲物质的饱和溶液由t2℃升温至t3℃时,其溶质质量分数增大
C.将t3℃时三种物质的饱和溶液恒温蒸发等质量的水,析出溶质的质量:甲>乙>丙
D.将t3℃三种物质的饱和溶液降温至t2℃,所得溶液的溶质质量分数:乙>甲=丙
1926年我国化学家侯德榜创立了“侯氏制碱法”,使原料NaCl的利用率从70%提高到96%,也使原来的副产物CaCl2转化成化肥NH4Cl.Na2CO3和NaCl的溶解度曲线如图所示,请回答下列问题:
①以NaCl为原料制取纯碱(Na2CO3),从元素守恒的观点来看,还需要补充 两种元素。(填写元素符号)
②t1℃时,Na2CO3的溶解度是 g。
③将t2℃时的Na2CO3的饱和溶液及NaCl的饱和溶液均降温至t1℃,此时Na2CO3溶液的溶质质量分数 (填”大于”“等于”小于”或“无法判断”)NaCl溶液的溶质质量分数。

化学是造福人类的科学,请利用所学知识回答下列问题。
(1)新型材料有着广泛的应用。
应用 |
“蛟龙”号深潜器 |
“神舟”五号宇航员航天服 |
新型水处理剂 |
用到的材料 |
特种钢 |
高强度涤纶 |
纳米铁粉 |
①上述材料中属于有机合成材料的是 。
②纳米铁粉能吸附废水中的某些污染物,被吸附后的废水经沉降、过滤可去除污染物。
下列物质也能因吸附而具有净水作用的是 (填字母)
a.生石灰 b.活性炭 c.纯碱
(2)溶液与人们的生产生活密切相关,图I为甲、乙、丙三种固体物质的溶解度曲线。
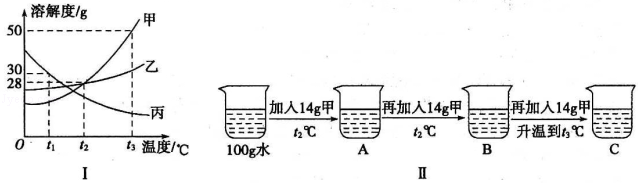
①t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是 。
②某同学按图Ⅱ所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是 (填字母)。
③t3℃时向盛有40g甲物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为 。(结果精确到0.1%)
硝酸钾、氯化钾的溶解度曲线如图1所示。
(1)P点的含义是 。
(2)当温度 时,氯化钾的溶解度大于硝酸钾的溶解度。
(3)t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液的是 ,其溶液的溶质质量分数为 (结果精确到0.1%)。
(4)图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为 。
(5)下列有关说法不正确的是 。
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
如图是X、Y两种固体物质的溶解度曲线。下列叙述正确的是( )

A.温度低于t2℃时,物质Y的溶解度小于X
B.X、Y的溶解度都随温度升高而增大
C.a点表示t1℃时X、Y的溶液都不饱和
D.Y的饱和溶液降低温度后,溶质质量分数不变