2 g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075 mol/L KMnO4溶液处理,反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的 KMnO4恰好与350 mL 0.1 mol/L (NH4)2Fe(SO4)2溶液完全反应,反应的离子方程式:MnO4-+5Fe2++8H+=Mn2++5 Fe3+ +4H2O
(1) KMnO4溶液与混合物反应,消耗KMnO4的物质的量为 mol。
(2)欲配制500mL 0.1mol/L NH4+溶液,需称取 (NH4)2Fe(SO4)2·6H2O (M=392g/mol)的质量为 g。
(3)混合物中 Cu2S的质量分数为 。
相关知识点

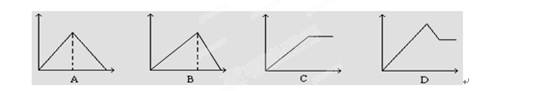
 H=-571.6kJ·mol-1
H=-571.6kJ·mol-1
 2SO3(g)。向2L的容器中充入2molSO2、1molO2,SO2的平衡转化率与温度的关系
2SO3(g)。向2L的容器中充入2molSO2、1molO2,SO2的平衡转化率与温度的关系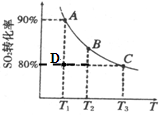
 25°C时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+) (填增大、减小或不变);
25°C时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+) (填增大、减小或不变); 粤公网安备 44130202000953号
粤公网安备 44130202000953号