元素位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素基态原子的3p 轨道上有4个电子。元素的原子最外层电子数是其内层的3倍。
(1)与所形成化合物晶体的晶胞如右图所示。
①在1个晶胞中,离子的数目为。
②该化合物的化学式为。
(2)在的氢化物()分子中,原子轨道的杂化类型是。
(3)的氢化物()在乙醇中的溶解度大于,其原因是。
(4)与可形成
①的空间构型为(用文字描述)。
②写出一种与互为等电子体的分子的化学式:。
(5)的氯化物与氨水反应可形成配合物,1该配合物中含有σ键的数目为。

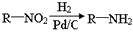
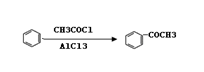
 为原料合成
为原料合成  单体的第一步的合成路线和最后一步的化学方程式(无机试剂任选)。
单体的第一步的合成路线和最后一步的化学方程式(无机试剂任选)。
 分别代表一种有机物,合成过程中其他产物和反应条件已略去。
分别代表一种有机物,合成过程中其他产物和反应条件已略去。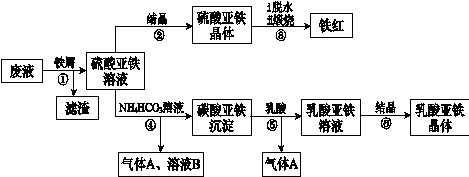
 W (s) + 3H2O (g) 请回答下列问题:
W (s) + 3H2O (g) 请回答下列问题: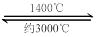 WI4 (g)。下列说法正确的有__________。
WI4 (g)。下列说法正确的有__________。 粤公网安备 44130202000953号
粤公网安备 44130202000953号