水泥是重要的建筑材料。水泥熟料的主要成分为 、 ,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
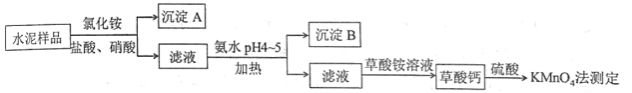
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是__________,还可使用___________代替硝酸。
(2)沉淀A的主要成分是_________________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为____________________________________。
(3)加氨水过程中加热的目的是___________。沉淀B的主要成分为_____________、____________(写化学式)。
(4)草酸钙沉淀经稀 处理后,用 标准溶液滴定,通过测定草酸的量可间接获知钙的含 量,滴定反应为: 。实验中称取 水泥样品,滴定时消耗了 的 溶液 ,则该水泥样品中钙的质量分数为______________。
重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为 ,还含有硅、铝等杂质。制备流程如图所示:

回答下列问题:
(1)步骤①的主要反应为:
上述反应配平后 与 的系数比为________。该步骤不能使用陶瓷容器,原因是________。
(2)滤渣1中含量最多的金属元素是________,滤渣2的主要成分是________及含硅杂质。
(3)步骤④调滤液2的 使之变________(填"大"或"小"),原因是________(用离子方程式表示)。
(4)有关物质的溶解度如图所示。向"滤液3"中加入适量 ,蒸发浓缩,冷却结晶,过滤得到 固体。冷却到________(填标号)得到的 固体产品最多。
a.
b.
c.
d.
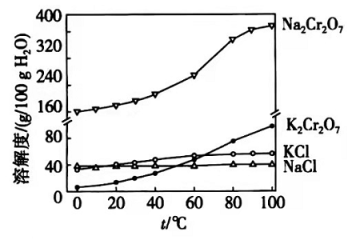
步骤⑤的反应类型是________。
(5)某工厂用 铬铁矿粉(含 40%)制备 ,最终得到产品 ,产率为________。
化学与生活密切相关。下列说法错误的是( )
| A. |
是指粒径不大于 的可吸入悬浮颗粒物 |
| B. |
绿色化学要求从源头上消除或减少生产活动对环境的污染 |
| C. |
燃煤中加入 可以减少酸雨的形成及温室气体的排放 |
| D. |
天然气和液化石油气是我国目前推广使用的清洁燃料 |
高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
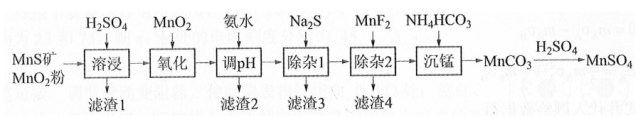
相关金属离子[ ]形成氢氧化物沉淀的pH范围如下:
|
金属离子 |
|
|
|
|
|
|
|
|
开始沉淀的pH |
8.1 |
6.3 |
1.5 |
3.4 |
8.9 |
6.2 |
6.9 |
|
沉淀完全的pH |
10.1 |
8.3 |
2.8 |
4.7 |
10.9 |
8.2 |
8.9 |
(1)"滤渣1"含有S和________;写出"溶浸"中二氧化锰与硫化锰反应的化学方程式________。
(2)"氧化"中添加适量的 的作用是将________。
(3)"调pH"除铁和铝,溶液的pH范围应调节为________~6之间。
(4)"除杂1"的目的是除去 和 , "滤渣3"的主要成分是________。
(5)"除杂2"的目的是生成 沉淀除去 。若溶液酸度过高, 沉淀不完全,原因是________。
(6)写出"沉锰"的离子方程式________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为 , 其中Ni、Co、Mn的化合价分别为+2、+3、+4。当 时, z=________。
下列实验不能达到目的的是( )
|
选项 |
目的 |
实验 |
|
A |
制取较高浓度的次氯酸溶液 |
将 通入碳酸钠溶液中 |
|
B |
加快氧气的生成速率 |
在过氧化氢溶液中加入少量 |
|
C |
除去乙酸乙酯中的少量乙酸 |
加入饱和碳酸钠溶液洗涤、分液 |
|
D |
制备少量二氧化硫气体 |
向饱和亚硫酸钠溶液中滴加浓硫酸 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
化学与生活密切相关。下列叙述错误的是( )
A. 高纯硅可用于制作光感电池 B. 铝合金大量用于高铁建设
C. 活性炭具有除异味和杀菌作用 D. 碘酒可用于皮肤外用消毒
下列实验现象与实验操作不相匹配的是( )
|
实验操作 |
实验现象 |
|
|
A |
向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置 |
溶液的紫色逐渐褪去,静置后溶液分层 |
|
B |
将镁条点燃后迅速伸入集满 的集气瓶 |
集气瓶中产生浓烟并有黑色颗粒产生 |
|
C |
向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 |
有刺激性气味气体产生,溶液变浑浊 |
|
D |
向盛有 溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 |
黄色逐渐消失,加KSCN后溶液颜色不变 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
硫代硫酸钠晶体(
)可用作定影剂、还原剂。回答下列问题:
(1)已知: , 。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
试剂:稀盐酸、稀 、 溶液、 溶液、 溶液
(2)利用 标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制:称取 某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在________中溶解,完全溶解后,全部转移至 的________中,加蒸馏水至________。
②滴定:取 的 标准溶液 ,硫酸酸化后加入过量KI,发生反应: 。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应: 。加入淀粉溶液作为指示剂,继续滴定,当溶液________,即为终点。平行滴定3次,样品溶液的平均用量为 ,则样品纯度为________%(保留1位小数)。
下列关于燃料的说法错误的是( )
| A. |
燃料燃烧产物 是温室气体之一 |
B. |
化石燃料完全燃烧不会造成大气污染 |
| C. |
以液化石油气代替燃油可减少大气污染 |
D. |
燃料不完全燃烧排放的 是大气污染物之一 |
化学在生活中有着广泛的应用,下列对应关系错误的是( )
|
化学性质 |
实际应用 |
|
|
A |
和小苏打反应 |
泡沫灭火器灭火 |
|
B |
铁比铜金属性强 |
腐蚀Cu刻制印刷电路板 |
|
C |
次氯酸盐具有氧化性 |
漂白粉漂白织物 |
|
D |
HF与 反应 |
氢氟酸在玻璃器皿上刻蚀标记 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
硼酸
是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含
及少量
)为原料生产硼酸及轻质氧化镁的工艺流程如下:
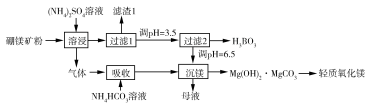
回答下列问题:
(1)在 "溶侵"硼镁矿粉,产生的气体在"吸收"中反应的化学方程式为_________。
(2)"滤渣1"的主要成分有_________。为检验"过滤1"后的滤液中是否含有 离子,可选用的化学试剂是_________。
(3)根据H3BO3的解离反应: , ,可判断 是_______酸;在"过滤2"前,将溶液pH调节至3.5,目的是_______________。
(4)在"沉镁"中生成 沉淀的离子方程式为__________,母液经加热后可返回___________工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是_________。
陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。下列说法错误的是( )
A."雨过天晴云破处"所描述的瓷器青色,来自氧化铁
B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐
D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
吸收工厂烟气中的SO2,能有效减少SO2对空气的污染。氨水、ZnO水悬浊液吸收烟气中SO2后经O2催化氧化,可得到硫酸盐。
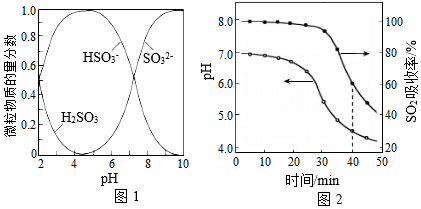
已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3﹣、SO32﹣的物质的量分数随pH的分布如图1所示。
(1)氨水吸收SO2.向氨水中通入少量SO2,主要反应的离子方程式为 ;当通入SO2至溶液pH=6时,溶液中浓度最大的阴离子是 (填化学式)。
(2)ZnO水悬浊液吸收SO2.向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(如图2)。溶液pH几乎不变阶段,主要产物是 ( 填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为 。
(3)O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO42﹣生成速率越大,其主要原因是 ;随着氧化的进行,溶液的pH将 (填“增大”、“减小”或“不变“)。
实验室制备下列气体,能实现的是( )
A.Cl2:MnO2与稀HCl溶液混合
B.C2H4:CaC2与H2O混合
C.CO2:加热饱和NaHCO3溶液
D.SO2:Cu丝与稀H2SO4混合