“侯氏制碱法”创立了更为先进的“制碱”工艺,主要反应是: 。如图是三种物质的溶解度曲线,下列叙述正确的是( )

| A. |
0℃时, 的溶解度大于 的溶解度 |
| B. |
中含有少量 ,可用降温结晶的方法提纯 |
| C. |
20℃时, 饱和溶液的溶质质量分数一定大于 不饱和溶液的溶质质量分数 |
| D. |
20℃时,将9.6g 加入到90.4g水中,可得到100g饱和溶液 |
下列实验操作能达到实验目的的是( )
|
选项 |
实验目的 |
实验操作 |
|
A |
比较铜和银金属活动性顺序 |
将金属分别放入稀盐酸中,观察现象 |
|
B |
除去 溶液中的 |
滴加适量 溶液 |
|
C |
鉴别羊毛衣物和纯棉布料 |
取样,灼烧闻气味判断 |
|
D |
测定空气中氧气含量 |
用木炭代替红磷在空气中燃烧 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
证据推理是学习化学的重要方法之一,下列推理中不正确的是( )
| A. |
氢气与空气混合点燃可能会发生爆炸, 与空气混合点燃也可能会爆炸 |
| B. |
酸雨的pH值小于7,pH值小于7的雨水一定是酸雨 |
| C. |
氧化物中一定含有氧元素,但含有氧元素的物质不一定是氧化物 |
| D. |
某物质燃烧后生成 和 ,则该物质一定含有 、 元素,可能含有 元素 |
如图是氯元素在元素周期表中的一个“方格”和其粒子结构示意图信息,下列说法中不正确的是( )

| A. |
|
| B. |
“?”处元素符号为 |
| C. |
氯原子的相对原子质量为35.45 |
| D. |
该粒子化学性质稳定 |
下列关于物质的性质和用途对应关系不正确的是( )
| A. |
化学性质稳定,能作保护气 |
| B. |
能与酸反应,用于治疗胃酸过多 |
| C. |
生石灰具有吸水性,可作食品干燥剂 |
| D. |
浓盐酸具有挥发性,可用于金属除锈 |
水是生命之源,下列关于水的说法正确的是( )
| A. |
植物油加入水中,振荡后能形成溶液 |
| B. |
工业废水未经处理直接排放 |
| C. |
硬水煮沸后可转化成软水 |
| D. |
电解水实验证明水由 、 组成 |
下列化学用语表达正确的是( )
| A. |
2个氢原子: |
| B. |
氮气中氮元素化合价: |
| C. |
氧化铝的化学式: |
| D. |
最简单有机物的分子式: |
宿迁是美酒之都,下列酿酒过程中发生化学变化的是( )
| A. |
粮食浸泡 |
B. |
酒曲发酵 |
C. |
蒸馏提纯 |
D. |
装瓶密封 |
用图﹣1所示装置制取干燥的 ,并对 的部分性质进行探究。
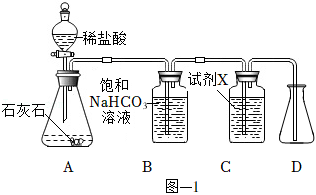
(1)装置A中发生反应的化学方程式为 。
(2)①装置B中饱和 溶液的作用是 。
②装置C中试剂 应该选用 (填字母)。
a.稀
b.浓
c. 溶液
(3)收集 并验满。将集满 的锥形瓶与盛有足量 溶液的注射器和传感器密封连接,缓慢的将 溶液注入到锥形瓶中,采集信息形成图像。见图﹣2。
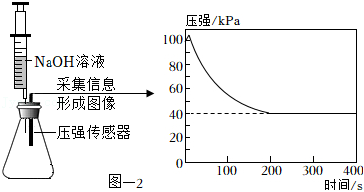
①检验装置D中 已经集满的方法是 。
②随着反应的进行,锥形瓶中压强降低的原因是 。
③反应结束后锥形瓶中的压强保持在 说明 。
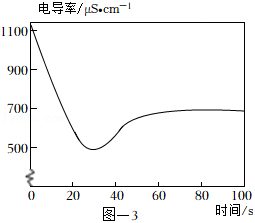
(4)取2mL饱和澄清石灰水于试管中,用4mL蒸馏水稀释,向其中缓慢通入足量 。测定反应体系的电导率变化如图﹣3所示。(忽略反应前后溶液体积的变化)
【查阅资料】
材料一:溶液的导电能力越强,溶液的电导率越大。
材料二:单位体积溶液中某离子的个数越多,则该离子的浓度越大,溶液的导电能力越强。相同浓度的不同离子导电能力不同。
材料三: 溶于水能完全解离出 和 。
遇到溶有 的水时,能反应生成易溶于水的 , 在水中能完全解离出 和 。
①石灰水中通入 气体,溶液的电导率先逐渐降低的主要原因是 。
②反应最终电导率的稳定值低于初始值的可能原因是 、 。
是化学实验中常见试剂。
(1)验证质量守恒定律。
步骤1:在锥形瓶中加入适量的 溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净,将盛有 溶液的锥形瓶和铁钉一起放在托盘天平上称量,记录所称质量为 。
步骤2:将铁钉浸入到 溶液中,塞好橡胶塞。观察实验现象,待反应有明显现象后,将盛有 溶液和铁钉的锥形瓶一起放在托盘天平上称量,记录所称质量为 。
①用砂纸将铁钉打磨干净的作用是 。
②步骤2中可观察到明显的实验现象是 。该变化可说明 和 的金属活动性由强到弱的顺序是 。
③若 ,可证明参加反应的 和 的质量总和等于 。
(2)探究 溶液对 分解具有催化作用。
①若要证明 溶液对 分解具有催化作用,除需证明 在反应前后化学性质和质量不发生改变外,还需证明的是 。
②为探究 在反应前后质量是否发生改变,某同学设计如下实验:
向 溶液中滴入10g a%的 溶液,待反应完全后,向试管中加入足量的 溶液,产生沉淀,过滤、洗涤、干燥,称量沉淀物为 。
上述实验步骤中若缺少“洗涤、干燥”,则通过沉淀物 计算出溶液中 的质量 。(填“大于”或“小于”或“等于”)
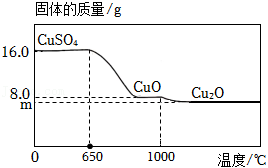
(3)将16.0g 置于坩埚中加热,固体质量与成分随温度变化的曲线如图所示。
①650℃时, 开始发生分解反应,生成 和另一种氧化物 , 的化学式为 。
②1000℃时, 开始发生分解反应,生成 和 。计算图中 的值。(写出计算过程,否则不得分)
连云港海洋资源丰富,应用前景广阔。
(1)海水晒盐。如图是利用海水提取粗盐的过程:

①“蒸发池”中质量逐渐减少的物质是 (填化学式)。
②实验室里除去粗盐中难溶性杂质一般步骤为溶解、过滤、蒸发,这三种基本操作中都要使用的玻璃仪器是 。
③析出晶体后的“母液”是氯化钠的 (选填“饱和溶液”或“不饱和溶液”)。母液中含有 ,向母液中加入澄清石灰水有白色沉淀生成,该复分解反应的化学方程式为 。
(2)海底探物。海底埋藏着大量的“可燃冰”,其主要成分是甲烷水合物(由甲烷分子和水分子组成),还含有少量的 等气体。
①下列说法正确的是 (填字母)。
a.可燃冰和干冰都属于混合物
b.可燃冰与煤相比是较清洁燃料
c.可燃冰和石油都属于可再生能源
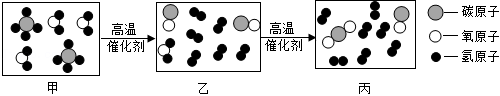
②利用 和 进行催化重整制氢气,反应前后分子变化的微观示意图如图所示。其中“乙→丙”发生反应的化学方程式为 。
2022年北京成功举办冬奥会,化学功不可没。
(1)冬奥会环保人员的服装面料是利用回收废弃的塑料瓶加工制成。
①塑料属于 (填字母)。
| A. |
a.金属材料 |
| B. |
b.复合材料 |
| C. |
c.合成材料 |
②回收废弃塑料可缓解 (填字母)。
| A. |
a.酸雨 |
| B. |
b.白色污染 |
| C. |
c.温室效应 |
(2)冬奥会火炬“飞扬”首次采用液氢作燃料。关于氢气液化的过程说法正确的是 (填字母)。
| A. |
a.氢分子的体积变小 |
| B. |
b.氢分子间的间隔变小 |
| C. |
c.氢分子的数目变少 |
(3)冬奥会上提供经过二氧化氯消毒处理的直饮水。
①二氧化氯的化学式为 。
②证明该直饮水是软水的实验方案为 。
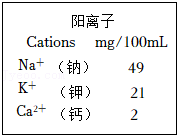
(4)冬奥会为运动员提供的某运动饮料包装标签部分说明如图。其中能预防骨质疏松、佝偻病的阳离子是 (填离子符号)。