有A、B、C三种物质,已知A为一种氯化物,B为一种钠盐,C为一种可溶性碱。下图表示的是A、B、C的溶液两两反应的实验现象。请根据有关实验现象回答:
(1)A的化学式___________;D的化学式________;蓝色沉淀的化学式是________;
(2)B与C反应的化学方程式:___________________;
(3)A溶液与洁净的铁钉反应的化学方程式:_________________。
阅读下列科普材料,回答相关问题。
【材料1】1915年4月22日下午5时,在第一次世界大战两军对峙的比利时伊珀尔战场,趁着顺风,德军一声令下开启了大约6000只压缩氯气(Cl2)钢瓶。霎时间,在长约60公里的战线上,黄绿色的云团飘向法军阵地。所经之地绿色植被枯黄褪色;英法士兵先是咳嗽继而喘息,甚至死亡,部分逃到高高的山上的士兵活了下来;战场上的武器锈迹斑斑。这就是战争史上第一次化学战。
(1)推测氯气可能具有的物理性质是______。
(2)推测氯气可能具有的化学性质是______。
(3)元素周期表中氯元素的信息如图所示,其原子的核外电子数为______。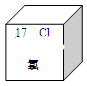
【材料2】氯气可用于制备多种消毒剂。①二氧化氯是一种高效、安全环保型杀菌消毒保鲜剂。②漂白粉是一种广泛普及的杀菌消毒漂白剂,有效成分是次氯酸钙[Ca(ClO)2],其水溶液遇空气中的二氧化碳生成碳酸钙和次氯酸[HClO],HClO起到杀菌、消毒、漂白的作用。
(1)①中二氧化氯的化学式为ClO2,其中氯元素的化合价为______。
(2)②中发生反应的化学方程式为______。
铁质水龙头长期使用容易生锈,小明从自家水龙头上取下一些铁锈样品,用图甲所示的装置进行实验。
(1)B处澄清石灰水变浑浊,反应方程式为 ,C处酒精灯的作用是
(2)实验结束,小明将所得的黑色固体物质放入足量的稀硫酸中,发现没有气泡,这说明生成物中 (有或没有)铁。
为解释这个现象,小明查阅下列资料:
Ⅰ。已知铁的氧化物有FeO、Fe3O4、Fe2O3,,在一定条件下,均能逐步失去其中的氧,最终被还原为铁。
Ⅱ。某炼铁厂对氧化铁和一氧化碳进行热反应分析,获得相关数据并绘制成下图。
通过分析资料确定:
①700℃时氧化铁和一氧化碳进行反应的产物是 (填FeO或Fe3O4或Fe).
②小明实验失败的主要原因是 。
如图是模拟海水制盐的流程:(已知:氢氧化镁不溶于水)

(1)实验①加入过量Ca(OH)2溶液的目的是 。
(2)实验结束后,兴趣小组对滤液进行探究:
【提出问题】滤液中除了氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想:
所以滤液中溶质除了氯化钠外,还含有 。
【验证猜想】
| 步骤 |
实验操作 |
实验现象 |
结论 |
| |
|
|
|
【实验结论】经过兴趣小组的实验验证,该猜想是正确的。
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤④的作用是除去杂质,请写出相关的化学反应方程式: 。如果要将精盐水继续提纯出NaCl晶体,应进行的操作是 。
(8分)有某固体混合物,已知其中可能含有Na2CO3、CaCO3、CuSO4、FeCl3四种物质中的两种或多种。按下图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应)
试根据实验过程和发生的现象填写以下空白:
(1)常温下,气体A水溶液的pH ____________7(填“大于”“小于”“等于”之一)。
(2)该固体混合物中,一定不存在的物质是(写化学式)_____________________________,理由是:_______________________________。
(3)在滤液E中,一定大量存在的阴离子是(写离子符号)_____________________。
(4)写出过程③中一定发生反应的化学方程式______________________________________。
(5)写出过程①中发生反应的一个化学方程式_______________________ 。
实验室有一瓶无色溶液,标签模糊,依稀可见
.为探究该溶液中是否有硫酸根,化学兴趣小组的同学设计以下甲、乙方案,并取样品实验、记录相关现象.

请根据上述信息,完成下列问题:
(1)方案甲得出的结论是:不能确定无色溶液中是否含有硫酸根.理由是.
(2)方案乙得出的结论是:无色溶液中含有硫酸根.则加入足量稀
的作用是;如果加入稀
有气泡产生,则可能发生反应的化学方程式是。(写1个)
(3)另取无色溶液少许,滴入紫色石蕊试液,溶液变红.若溶液中只含有一种阳离子,则方案乙中产生白色沉淀的化学方程式为。
我国拥有丰富的海洋资源,开发利用这些宝贵的资源有力地促进了我国经济的发展。从海水中提取的粗盐中除了NaCl外,还含有泥沙等杂质。根据下列实验室中除去泥沙等杂质的实验步骤,回答相关问题:
(1)在过滤操作中要用到的玻璃仪器有烧杯、玻璃棒 、 (填仪器名称)。
(2)上述经过滤后的滤液中,还含有Ca2+、Mg2+等阳离子。要想知道该滤液是硬水还是软水,可加入 进行检验。生活中可以将水 而使硬水变为软水。
(3)海水提取出粗盐后的母液中,还含有较多的氯化镁,工业上从母液中提取氯化镁的过程如下图,电解熔融氯化镁可制得金属镁和氯气。工业上也可用电解饱和NaCl水溶液的方法制得氢氧化钠、氯气(Cl2)和氢气,请写出该反应的化学方程式: 。
以电解食盐水为基础制取氯气、氢氧化钠等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不符合电解要求,因此必须经过精制。以粗盐为原料的“氯碱工业”流程如下: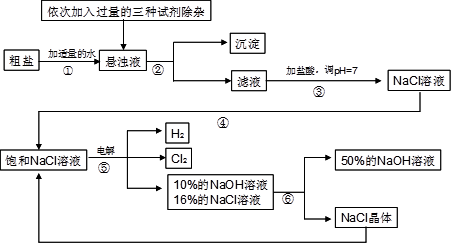
(1)氯气、氢氧化钠在工业上有广泛的用途。下列关于氢氧化钠的描述中,不正确的是 。
| A.能去除油污,可做厨房清洁剂 | B.易溶于水,溶解时放出大量的热 |
| C.水溶液能使石蕊溶液变红 | D.可用作某些气体的干燥剂 |
(2)操作②的名称是 ,该操作所需的玻璃仪器是 ;操作④的名称是 ,该操作需玻棒不断搅拌,这是为了防止 。
(3)操作①②间除杂质时所加的三种试剂是NaOH溶液、Na2CO3溶液、BaCl2溶液(均过量),其顺序要求是:Na2CO3溶液必须在BaCl2溶液之 (填“前”或“后”)加入。有同学提出用 溶液代替BaCl2溶液可达到同样的目的。
(4)电解饱和NaCl溶液的化学方程式是 。
(5)该流程中可以循环利用的物质是 。
比较、分析、归纳是学习化学的重要方法。通过比较可以发现相同的反应物在不同外界条件下,会发生不同的反应。请参照示例归纳反应规律:
| 组别 |
化学方程式 |
规律 |
| 示例 |
 |
反应物相同时,反应物的量不同,生成物不同 |
| (1) |
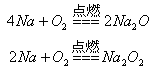 |
|
| (2) |
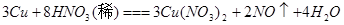 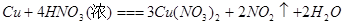 |
|
空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应。下图是以空气和其他必要的原料合成氮肥(
)的工业流程。请按要求回答下列问题:

(1)步骤①中发生的是变化(填"物理"或"化学")。
(2)写出步骤③中发生反应的化学方程式。
(3)上述化学反应中属于化合反应的有个。
(4)下图是化肥硝酸铵包装袋上的部分说明:硝酸铵应具有的性质是(填字母)。

| A. |
易溶于水 |
B. |
有挥发性 |
C. |
受热易分解 |
施用该类肥料时,要避免与碱性物质混合使用,写出硝酸铵与熟石灰反应的化学方程式。
氢氧化钴[Co(OH)2]受热易分解,能与酸性溶液反应,可作涂料和清漆的干燥剂,制备方法为:①Co+2HCl=CoCl2+H2↑,②CoCl2+2NaOH=Co(OH)2↓+2NaCl。下列判断正确的是
| A.钴的金属活动性比铜的弱 | B.①为置换反应,②为复分解反应 |
| C.氢氧化钴的化学性质稳定 | D.氢氧化钴可以干燥氯化氢气体 |
某化学兴趣小组的同学参照教科书内容,在学校实验室里完成了以下两个实验:
实验一:配制溶质质量分数为6%的NaCl溶液50 g,按如下步骤进行操作:
实验二:称取5.0 g粗盐进行提纯。粗盐除含有NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了有效将粗盐提纯,实验的各步操作流程如下图所示:
请你根据以上信息回答下述问题:
(1)配制50 g溶质质量分数为6%的NaCl溶液,需NaCl______g,水______mL。
(2)NaCl溶解过程中用到了玻璃棒,它的作用是________________。
(3)粗盐提纯时,操作Ⅰ的名称为__________________。
(4)某同学所得精盐比其他同学明显要少,原因可能是____________________。
A.溶解时将5.0 g粗盐一次全部倒入水中,立即过滤
B.蒸发时有一些液体、固体溅出
C.提纯后所得精盐尚未完全干燥
(10湛江22).(8分)某学校化学兴趣小组用NaCl固体(含有的杂质CaO)来配制一定质量分数的NaCl溶液,实验的流程图如下: 
请回答:
(1)写出适量HCl加入到溶液B中所发生反应的化学方程式为__________________________。
(2)操作2的名称是__________,在溶液A中加入过量碳酸钠的目的是________________。
(3)若要配制100g质量分数为10%的氯化钠溶液,除了用到天平、烧杯、量筒外,还需用到的玻璃仪器是__________,其作用是______________________________。
【10桂林30】 (6分) A、B、C、D、E是初中化学中的五种常见物质。C、D是单质,C为紫红色固体,D被认为是最清洁的能源。B的浓溶液常用做干燥剂。已知Fe和A、B的水溶液分别能发生反应:
①Fe + A → C + E; ②Fe + B → D + E 。
(1)写出A、B、C的化学式: A , B ,C 。
(2)现有Fe和A、C三种固体组成的混合物,小刚想测定该混合物中C物质的质量分数,他设计并完成了以下实验:
你认为,小刚的实验数据处理是否正确(填“正确”或“ 不正确”) ,理由是 。
活性氧化锌(ZnO) 是一种面向21世纪的新型高功能精细无机产品。用粗ZnO制备活性ZnO的生产工艺流程做如下图所示。
I制备活性氧化锌
一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如下: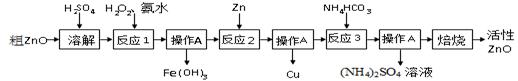
【查阅资料】
1、粗ZnO中常含杂质FeO、CuO
2、反应3是为了制得碱式碳酸锌、碱式碳酸锌经焙烧可制得活性ZnO
3、已知:几种物质沉淀时的pH如下表:
| 物质 |
Fe(OH)2 |
Fe(OH)3 |
Zn(OH)2 |
Cu(OH)2 |
| 开始沉淀时pH |
6.34 |
1.48 |
6.2 |
5.2 |
| 完全沉淀时pH |
9.7 |
3.2 |
8.0 |
6.4 |
| Fe(OH)2是一种絮状沉淀,不易除去,处理时常将其转化为Fe(OH)3而除去。 |
【问题讨论】
(1)溶解前将氧化锌粗品粉碎成细颗粒,目的是___________ __________ _ 。
(2)写出ZnO与加稀硫酸反应的化学方程式 。
(3)反应1的目的将Fe2+氧化为Fe3+,并完全沉淀Fe(OH)3 ,为了暂不形成Cu(OH)2、Zn(OH)2 ,该步骤需控制溶液pH的范围是 ,操作A的名称是 。
(4)反应2中加入锌发生的反应属于 反应(填化学反应的基本类型)。
Ⅱ测定碱式碳酸锌的化学式
碱式碳酸锌的化学式是xZnCO3•yZn(OH)2•zH2O,用下列装置测定碱式碳酸锌的化学组成。(假设每步反应、吸收均完全)
提示:碱式碳酸锌xZnCO3•yZn(OH)2•zH2O受热分解为ZnO、H2O、CO2三种产物,其中
ZnCO3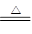 ZnO+CO2↑ Zn(OH)2
ZnO+CO2↑ Zn(OH)2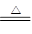 ZnO+H2O
ZnO+H2O
【实验步骤】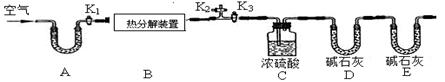
①按图连接好装置,并检查装置的 ;
②在热分解装置中装入68.2g样品,打开活塞 ,关闭 ,缓缓鼓入空气数分钟;
③称量装置C、D的质量;
④关闭活塞K1,K2,打开K3,启动热分解装置,使样品充分热解;
⑤停止加热,继续通空气至装置冷却到室温; ⑥再次分别称量装置C、D的质量.
【记录数据】该小组同学按上述实验步骤进行实验,并记录了如下数据:
| |
装置C的质量(/g) |
装置D的质量(/g) |
| 实验前 |
198.4 |
235.7 |
| 实验后 |
209.2 |
244.5 |
【实验分析及数据处理】
(1)A处干燥管盛放的药品是碱石灰(CaO与NaOH的固体混合物),其作用是 。
(2)第⑤步继续通空气的目的是 。
(3)E处碱石灰的作用是 ,若没有此装置,测得二氧化碳的质量 (填“偏大”、“偏小”或“无影响”)。
(4)根据上述数据,计算xZnCO3•yZn(OH)2•zH2O中x:y:z的最简比=
该碱式碳酸锌受热分解的化学方程式为 。