探究学习小组在实验室中用图1所示装置制取
并探究
与过氧化钠(
)的反应。

查阅资料得知:过氧化钠(
)是一种淡黄色固体,能与
,
发生反应:
,
↑
请回答下列问题:
(1)装置
中发生反应的化学方程式为,利用装置
制取
的优点是.
(2)装置
的作用是吸收
中混有的
,发生反应的化学方程式为.
(3)装置
的作用是.
(4)装置
中收集到的气体是(填化学式),该气体还可以用下列图2装置中的进行收集(填写字母序号).

(5)为探究反应后装置
硬质玻璃管中固体的成分,该小组同学进行了如图3实验:

根据判断,反应后装置 硬质玻璃管中固体为.
“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来了。”
小红看到这段话后非常感兴趣,她和同学们一起对该问题进行了探究。
[查阅资料]氢氧化钠、氢氧化钾、氢氧化钙等物质能使无色酚酞溶液变红。
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想]①可能有一种气体和另一种物质生成②反应过程中可能有能量变化
[设计装置]如右图所示

[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开右图装置中分液漏斗的活塞,控制滴加水的速度,
观察到试管内有气泡产生,用带火星的木条靠近P处,
木条复燃。说明生成的气体是______ _______;
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:_______________
实验二:探究反应后生成的另一种物质是什么?
(1)小军猜想另一种物质可能是Na2CO3,但小红通过设计实验:向溶液中滴加少量稀盐酸,无气泡产生,证实不存在 CO32-;
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,小军预测反应中应有
生成;
[表达]由实验探究的结果,写出过氧化钠和水反应的化学方程式:_ ____。
(1)家庭生活中制作食品经常用到碳酸钠(苏打)和碳酸氢钠(小苏打),碳酸氢钠不稳定,在潮湿空气中缓慢分解,受热至65
以上迅速分解,270
时完全分解为碳酸钠。某同学为探究它们的性质差异,设计了图所示装置并进行实验。请回答:

①加热一段时间后,
两烧杯分别看到的现象是;由此可得出的结论是;
②碳酸氢钠分解的化学反应方程式:;
③该装置设计的优点是;
④实验中应注意的问题是。
(2)在日常生活和工农业生产中,溶液有着广泛的应用。比如,氨碱工业用到的是饱和食盐水,医疗上使用的则是0.9%的生理盐水。请按要求设计并完成一下实验:
实验用品:氯化钠溶液、氯化钠、硝酸钾、蒸馏水、烧杯、试管、玻璃棒、药匙
探究实验一:澄清透明的氯化钠溶液是否是饱和溶液
| 实验步骤 |
实验现象 |
实验结论 |
| 取一只试管倒入约
氯化钠溶液 ,用药匙加入少量氯化钠固体,振荡,观察现象 |
氯化钠固体溶解 |
探究实验二:将不饱和氯化钠溶液变为饱和溶液并探究饱和氯化钠溶液还能否溶解硝酸钾
| 实验步骤 |
实验现象 |
实验结论 |
|
不饱和溶液 变为饱和溶液 |
||
育才中学的某研究小组在探究维生素C水溶液的酸碱性时,不慎误把维C泡腾片(保健品。主要成分如图所示)当做维生素C片放入了水中,结果发现有大量气泡产生,于是引起了该小组同学的探究兴趣。

【提出问题】该气体成分是什么?
【猜想与假设】小青说:该气体可能含有CO2 、O2、 CO、 H2 、 N2 中的一种或几种。小丽说:不可能含有 N2,因为
小亮说:不可能含有H2 和CO,因为从药品安全角度考虑,H2易燃易爆,CO
最后研究小组的同学共同认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
| 编号 |
实验操作 |
实验现象 |
| ① |
将气体通入澄清的石灰水 |
澄清石灰水变浑浊 |
| ② |
将带火星的木条伸入到该气体中 |
带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有 ,
(2)由实验② (填“能”或“不能”)确定该气体中不含氧气,理由是
某实验小组的同学想用碳酸钠溶液与饱和石灰水反应来制取少量氢氧化钠.
(1)该复分解反应能发生的理由是.
(2)有人提出:实验时没有注意药品的用量,所得到的氢氧化钠溶液可能不纯.
猜想一:只含
.
猜想二:含有 和 .
猜想三:.
(3)为了验证猜想一成立,请你根据可选用的试剂,完成实验设计方案并填写以下表格.可选试剂:
溶液、稀盐酸、
溶液
| 实验步骤 |
实验操作 |
预期现象及结论 |
| 1 |
取少量所得溶液于试管中, |
证明原溶液中不含有 |
| 2 |
另取少量所得溶液于试管中, |
结合步骤1,猜想一成立 |
空气中氧气含量测定的再认识。
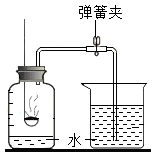
【实验回顾】如图是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。写出红磷燃烧的化学方程式_______________________。
步骤如下:
①用弹簧夹夹紧橡皮管。
②点燃燃烧匙内的红磷,立即伸入瓶中并塞紧塞子。
③_____________________________________。
④观察并记录水面的变化情况。
【实验反思】多次实验,发现集气瓶内上升的水的体积始终小于瓶内原空气体积的1/5。
【实验改进1】
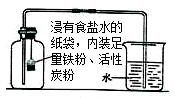
I.根据铁在空气中生锈的原理(铁与氧气和水发生反应生成铁锈)设计右图实验装置,再次测定空气中氧气含量。装置中的食盐水和活性炭会加速铁生锈。
II.测得实验数据如表
| 测量项目 |
实验前 |
实验后 |
|
| 烧杯中水的体积 |
烧杯中剩余水的体积 |
集气瓶(扣除内容物)和导管的容积 |
|
| 体积/mL |
80.0 |
54.5 |
126.0 |
【交流表达】(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁,写出该反应的化学方程式____________________________________。
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是________。(消耗的水的体积忽略不计,计算结果保留一位小数)。
【猜想与假设】根据铁生锈的原理,某同学对最终生成的铁锈的主要成分作出猜想:
(Ⅰ)氧化铁(Ⅱ)碳酸铁,你认为猜想 (填序号)一定是错误的,理由是 。
【实验改进2】
使用右图装置进行实验。实验前应先进行的操作是______________________。

【实验过程】步骤1:在注射器中放入装有足量铁粉、活性炭粉的浸有食盐水的纸袋,封闭。
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹。
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化。
【数据处理】实验中需要记录的数据是___________________________________________。
计算得出氧气约占空气总体积的1/5。
【计算】铁的氧化物有多种,116g四氧化三铁与多少g氧化亚铁(FeO)中所含的氧元素质量相等。(写出计算过程)
【实验评价】与燃烧红磷法相比,用改进实验测定空气中氧气含量的优点是____________
____________________________________________。
甲为人体吸入空气和呼出气体成分对比图。
含量变化真有这么大?
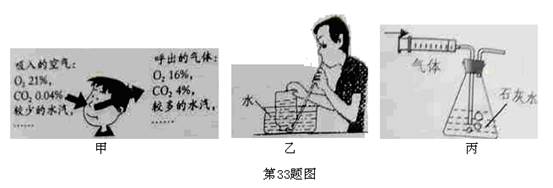
(1)利用图乙所示法收集一瓶呼出的气体,标上
;取一个同样装有空气的集气瓶,标上
。将两根同样的小木条点燃后同时伸入
瓶和
瓶,
瓶中的木条先熄灭。这个实验现象(选填"能"或"不能")说明呼出的气体中二氧化碳更多。
(2)用大针筒将
人体呼出气体压入
澄清石灰水中(如图丙),澄清石灰水变浑浊;用同样的方法将
空气压入另一瓶
澄清石灰水中,请说出澄清石灰水是否变浑浊并解释原因:。
竹炭包是一种集观赏与空气净化为一体的产品。这种产品可对车内及室内空气中的一氧化碳、甲醛等有害气体进行吸附。某课外活动小组对竹炭进行初步探究。
【提出问题】竹炭中是否含有碳元素
【猜想与假设】竹炭中含有碳元素
【查阅资料】①新鲜的血液,遇一氧化碳由鲜红变为暗红。
②氢氧化钠溶液可以吸收二氧化碳。
【设计实验】所用装置如下图所示。(A装置的作用为吸收空气中的水和二氧化碳)

(1)实验开始后,C装置中产生白色沉淀,发生反应的化学方程式为 ,,E装置中新鲜的鸡血变为暗红色。
(2)小玥认为应在A、B装置间,再增加一个C装置,目的是 。
(3)课外活动小组的同学设计的这套装置的不足之处是 ,请你设计解决的方法 。
【结论】竹炭中含有碳元素。
【拓展应用】竹炭细密多孔,竹炭牙膏中含有竹炭等成分具有消炎、止痛、化淤、去污等功效,下列有关竹炭牙膏的用途描述不正确的是 。
A.可除衣领袖口等处的汗渍 B.不能除去口中异味C.虫咬、灼伤可消炎止痛
一辆载满20t电石的挂车,在浙江滨江区燃起熊熊大火并伴有大量黑烟。事故路面上洒落了五六百米燃着的石头。这辆货车在雨中整整燃烧了一天,消防官兵对大火也束手无措,场面让人震撼。大家对电石的化学性质产生了浓厚的兴趣,请你一起与他们完成下列探究活动.
【查阅资料】电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体。常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟。
【猜想与假设】
电石与水反应生成的可燃性气体是:氧气、氢气或乙炔(C2H2);同学们做出以上猜想的依据是 ,大家讨论后,一致认为该气体不可能是氧气,原因是 。电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙中的一种。同学们经过讨论认为白色固体不可能是氧化钙,因为氧化钙会与水反应。
【实验探究】
| 实验步骤 |
实验现象 |
实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃. |
气体燃烧,产生黄色火焰并伴有浓烈黑烟. |
电石与水反应产生的气体是 |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸. |
固体溶解, |
电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后生成的固体于试管中加水,向上层清液中滴加 . |
溶液变红 |
电石与水反应产生的固体是氢氧化钙 |
【反思交流】请根据以上实验结论写出电石与水的反应的化学方程式 ;
载有电石货车可以在雨中整整燃烧一天而不熄灭,说明电石与水反应是 (填“吸热”或“放热”)反应。
利用如图所示的装置可进行一氧化碳还原氧化铁的实验,其中,氮气可用作本实验的保护气; 盛放氧化铁的是一支带有支管的试管,其支管可用于导出试管内的气体;酒精灯带网罩;整套装置的气密性良好.实验前,弹簧夹a、b均处于关闭状态,开始实验时,打开a,通入氮气一段时间后点燃酒精灯,再关闭a,打开b.请联系所学知识回答下列问题:
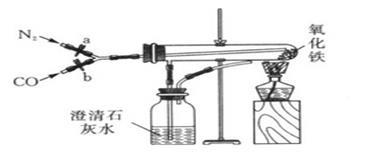
(1)该实验过程中可以观察到的现象有:_________________、_________________。
(2)试管内一氧化碳与氧化铁反应的化学方程式为____________________________。
(3)实验结束时,应先打开a,再___________,然后___________,继续通氮气直至装置冷却。(选填“A”或“B”)A.熄灭酒精灯 B.关闭b
(4)待试管冷却后,把生成的黑色粉末倒在白纸上后;用磁铁靠近黑色粉末,黑色粉末全部被吸引;再取少量黑色粉末放入足量硫酸铜溶液中,搅拌后发现黑色粉末部分变红。
【提出问题】炼出来的黑色粉末的成分是什么呢?
【查阅资料】在铁的氧化物中只有氧化铁是红棕色,其余都是黑色;只有氧化亚铁在空气中会很快被氧化成氧化铁;只有四氧化三铁有磁性。
【综合探讨】同学们得出此次炼铁得到的生成物是___________________。
(5)请从两个不同角度评价该实验的优点:_______________,_________________。
请根据如图实验装置,回答问题。

(1)写出仪器a的名称 。
(2)若实验室用氯酸钾和二氧化锰共热制取氧气,选用的发生装置和收集装置是 ,写出该反应的化学方程式 。
(3)将B制取的气体通入G装置,探究燃烧的条件。观察到Y型管左边的白磷燃烧,右边的白磷不燃烧,可探究出燃烧所需的条件是 。
(4)若用B、F装置制取二氧化碳。当观察到 时,证明二氧化碳收集已满;若F装置中没有出现上述现象。其可能原因是 。(写一个)
天然气的主要成分是甲烷,某化学兴趣小组的同学对甲烷燃烧的产物进行了探究。
【提出问题】甲烷燃烧后生成了哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】甲同学:CO2、H2O 乙同学:CO、H2O
丙同学:NH3、CO2、H2O 丁同学:CO2、CO、H2O
你认为 同学的猜想肯定是错误的,理由是 。
【实验探究】为了验证上述几位同学的猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:

(1)A、B装置的顺序能否颠倒? (填“能”或“否”)。
(2)甲烷在一定量的O2中燃烧用的是纯净O2而不用空气的原因是 。
(3)实验中观察到装置A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断 同学猜想成立。
(4)请写出B中澄清石灰水变浑浊,C中红色粉末变成黑色的化学方程式:
、 。
【反思与交流】为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是
。
在学习过程中,小青同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体也有多种可能?
【猜 想】碳与氧化铜反应生成的气体中:①只有CO2,则发生的化学方程式是 ;
②只有 ;③既有CO,又有CO2。
【查阅资料】浸有磷钼酸溶液的氯化钯试纸遇CO2无变化,但遇到微量CO会立即变成蓝色。
【方案设计】通过上述资料和已有知识,小青初步设想用浸有磷钼酸溶液的氯化钯试纸和澄
清的石灰水对碳与氧化铜反应生成的气体进行检查。
【实验验证】经过思考之后,小青设计了如下实验装置:

【实验步骤】
(1)打开弹簧夹,先通一会儿纯净、干燥的N2,通一会儿N2的目的是 ;
(2)关闭弹簧夹,点燃酒精灯加热。
【结 论】充分反应后,小青观察到:试纸 ,石灰水 ,证明猜想③是正确的,
A中可能观察到的现象 。
【定量计算】小青称取碳和氧化铜的混合物的质量为1g,充分反应后,装置C的质量增
加了0.22g。计算装置C中生成碳酸钙的质量是多少克?
【反思与评价】从环保的角度分析该实验装置中不完善之处是 。
用图甲所示的电解水装置来测定水的组成。

【实验步骤】
(1)按图安装好装置,检验装置气密性。
(2)在U型管中装入水(水面略低于支管口)。
(3)取下注射器,打开电源一段时间后,关闭电源。
(4)将注射器活塞推到顶后连接注射器,再次打开电源。
当注射器二中活塞停留在10mL刻度时,关闭电源。
(5)检验气体。
【实验结论】水是由 组成的。电解水的符号表达式 。
【问题讨论】
(1)实验开始时先打开电源通电一段时间后再接上注射器的目的是 。
(2)实验结束时注射器一中活塞停留在 刻度处。将该注射器带上针头,移向燃着的木条旁,推动活塞,现象是 。
(3)水电解的过程可用下列图示表示。粒子运动的先后顺序是 。
化学课上,同学们做了人体呼出的气体使澄清石灰水变浑浊实验后,对呼出的气体中主要成分及含量非常好奇,设计了如下实验进行探究。
【提出问题】呼出的气体中有哪些主要成分,它们的含量是多少?
【查阅资料】①呼出的气体中仍含有O2。②CO2在饱和NaHCO3溶液中的几乎不溶解。③白磷燃烧需要氧气,白磷燃烧所需的最低温度为40℃,燃烧现象和产物均与红磷相同。④氢氧化钠溶液能吸收二氧化碳,并与二氧化碳反应生成碳酸钠和水。
【猜想与实践】猜想:呼出的气体中主要成分是N2、O2、CO2、水蒸气等。
实验Ⅰ:验证呼出的气体中含有水蒸气。
(1)实验操作:取一洁净干燥的玻璃片,对着其哈气,观察到________,可以判断呼出的气体中含有水蒸气。
实验Ⅱ:验证呼出的气体中含有N2、O2、CO2,并测其含量。同学们在老师的指导下设计了如图所示装置(B是带有刻度的量气装置)。

(2)实验记录
| |
实验操作 |
主要实验现象 |
实验结论及解释 |
| ① |
检查装置的气密性,向装置中加入药品,关闭止水夹a~f。 |
(不填) |
装置的气密性良好 |
| ② |
打开b、c、d,向B中吹入一定量气体后关闭d,并冷却到室温。 |
B中液体进入到A中,B中液体减少500ml。 |
收集了500ml气体 |
| ③ |
关闭b,打开a、e、f,用打气筒向A中缓缓充气,直到B中气体刚好全部排出 |
A中的液面下降,B中的液面上升至最高,C中的左侧导管口有 ①_______,且液面下降,液体沿导管进入D中,D中液体为475ml |
呼出气体中含有CO2 |
| ④ |
关闭e、f,用凸透镜聚光引燃白磷. |
白磷燃烧,产生大量白烟,放出大量热 |
呼出气体中含有O2,该反应的文字表达式为: ②____________ |
| ⑤ |
待白磷熄灭并冷却到室温,打开f。 |
D中液体倒吸入C瓶中,C瓶中液面上升,D中剩余液体为400ml。 |
呼出气体中含有 ③____________。 |
同学们经过3次重复实验,确认了呼出的气体中的主要成分及其含量。
【实验反思】
(3)该实验设计依据的N2性质有__________(填字母序号)。
A.难溶于水
B.不能和NaOH溶液反应
C.不能燃烧,也不支持燃烧
D.无色无味的气体
(4)在实验(2)的操作⑤中,未等C中的气体的冷却,就打开f止水夹读数,则所测的O2的体积分数会_____(填“偏大”、“不变”、或“偏小”) 。