科学研究中,常通过对实验数据的分析计算,得出某未知物质的相对分子质量,从而推测该物质的分子式。某科研小组经反复实验,发现2A+3B=2C+4D中,3.2gA恰好和4.8gB完全反应,生成4.4gC.请问:
(1)同时生成D的质量为 g。
(2)若D的相对分子质量为18,求A的相对分子质量(写出计算过程)。
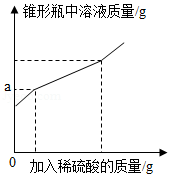
为测定久置于空气中的氢氧化钠样品的变质程度,某化学活动小组称取该固体样品6.5g放入锥形瓶中,加水溶解,配成50g溶液,再向锥形瓶中滴加稀硫酸,反应过程中产生气体质量的部分实验数据和锥形瓶中溶液质量变化的图象如表所示:
加入稀硫酸的质量/g |
40 |
65 |
75 |
产生气体的质量/g |
1.1 |
2.2 |
2.2 |
(1)6.5g样品与稀硫酸完全反应产生气体的质量是 g。
(2)6.5g样品中碳酸钠的质量分数是 。(结果精确至0.1%)
(3)以上三次的实验数据中,只有一次加入的稀硫酸与锥形瓶中溶液的溶质恰好完全反应。
①如图图象中a的数值是 。
②求该实验中所用稀硫酸的溶质质量分数。(写出计算过程)
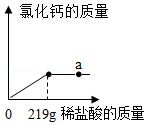
实验室模拟高温煅烧石灰石的方法制取二氧化碳,取35g石灰石样品(假设杂质受热不分解且不与酸反应),煅烧一段时间恢复到室温,测得生成11g二氧化碳。向剩余固体中逐滴加入某盐酸至不再反应为止,又生成2.2g二氧化碳,加入盐酸的质量与生成的氯化钙质量关系如图:
(1)石灰石样品的质量分数是 (结果保留一位小数,下同);
(2)a点溶液的pH 7(填“<”“>”或“=”);
(3)求所加盐酸的溶质质量分数(写出计算过程)。
推广车用乙醇汽油,可以减少汽车尾气污染。利用秸秆为原料可生产乙醇(C2H6O),其中包含葡萄糖(C6H12O6)转化为乙醇的反应(C6H12O6 2C2H6O+2CO2↑)。每生产2.3t乙醇,理论上参加反应的葡萄糖的质量是多少?(写出计算过程)
实验测成分
小伟同学在实验室中对某品牌除锈剂的有效成分及含量进行探究。
(1)定性检验:
小伟同学使用 、 分别与除锈剂反应,通过实验现象确定除锈剂的主要成分是硫酸。
(2)定量测定:
小伟同学利用碳酸钠溶液测定除锈剂中硫酸的质量分数,实验过程如下:
①向烧杯中加入50g除锈剂;
②向除锈剂中滴加碳酸钠溶液,边滴加边搅拌,至不再有气泡放出,共消耗碳酸钠溶液40g;
③反应后,烧杯中剩余物质的总质量为87.8g(除锈剂中其他成分不与碳酸钠反应,反应中产生的气体全部逸出)
根据上述实验数据计算除锈剂中硫酸的质量分数。
长期使用的热水锅炉会产生水垢。水垢主要成分是碳酸钙和氢氧化镁。某兴趣小组为了测定水垢中CaCO3的含量,将6g水垢粉碎放在烧杯中,然后向其中加入40g某浓度的稀盐酸,使之充分反应(水垢中除碳酸钙和氢氧化镁外都不与稀盐酸反应)。实验数据记录如下:
反应时间/min |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
烧杯内所盛物 质的总质量/g |
46.0 |
45.2 |
44.8 |
45.1 |
44.1 |
43.9 |
43.8 |
43.8 |
43.8 |
试计算:
(1)表中有一数据是不合理的,该数据的测得时间是第 min;
(2)水垢中CaCO3的质量分数(计算结果精确至0.1%)。
某同学用质量分数为15%的稀硫酸处理某造纸厂含NaOH的碱性废水样品:
(1)用9.2g质量分数为98%的浓硫酸能配制上述稀硫酸 g(计算结果保留整数)。
(2)若上述造纸厂废水75g能与9.8g 15%的稀硫酸恰好反应(设只发生NaOH与硫酸的反应),试计算该废水中NaOH的质量分数(写出计算过程,结果精确到0.1%)。
碳酸氢钠是面点膨松剂的主要成分之一。
小芳同学研究反应2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑中NaHCO3与CO2之间量的关系。
(1)理论计算:1.26g NaHCO3粉末与足量稀硫酸反应,计算生成CO2的质量(写出计算过程)。
(2)实验分析:小芳用右图装置进行实验,向盛有足量稀硫酸的锥形瓶中加入1.26g NaHCO3粉末,完全反应至不再产生气泡。称取反应前后质量如下表,发现反应前后质量变化值 (填“大于”、“小于”或“等于”)生成CO2质量的理论值,原因可能是 。
反应前 |
反应后 |
|
NaHCO3/g |
锥形瓶+稀硫酸/g |
锥形瓶+反应后溶液/g |
1.26 |
24.59 |
25.36 |
某化学拓展课堂的主题是:探秘氯化钠样品。
主题Ⅰ:探究氯化钠样品中杂质的成分
已知所提供的氯化钠样品中,可能含有硫酸钠、氯化镁、氯化钙中的一种或几种杂质。甲同学的实验探究过程记录如下: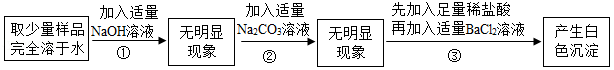
根据以上实验信息,甲同学得出结论:此氯化钠样品中含有的杂质是硫酸钠。
[实验分析]
(1)步骤①中加入适量NaOH溶液的目的是 。
(2)乙同学认为步骤③中不需要加入足量稀盐酸,你是否同意他的观点? (选填“同意”或“不同意”),请说明原因 。
主题Ⅱ:测定氯化钠样品中氯化钠的质量分数
确定了氯化钠样品中杂质的成分后,甲同学对样品中氯化钠的质量分数进行测定。称取20.0g氯化钠样品于烧杯中,加足量的水充分溶解,再向其中加入氯化钡溶液至不再产生沉淀为止,沉淀经过滤、洗涤、干燥后称量,其质量为2.33g。请计算该样品中氯化钠的质量分数。(写出计算步骤,计算结果精确到0.1%)
某纯碱样品中含有少量氯化钠杂质。称取该样品22.8g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。试回答:
(1)生成CO2的质量 。
(2)22.8g样品中氯化钠的质量为 。
(3)计算所得溶液中溶质的质量分数。(写岀解题过程,计算结果精确到0.1%)

用久的热水瓶内胆有一层水垢【主要成分是CaCO3和Mg(OH)2】。兴趣小组为了解具体成分进行了实验。他们取样品25克放入质量为100克的锥形瓶中,置于电子天平上,往瓶内加入150克稀盐酸时,恰好完全反应(样品中的杂质不与稀盐酸反应),此时天平示数如图。对所得混合物进行过滤、洗涤、干燥、称量,得到固体4.2克。请回答下列问题:
(1)恰好完全反应时,溶液中的溶质为 (填化学式)。
(2)样品中CaCO 3的质量分数是多少?
(3)反应结束时溶液中MgCl 2的质量分数是多少?(精确到0.1%)。

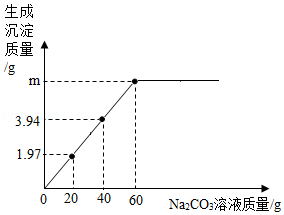
向200g NaCl和BaCl2的混合溶液中加入Na2CO3溶液。反应过程中滴加Na2CO3溶液的质量与生成沉淀的质量关系如图所示。请计算:
(1)m的值是 g;
(2)原混合溶液中BaCl2的质量分数是多少?
向200g NaCl和BaCl2的混合溶液中加入Na2CO3溶液。反应过程中滴加Na2CO3溶液的质量与生成沉淀的质量关系如图所示。请计算:
(1)m的值是 g;
(2)原混合溶液中BaCl2的质量分数是多少?

CO2是最主要的温室气体,也是巨大的碳资源,CO2的低能耗捕集、转化和利用正受到世界各国的广泛关注。
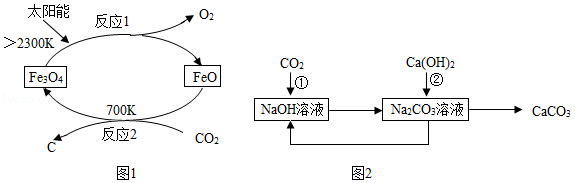
(1)以CO2为原料制取炭黑的太阳能工艺如图1所示。
①反应1的基本类型为 。
②反应2中碳元素的化合价 (填“升高”“不变”或“降低”)。
(2)利用NaOH溶液吸收CO2,部分转化关系见图2。
反应①的化学方程式为 ,该转化中循环使用的物质是 。
(3)利用Na2CO3或K2CO3溶液吸收低浓度的CO2,将其转化为NaHCO3或KHCO3,NaHCO3或KHCO3受热分解生成高浓度的CO2储存利用,生成的Na2CO3或K2CO3循环使用以降低生产成本。
吸收剂 |
Na2CO3 |
K2CO3 |
20℃最高浓度(g/L) |
212 |
1104 |
价格(元/Kg) |
1.25 |
9.80 |
根据表中信息,选择K2CO3溶液作吸收液的优点是 。
(4)利用一种新型“人造树叶”将CO2转化为乙醇(C2H5OH)的反应如下:2CO2+3H2O C2H5OH+3O2,研究显示,1L“人造树叶”每天能从空气中吸收968g CO2,计算1L“人造树叶”工作1天可得到乙醇的质量(写出计算过程)。
(5)某研究小组设计如图3所示实验,探究CO2和H2在一定条件下反应的产物。
查阅资料:①CO2和H2在合适催化剂和一定温度下反应转化为CO和H2O;
②白色无水硫酸铜吸水后变为蓝色。
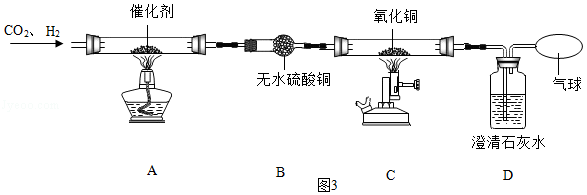
实验过程中观察到的主要现象有:B装置中白色固体变为蓝色,C装置中黑色固体变为红色,D装置中澄清石灰水变浑浊。
①设计B装置的目的是 。
②C装置中发生的反应的化学方程式为 。
③研究小组反思后认为,根据上述实验现象不能确认CO2和H2反应生成了CO,理由是 。