洁厕灵是常用的陶瓷清洗液,小彭同学对某品牌洁厕灵的有效成分及其含量进行研究。
(1)查阅资料得知:洁厕灵有效成分是HCl.HCl的含量可通过已知溶质质量分数的NaHCO 3溶液来测定,其它成分均不参与反应。请完成HCl与NaHCO 3反应的化学方程式:HCl+NaHCO 3=NaCl+ +CO 2↑。
(2)配制一定溶质质量分数的NaHCO 3溶液,需要用到的玻璃仪器有烧杯、滴管和 。
(3)向一锥形瓶中加入100克该品牌的洁厕灵,再逐次加入相同质量分数的 NaHCO 3溶液,测出每次锥形瓶中反应后溶液的总质量,数据记录如下:
| |
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
| 加入NaHCO 3溶液的质量/g |
40 |
40 |
40 |
40 |
40 |
| 反应后溶液的总质量/g |
138.9 |
177.8 |
216.7 |
255.6 |
295.6 |
试分析计算下列问题:
①第一次实验时,所加 NaHCO 3溶液中溶质质量是多少克?
②该品牌洁厕灵中HCl的质量分数是多少?
海洋是一个巨大的宝库,从海水中得到的食盐不仅可作调料,还可作化工原料。氯碱工业就是以电解食盐水为基础的,化学方程式为:2NaCl+2H 2O  Cl 2↑+H 2↑+2NaOH.某科学兴趣小组模拟氯碱工业,将一定浓度的氯化钠溶液通电一段时间(只发生上述反应),收集到0.02克H 2.停止通电,向所得溶液中加入10克盐酸后,溶液恰好为中性。求:
Cl 2↑+H 2↑+2NaOH.某科学兴趣小组模拟氯碱工业,将一定浓度的氯化钠溶液通电一段时间(只发生上述反应),收集到0.02克H 2.停止通电,向所得溶液中加入10克盐酸后,溶液恰好为中性。求:
(1)电解过程中消耗氯化钠的质量。
(2)所加盐酸中溶质的质量分数(用化学方程式计算)。
用"盐酸﹣﹣硫化钡法"生产BaCl 2会放出有毒气体H 2S(其水溶液有酸性),可用NaOH吸收H 2S制取Na 2S进行处理。如表为H 2S回收工艺的各项生产成本:
表:H 2S回收工艺的各项生产成本
| 项目 |
单价(元/吨) |
| NaOH |
2500 |
| Na 2S |
5000 |
| 辅助费用(以处理1吨H 2S计) |
1114 |
(1)工业处理尾气需考虑经济效益和社会效益,根据上述资料分析,单从经济效益考虑这种处理H 2S的方法是 (选填"盈利"或"亏损")的。
(2)若某化工厂每天要处理10吨H 2S,需消耗NaOH多少吨?(写出计算过程,结果保留1位小数)
在学习了金属的化学性质后,科学老师布置了一项课外学习任务:调查化工颜料店出售的涂料添加剂"银粉"是什么金属?某学习小组通过调查,分别获得了"银粉"是银粉、铝粉、锌粉这三种不同结果。为了确定究竟是哪一种金属,学习小组同学将一小包"银粉"带回实验室,进行了如下实验和分析。(相关反应的化学方程式为:Zn+2HCl═ZnCl 2+H 2↑;2Al+6HCl═2AlCl 3+3H 2↑)
(1)取少量"银粉"于试管中,滴加适量盐酸,观察到有 产生,说明"银粉"一定不是银。
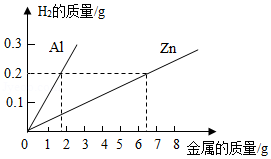
(2)为了进一步确定"银粉"是铝还是锌,学习小组通过理论计算,获得两种金属分别与足量盐酸反应产生氢气的质量关系,并绘制成如图所示图象。
(3)取1.8克"银粉"(杂质忽略不计)加入到50克稀盐酸中,恰好完全反应,生成氢气0.2克。根据如图可知,"银粉"是 。请计算:本实验所用稀盐酸的溶质质量分数为多少?
实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na 2CO 3的质量分数,小明进行了如下实验。
①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀盐酸100克;
②向上述3个烧杯中分别加入3份质量不同的样品;
③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出)。实验数据如下:
| |
实验一 |
实验二 |
实验三 |
| 反应前稀盐酸+烧杯质量(克) |
150 |
150 |
150 |
| 反应前固体样品质量(克) |
4 |
8 |
12 |
| 反应后烧杯内物质+烧杯质量(克) |
m |
155.8 |
158.7 |
已知实验中发生的化学反应:NaOH+HCl═NaCl+H 2O
Na 2CO 3+2HCl═2NaCl+H 2O+CO 2↑
(1)分析表中数据,写出判断实验二中的样品已完全反应的理由: 。
(2)表中的m值为 。
(3)根据实验二中的数据计算样品中Na 2CO 3的质量分数。
某兴趣小组设计如下实验探究质量守恒定律。
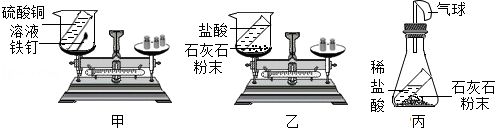
(1)如图甲,小柯将烧杯放在天平左盘,使天平重新平衡。然后取下烧杯把铁钉放入试管中,一段时间后,再把烧杯放回天平左盘,最后天平是否平衡? 。反应后试管内溶液的质量 (选填"增加"、"减少"或"不变")。
(2)如图乙,小妍将烧杯放在天平左盘,使天平重新平衡。然后倾斜烧杯使盐酸与石灰石粉末混合,一段时间后再把烧杯放回天平左盘,发现天平不再平衡。其原因是 。小柯对该实验装置进行改进,把烧杯换成锥形瓶(如图丙,装置气密性良好)。你认为能否验证质量守恒定律并阐述理由: 。
(3)小妍想测定实验所用石灰石中碳酸钙的质量分数,取6克石灰石粉末与足量的稀盐酸充分反应,反应后总质量减少2.2克。求石灰石中碳酸钙的质量分数(杂质与稀盐酸不反应)。(结果精确到0.1%)
徐州地区石灰石资源丰富。某化学兴趣小组称取4.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 |
剩余固体的质量 |
第一次加入10g |
3.0g |
第二次加入10g |
2.0g |
第三次加入10g |
l.0g |
笫四次加入10g |
0.6g |
请计算:
(1)4.0g石灰石样品中碳酸钙的质量是 g。
(2)10g稀盐酸能与 g碳酸钙正好完全反应。
(3)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1% )。
牙膏中的摩擦剂可以增强牙膏对牙齿的摩擦作用和去污效果。已知某品牌牙膏中的摩擦剂是CaCO3和SiO2(SiO2不溶于水也不与稀盐酸反应)。为了测定摩擦剂中CaCO3的质量分数,通过实验测得如图数据:

(1)生成CO2质量为 g;
(2)求摩擦剂中CaCO3的质量分数。
高铁酸钠(Na2FeO4)是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为:3NaClO+2Fe(NO3)3+10NaOH═2Na2FeO4↓+3NaCl+6NaNO3+5H2O
(1)在Fe(NO3)3中,铁元素和氮元素的质量比为 (填最简比)。
(2)现称取44.7g次氯酸钠,最多能制得高铁酸钠的质量是多少?(列式计算)
温馨提示:NaClO的相对分子质量为74.5;Na2FeO4的相对分子质量为166。
汽车制造是盐城市的支柱经济产业之一,汽车制造过程中要用到大量的铁、铜、铝等金属材料,请按要求填空.(1)汽车制造中用得最多的金属材料是钢.钢 (填"是"或"不是")纯金属.车体表面喷漆不仅美观,而且可有效防止钢铁与 接触而生锈.炼铁的原理是利用一氧化碳与氧化铁反应还原出铁,反应的化学方程式为 .
(2)汽车电路中的导线大都是铜芯的,这主要是利用了铜的 性.将赤铜矿(主要成分Cu 2O)和辉铜矿(主要成分Cu 2S)混合焙烧可得到铜,请将反应的方程式补充完整:2Cu 2O+Cu 2S  6Cu+ .
6Cu+ .
(3)铁、铜、铝三种因素在地壳中的含量多少顺序为Al>Fe>Cu,但三种金属被人类发现和利用的时间是铜最早,而铝最晚,这跟它们的 有关.铝具有很好的抗腐蚀性能,原因是 .
(4)镁铝合金是汽车制造中的重要材料之一.为测定某镁铝合金(只含镁、铝两种元素)的组成成分,某学习小组取3.9g合金粉末加入100.0g过量的盐酸中,向充分反应后的溶液中加入过量20.0%的氢氧化钠溶液,最终得到沉淀2.9g.
【质疑】通过讨论,大家认为得到的沉淀质量数据可能有问题.按初中化学现有知识计算,沉淀的质量至少为 g.
【探讨】经向老师请教,同学们了解到氢氧化铝沉淀可与氢氧化钠溶液反应,产生可溶性的偏铝酸钠,反应如下:NaOH+Al(OH) 3═NaAlO 2+2H 2O
【计算】若已知产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示,请计算:
①该合金中镁的质量为 g;铝的质量为 g.
②加入的盐酸溶质质量分数为多少?(请写出计算过程)

某兴趣小组用熟石灰中和实验室用含有硫酸的废水,向100g该废水样品中加入7.4g熟石灰,恰好完全反应(废水中的其它物质不参与反应).
(1)请完成该反应的化学方程式:H 2SO 4+Ca(OH) 2═CaSO 4+ .
(2)计算该废水中H 2SO 4的质量分数(写出计算过程)
为测定某黄铜(铜、锌合金)中铜的质量分数,某同学取20g黄铜样品放入盛有200g稀硫酸的烧杯中,恰好完全反应(铜与稀硫酸不反应),测得烧杯中剩余物质的总质量为219.8g,试计算:
(1)生成氢气的质量 g.
(2)该黄铜样品中铜的质量分数,所用稀硫酸的溶质质量分数.(写出计算过程)
向盛有26.4g硫酸钠和碳酸钠混合物的烧杯中加入218g稀硫酸,恰好完全反应,固体全部消失,烧杯内物质总质量减少了4.4g。(化学反应方程式为Na 2CO 3+H 2SO 4═Na 2SO 4+H 2O+CO 2↑),请计算:
(1)原混合物中碳酸钠的质量。
(2)反应后所得溶液中溶质的质量分数。
在锥形瓶中加入80.0g质量分数为10%的硫酸铜溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净后在天平上称得质量为56.0g,再将盛有硫酸铜溶液的锥形瓶和铁钉一起放在天平上称量,记录所称得质量m 1.将上述铁钉浸到硫酸铜溶液中,待反应一段时间后溶液颜色改变时,将盛有硫酸铜溶液和锥形瓶放在天平上称量,记录所称的质量为m 2。
(1)m 1 m 2(填">"或"="或"<")。
(2)锥形瓶的质量为 (用含m 1或m 2的代数式表示)。
(3)若硫酸铜反应完全,求此时所得溶液的质量(写出计算结果)。