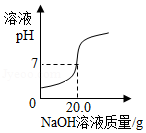
梧州市某化学兴趣小组检测某硫酸厂排放的废液中硫酸的含量,取废液样品100g,逐滴加入4%的NaOH溶液,溶液的pH随加入NaOH溶液质量变化如图所示(假设废液中其它成分均为中性,且不和NaOH反应)。
请计算:
(1)H 2O的相对分子质量= 。
(2)该废液中硫酸的质量分数。(结果精确到0.01%)
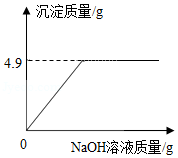
将氯化钠和氯化铜的固体混合物20g完全溶于100g水中,再向所得的溶液中加入溶质质量分数为10%的NaOH溶液。有关的变化如图所示。(反应的化学方程式为:CuCl 2+2NaOH═Cu(OH) 2↓+2NaCl)请计算:
(1)NaOH中氧元素和氢元素的质量比为 。
(2)求恰好完全反应时,所用NaOH溶液的质量。(写出计算过程)
(3)求恰好完全反应时溶液中溶质的质量分数。(写出计算过程,结果精确到0.1%)
为测定某过氧化钠样品的纯度,将2g该样品与足量水发生如下反应(杂质不参与反应):2Na 2O 2+2H 2O═4NaOH+O 2↑生成气体质量与时间的关系如图所示。回答问题:
(1)生成氧气的质量是 g。
(2)列式计算该样品中过氧化钠的质量分数。

某兴趣小组在实验室用硫酸铜溶液和氢氧化钠溶液制取少量氢氧化铜固体。他们的实验过程和相关数据如图所示。请计算:
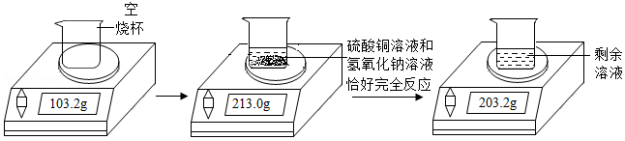
(1)生成沉淀的质量为 g。
(2)恰好完全反应后所得溶液的溶质质量分数。
4分)某工厂化验室用56%的氢氧化钾溶液洗涤50g石油产品中的残余硫酸。它们的关系如图所示。计算:这种石油产品中硫酸的溶质质量分数。

某样品由氧化铜和铜组成。取10.0g该样品于烧杯中,向其中加入92.0g稀硫酸,恰好完全反应后,过滤,所得滤液质量为100.0g。
(1)所取样品中铜的质量为 。
(2)从反应后所得的100.0g滤液中取出10.0g溶液,将其稀释为10%的溶液,需要加水多少克?
为测定某黄铜(铜锌合金)样品中铜的含量,某化学活动小组分三次进行实验,实验数据如表,请回答下列问题:
所取药品 |
第一次 |
第二次 |
第三次 |
黄铜样品质量(g) |
12 |
10 |
10 |
稀盐酸质量(g) |
100 |
100 |
150 |
生成气体质量(g) |
0.2 |
0.2 |
0.2 |
(1)第 次实验中,药品成分恰好完全反应。
(2)黄铜样品中铜的质量分数是多少?恰好完全反应时所得溶液的溶质质量分数是多少?(精确到0.1%)
某实验小组欲测定一瓶Ba(NO 3) 2溶液的质量分数,取100g Ba(NO 3) 2溶液,向其中逐渐加入Na 2SO 4溶液,加入溶液质量与生成沉淀质量关系如下表:
| 次数 |
1 |
2 |
3 |
4 |
5 |
| 加入Na 2SO 4溶液质量/g |
20 |
40 |
60 |
80 |
100 |
| 生成沉淀质量/g |
2.33 |
4.66 |
m |
9.32 |
9.32 |
(1)表格中m的数值为 ;
(2)加入Na 2SO 4溶液与原Ba(NO 3) 2溶液质量比为 时恰好完全反应;
(3)计算原Ba(NO 3) 2溶液溶质的质量分数。
某混合溶液中含有硫酸和盐酸,取该混合溶液20g于烧杯中,不断滴加氢氧化钡溶液,反应过程中烧杯中产生沉淀的质量、溶液pH的变化如图所示(BaCl 2溶液呈中性)。求:
(1)完全反应后生成沉淀的质量为 g;
(2)计算20g混合溶液中HCl的质量为多少?

为了测定某硫酸铜溶液的质量分数,小杨同学取50.0g样品置于烧杯中,逐滴加入氢氧化钠溶液,加入氢氧化钠溶液质量和生成沉淀质量的关系如图所示。请计算:
(1)NaOH的化学式量为 。
(2)硫酸铜刚好完全反应时,所得溶液的质量为 g(保留一位小数)。
(3)硫酸铜溶液中溶质的质量分数是多少?(写出计算过程)

有一袋已部分变质的Ca(OH) 2(含杂质CaCO 3)固体样品,把该样品投入足量水中,充分搅拌后通入二氧化碳,沉淀质量与反应的二氧化碳质量关系如图所示。【提示:CO2+Ca(OH)2=CaCO3↓+H2OCO2+CaCO3+H2O=Ca(HCO3)2】
请回答下列问题
(1)Ca(OH) 2由 元素组成,其中H元素与O元素的原子个数比为 ;
(2)碳酸钙(CaCO 3)的相对分子质量为 ;
(3)生成沉淀最多时,参加反应的气体质量为 g;
(4)计算样品中碳酸钙的质量分数。(要求写出计算过程,结果精确到0.1%)

某纯碱样品中含有少量的氯化钠。取该样品13.9g完全溶于206.1g水中,加入90g CaCl 2溶液,恰好完全反应
后生成沉淀的质量为10g。求:
(1)生成的沉淀物的化学式为: ;
(2)样品中碳酸钠的质量为: g;
(3)反应后溶液中溶质质量分数。(要求写出计算过程)
食用小苏打含有 NaHCO 3外还含有少量NaCl.为了测定某食用小苏打中NaHCO 3的质量分数,某同学做了如下实验:称取一定量该样品于烧杯中,加水使其完全溶解,得到104.4g溶液,再向其中滴加100g稀盐酸,恰好完全反应时得到200g溶质质量分数3.1%的不饱和溶液。(反应的化学方程式为:NaHCO 3+HCl═NaCl+H 2O+CO 2↑)请计算:
(1)NaHCO 3中碳、氧元素的质量比为 ,
(2)生成CO 2的质量为 g,
(3)该食用小苏打中 NaHCO 3的质量分数(写出计算过程)。
将氯酸钾和二氧化锰的固体混合物20g加入试管中,加热。待完全反应后,将试管冷却、称量,试管内固体物质为15.2g。计算:
(1)反应生成的氧气质量为 g。
(2)列式计算原固体混合物中氯酸钾的质量。