工业上用电解氧化铝的方法制金属铝,反应的化学方程式为:
2Al2O3 4Al +3O2↑。
4Al +3O2↑。
如果制得54g铝,计算需要电解氧化铝的质量。
钛(Ti)和钛合金被认为是21世纪的重要金属材料。钛可通过如下反应制得:TiCl4 + 2Mg  Ti + 2MgCl2。若要制得24 g钛,请计算需要镁的质量。
Ti + 2MgCl2。若要制得24 g钛,请计算需要镁的质量。
发射通讯卫星的火箭用联氨(N2H4)做燃料,用四氧化二氮(N2O4)助燃,生成物不会对大气造成污染,其反应的化学方程式为:2N2H4 + N2O4 点燃 3N2 + 4H2O,请计算12.8 g N2H4完全燃烧需要N2O4的质量。
四氯化硅(
)是一种 重要的化工原料,遇水会发生如下反应:
某地曾发生将含有四氯化硅的废料倒入池塘造成污染的事件,事后环保人员在受污染的池塘中投放熟石灰〔
〕作了有效处理。
(1)已经
不跟
反应,为了确定投入熟石灰的质量,要先测定废料倒入池塘后生成盐酸的质量。选用下列哪组数据能确定池塘中生成
的质量
A.倒入废料的总质量、废料中
的质量分数
B.池塘水的
C.池塘水中
的质量分数
(2)经测定池塘水中共有0.365吨盐酸,则需要加入多少吨熟石灰才能将其完全反应。
(列式计算,相对原子质量:
:1
:16
:35.5
:40)
(2分)氢化钙(CaH2)固体可用于登山队员的能源提供剂,它和水反应生成氢氧化钙和氢气:CaH2 + 2H2O ="=" Ca(OH)2 + 2H2↑,氢气供燃烧之需。现有84g氢化钙与足量水反应,可生成多少克氢气?
古代湿法炼铜的反应原理是:Fe+CuSO4= FeSO4+Cu,若得到16Kg的铜,理论上需要铁质量是多少?
某氯化钠溶液中含有氯化镁(MgCl2),学习小组为测定其中氯化镁的质量分数,在50.0g该溶液中加入50.0g氢氧化钠溶液恰好完全反应,经测定生成沉淀的质量为2.9g。请回答下列问题:
(1)反应后溶液的质量为 g;
(2)求原氯化钠溶液中氯化镁的质量分数(写出计算过程)。
某工厂化验室用20%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液20g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少?(写出计算过程)
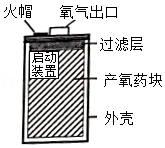
某简易制氧装置的示意图如图,其原理是通过撞击火帽触发启动装置产生热量,使产氧药块分解而持续释放氧气。
(1)装置中过滤层的作用是 。
(2)若产氧药块由氯酸钾(KClO3)和二氧化锰等组成,为得到一个人呼吸2小时所需氧气的量(折算后质量为48g),计算产氧药块中至少含氯酸钾的质量(写出计算过程)。
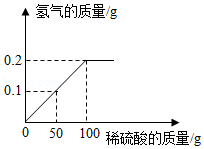
铜锌合金又称假黄金。向盛有30g铜锌合金粉末样品的烧杯中逐渐加入稀硫酸,生成氢气的质量与加入稀硫酸的质量关系如图所示,计算:
(1)充分反应后生成氢气的质量为 g。
(2)合金样品中锌的质量。
(3)恰好完全反应时,所得溶液溶质的质量分数。(结果保留一位小数)
科学兴趣小组同学在综合实践活动中了解到,某石灰厂有一批石灰石原料,其中含有的杂质二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组同学取用2克这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸20克分4次加入,充分反应后,经过滤、干燥等操作后称量,每次盐酸用量及剩余固体的质量见表,利用实验数据绘制的图象见图.
| 稀盐酸的用量 |
剩余固体的质量 |
| 第一次加入5克 |
1.5克 |
| 第二次加入5克 |
克 |
| 第三次加入5克 |
0.5克 |
| 第四次加入5克 |
0.3克 |
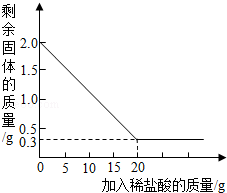
计算:
(1)分析上述图与表,第二次加入稀盐酸后,剩余固体的质量是 克;
(2)该石灰石样品中碳酸钙的质量分数;
(3)所用稀盐酸中溶质的质量分数是多少?
某化学兴趣小组同学在进行实验室制取氧气时,取了34.0g 过氧化氢溶液,又称取了0.5g二氧化锰,放入烧杯中至不再产生气泡,称得烧杯内剩余物的质量为33.7g,
求:(1)生成氧气的质量是多少?
(2)参加反应的过氧化氢的质量是多少?
请根据下图所示的实验过程和提供的数据计算:
(1)最终生成的不饱和溶液中溶质的质量为 。
(2)合金中铜的质量分数 ;
(3)求所加稀硫酸的溶质质量分数。
(4)(1)配制本实验需要的稀硫酸,大斌选用的是98%的浓硫酸,请问在配制过程中需要另外加水多少克?
某同学取2.5g石灰石,滴加30g稀盐酸,所产生的气体质量与滴入盐酸质量的关系如下图所示。
试根据图中数据计算:
Ⅰ.反应生成二氧化碳的物质的量为 (19) mol.
Ⅱ.石灰石中碳酸钙的质量分数(根据化学方程式计算)。(20)
Ⅲ.该反应结束后,所得溶液中滴加石蕊试液,可观察到现象是 (21) 。
某化工厂用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取12g纯碱样品放入烧杯中,称得烧杯及纯碱样品的总质量为158g,再把100g稀盐酸平均分成四份,依次加入到样品中,每次均充分反应。实验数据记录如下:
| 所加盐酸的次数 |
第一次 |
第二次 |
第三次 |
第四次 |
| 盐酸的质量/g |
25 |
25 |
25 |
25 |
| 烧杯及所盛物质总质量/g |
181.2 |
204.4 |
228.6 |
253.6 |
请计算:(要求计算过程)
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量。
(2)该产品中碳酸钠的质量分数是否合格?