下列操作或反应所对应的曲线正确的是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|
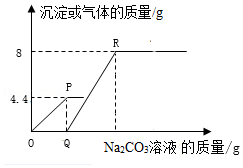
向一定质量CaCl 2和HCl的混合溶液中逐滴加入溶质质量分数为10.6%的Na 2CO 3溶液,实验过程中加入Na 2CO 3溶液的质量与产生沉淀或气体的质量关系如图所示,下列说法错误的是( )
| A. |
P点时的溶液中只含一种溶质 |
| B. |
R点对应坐标的数值为180 |
| C. |
O至P过程中溶液的pH变大 |
| D. |
Q至R段表示生成沉淀的过程 |
现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中不正确的是( )

A.生成氢气的质量:甲>乙>丙
B.相对原子质量:乙>丙>甲
C.金属活动性:乙>甲>丙
D.消耗硫酸的质量:甲>乙>丙
下面是同学们在复习中梳理得到的一组图象,其中图象与实验描述一致的是( )
A. 将氢氧化钡溶液逐滴滴入稀硫酸中至过量
将氢氧化钡溶液逐滴滴入稀硫酸中至过量
B.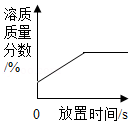 浓硫酸敞口放置一段时间
浓硫酸敞口放置一段时间
C.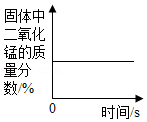 加热一定量氯酸钾和二氧化锰固体的混合物
加热一定量氯酸钾和二氧化锰固体的混合物
D. 等质量的镁、铁分别与溶质质量分数相等且足量的稀硫酸反应
等质量的镁、铁分别与溶质质量分数相等且足量的稀硫酸反应
一定质量M、N两种金属,分别与相同质量和相同质量分数的稀硫酸反应,生成氢气的质量与反应时间的关系如图所示。分析图象得到的以下结论中,不正确的是( )

A.两种金属的活动性:M>N
B.两种金属生成氢气的质量:M=N
C.两种金属消耗稀硫酸的质量:M=N
D.充分反应后,得到溶液的质量:M=N
在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金属,其发生反应的质量关系如图所示,读识如图并判断,下面推理合理的是( )
①反应速率:Mg>Fe>Zn
②反应生成氢气质量:Mg=Fe=Zn
③反应后溶液质量:Mg=Fe=Zn
④反应后溶液溶质质量分数:Mg<Fe<Zn。

A.①②B.③④C.①③D.②④
某研究所利用热分析仪对草酸钙晶体(CaC 2O 4•xH 2O)进行热分解,获得相关数据,绘制成固体质量﹣分解温度的关系如图所示。下列说法正确的是( )

A.CaC 2O 4•xH 2O中x=2
B.500~650℃范围内的残留固体为CaC 2O 4
C.固体质量由12.8g变为10.0g时发生的反应为CaC 2O 4  CaCO 3+CO↑
CaCO 3+CO↑
D.800℃以上时,固体成分的化学式为CaCO 3
向质量均为m的锌粉和铁粉中分别滴加100g相同质量分数的稀硫酸,反应过程中产生气体的质量与所加稀硫酸的质量关系如图所示,下列叙述正确的是( )

A.反应后均得到无色溶液
B.反应结束后两种金属均有剩余
C.折线b表示的是铁和稀硫酸反应的情况
D.反应结束后所得溶液的质量相等
能反映相关实验过程中量的变化的图象是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|
活性炭可处理大气污染物NO.在一定条件下的密闭容器中,NO气体与活性炭中的C反应生成甲、乙两种气体,其中甲是空气中含量最多的气体.测得各物质的质量如下表所示:
物质质量/g 反应时间/min |
活性炭 |
NO |
甲 |
乙 |
0 |
28.72 |
5.00 |
0 |
0 |
4 |
28.00 |
1.40 |
x |
2.64 |
下列说法正确的是( )
A.生成甲、乙的分子数之比为1:1
B.反应消耗的C与NO的质量之比为2:5
C.x的值为26.76
D.反应中活性炭只起吸附作用
质量相同的下列四种物质,完全分解后制得氧气质量最多的是( )
A.H2O2B.H2OC.KClO3D.KMnO4
如图对应关系正确的是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|
120℃时,取3g有机物R在氧气中完全燃烧,产物只有CO 2和H 2O.将其燃烧产物依次通过足量的浓硫酸和足量的澄清石灰水中,最终浓硫酸增重1.8g;澄清石灰水中产生10g沉淀。下列判断正确的是( )
A.R的化学式一定是CH 2O
B.6g R完全燃烧消耗氧气6.4g
C.R中碳元素的质量分数约为85.7%
D.R仅由C、H两种元素组成,其质量比为6:1
工业上常用空气中的氮气生产硝酸,其反应方程式如下:
①N 2+3H 2  2NH 3②4NH 3+5O 2
2NH 3②4NH 3+5O 2  4NO+6H 2O
4NO+6H 2O
③2NO+O 2═2NO 2④3NO 2+H 2O═2HNO 3+NO(NO难溶于水)
下列说法错误的是( )
A.上述①②③④中反应前后均有元素化合价的变化
B.用H 2O吸收NO 2的过程中通入过量的O 2可以提高硝酸的产量
C.反应②④都不属于四种基本反应类型中的任何一种,反应①③均属于化合反应
D.在密闭容器中,将46g NO 2溶于64g H 2O中形成HNO 3溶液,其溶质的质量分数约为38.2%