回答下列问题。
(1)某兴趣小组参观火力发电厂,了解到废气中的SO2、NO2、CO、CO2会影响环境,设计如图流程处理废气。
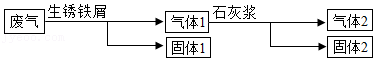
①用生锈铁屑处理废气中的CO,体现CO 性。
②用石灰浆不用石灰水的原因是 。
③固体2中有 (写两种物质)。
(2)A~D为初中化学常见物质,转化关系如图。A是由两种元素组成的钙盐,C是火力发电厂排放的温室气体。
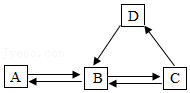
①B转化为A的化学方程式为 。
②若D广泛用于玻璃、洗涤剂的生产,则D转化为B的基本反应类型是 ;检验D中阴离子的方法是 。
③将足量C通入石蕊溶液中,现象是 ;测得该溶液pH=4,加热至90s时C完全排出,画出加热过程pH变化图像。
金属在生产和生活中的应用极为广泛。
(1)生铁和钢是两种含碳量 的铁合金(填“相同”或“不同”)。
(2)下列生活用品利用金属良好导热性的是 (填序号)。
A.镀铬水龙头
B.铸铁暖气片
C.黄铜钥匙
(3)我国古代很早就认识到铜盐溶液里的铜能被铁置换,这一方法是湿法冶金技术的起源。铁与硫酸铜溶液反应的化学方程式为 。
(4)焊接钢轨的反应原理是铝与氧化铁在高温条件下反应生成铁和氧化铝,该反应的化学方程式为 。
(5)已知氧化镁和氧化铝都能与酸反应生成盐和水。现有氧化镁、氧化铝和铁的混合物9.9g,向其中加入245g质量分数为10%的稀硫酸,恰好完全反应,得到254.8g溶液,则原混合物中氧化镁的质量为 g。
铁及其化合物在生产生活中有广泛的应用。
(一)铁的应用和防护
(1)某麦片中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的铁元素,反应的化学方程式为 。
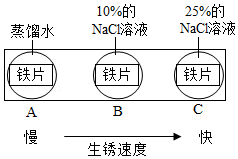
(2)铁锈主要成分是Fe 2O 3•nH 2O,铁生锈主要与空气中的 有关。
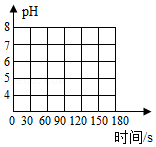
(3)如图实验说明NaCl在铁生锈中的作用是 。
(4)铁生锈的次要过程:Fe 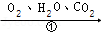 FeCO 3•nH 2O
FeCO 3•nH 2O  FeCO 3
FeCO 3
写出Fe转化为总反应的化学方程式 。
(5)为防止铁生锈,可对铁制品进行"发蓝"处理,使其表面生成致密氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为 。
(二)废铁的再利用
黄钠铁矾[NaFe x(SO 4) y(OH) z]是一种高效净水剂。用废铁屑(主要成分为Fe,含少量Fe 2O 3和FeCO 3)制备黄钠铁矾的主要流程如图:
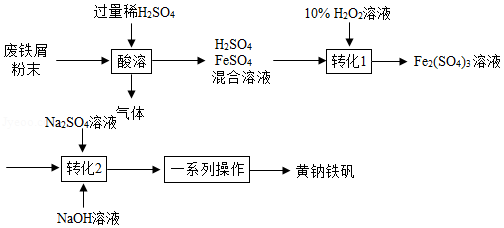
(1)将废铁屑研磨成粉末的目的是 。
(2)"酸溶"时H 2SO 4与Fe、FeCO 3反应,还发生反应的化学方程式有 和Fe+Fe 2(SO 4) 3=3FeSO 4。
(3)"转化1"发生反应的化学方程式为 。反应时温度不宜过高的原因是 。
(三)黄钠铁矾组成确定
称取9.70g黄钠铁矾,用如图装置进行热分解实验。
【资料】
①NaFe x(SO 4) y(OH) z在T 1℃分解会生成H 2O(气态),提高温度至T 2℃继续分解产生SO 3气体,并得到Fe 2O 3和Na 2SO 4。
②浓硫酸可用于吸收SO 3。
(1)装配好实验装置后,先要 。
(2)分别控制温度在T 1℃、T 2℃对A中固体加热。
①控制温度在T 1℃加热,实验后测得B装置质量增加1.08g。
②用D装置替换B装置,控制温度在T 2℃,加热至反应完全。
③T 1℃、T 2℃时,加热后均通入一段时间N 2,目的是 。
(3)反应完全后,将A装置中固体溶于足量水,过滤、洗涤、烘干得4.80g固体,将滤液蒸干得1.42g固体(不含结晶水)。
结论:NaFe x(SO 4) y(OH) z中,x:y:z= 。
反思:若该实验过程中缺少C装置,则x:z的值 (选填"偏大""偏小"或"不变")。
科学课上,老师告诉学生“能发生复分解反应的两种盐通常是可溶的”.有“通常”就有“例外”,能否找到某些可溶性盐和难溶性盐发生复分解反应的证据呢?科学兴趣小组进行了探究.
【查阅资料】①水溶液中的复分解反应一般朝着溶液中离子浓度(单位体积溶液中离子数目的多少)减少的方向进行.
②了解到某些难溶性盐的溶解能力和颜色.
3溶液,再加入过量NaCl溶液,有白色沉淀生成.
再往该试管中加入少量KI溶液,白色沉淀转化为黄色沉淀.
【分析讨论】(1)为什么要加入过量的NaCl溶液?请说明理由.
(2)写出加入少量KI溶液后发生反应的化学方程式.
(3)该反应能发生的原因是AgI在水中的溶解能力 AgCl(选填“大于”、“等于”或“小于”).
【得出结论】某些可溶性盐和难溶性盐之间能发生复分解反应.
某实验小组在做“用澄清石灰水检验二氧化碳”的实验时,发现一个有趣的实验现象:

试管中浑浊现象为何消失?实验小组的同学对此实验进行了下列探究活动:
(1)根据已学知识,实验小组对CO2使澄清石灰水变浑浊的现象作出了合理的解释,其化学方程式为 。
(2)【查阅资料】
①碳酸盐一般不溶于水,如碳酸钙不溶于水。
②碳酸钙能与二氧化碳、水反应生成碳酸氢钙[Ca(HCO3)2],碳酸氢钙易溶于水。
③碳酸氢钙受热易分解,生成碳酸钙、二氧化碳、水。
从物质组成角度分类,碳酸氢钙应属于 。
A.氧化物 B.酸 C.碱 D.盐
写出碳酸氢钙受热分解的化学方程式 。
【提出问题】碳酸氢钙能与哪些物质反应呢?
【假设与猜想】猜想I:能与盐酸反应
猜想∐:能与氢氧化钠反应
……………
(3)【设计实验并验证】
实验步骤 |
实验现象 |
结论 |
实验一:取丙中少量液体于试管中,滴加稀盐酸 |
有 生成 |
猜想I成立 |
实验二:取丙中少量液体于试管中,滴加氢氧化钠溶液 |
有白色沉淀生成 |
猜想II成立 |
实验三:取丙中少量液体于试管中,加热 |
澄清液体又变浑浊 |
验证了资料描述 |
根据验证实验写出碳酸氢钙与盐酸反应的化学方程式 。
【讨论与反思】
该实验小组在实验中发现问题,并对问题进行不断探究。他们不但发现了新的物质,还了解了它的一些性质,并对生活中煮沸可以降低水的硬度、水垢的形成以及自然界中溶洞与钟乳石的形成有了更进一步的认识。
化学兴趣小组的同学在探究碱的化学性质时,完成了如图1所示的两个实验。实验后,小明同学将废液倒入同一废液缸中,发现混合废液浑浊并显红色。请你完成下列问题:
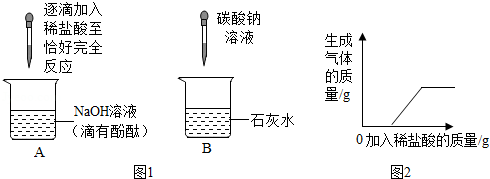
(1)A实验中发生反应的现象为 。
(2)B实验中发生反应的化学方程式是 。
(3)【提出问题】废液中,能使酚酞溶液变红的物质可能是哪些呢?
【作出猜想】猜想一:废液中,能使酚酞溶液变红的物质可能是NaOH;
猜想二:废液中,能使酚酞试液变红的物质还可能是 ;
猜想三:废液中,能使酚酞溶液变红的物质还可能是Ca(OH)2。
【实验验证】同学们对可能含有的碱性物质进行确定,取一定量的废液过滤,向滤液中逐滴加入稀盐酸,根据反应现象得到如图2所示的图象。
【结论】分析图象数据得出,废液中使酚酞变红的物质一定是 ,一定不是 。
【拓展提高】为了使以上废液实现安全排放,你的做法是 。
铝是重要的轻金属,广泛应用于航空、电讯和建筑领域。铝亦有其特殊的性质,试根据以下信息填空或简答。
(1)按金属的活动性顺序,铝比锌 。但是将铝片和锌粒分别投入稀硫酸中,铝片表面产生的气泡却比锌粒少而慢。为了探究铝与酸反应的规律,小强用相同质量、相同形状的光亮铝片设计如下实验。
实验一 |
实验二 |
实验三 |
实验四 |
|
实验现象 |
铝表面产生气泡很小且慢 |
铝表面产生大量气泡 |
铝表面产生大量气泡 |
铝表面产生大量气泡且快 |
(2)比较实验三、实验四说明铝与酸反应产生氢气的速率,与 有关。
(3)比较实验一、实验二说明铝与酸反应产生氢气的速率,可能与 、 粒子和温度、金属与酸的接触面积等多种因素有关。
(4)写出实验二中发生反应的化学方程式 。
(5)小芳将长条状铝片的一端放在酒精灯火焰上灼烧片刻,轻轻摇动铝条,受热一段会左右摇晃,却不像蜡烛那样滴落。为探究其原因,小芳查阅资料得知:铝的熔、沸点分别是660℃、2460℃;氧化铝的熔、沸点分别为2054℃、2980℃。
试解释上述实验现象: 。