下列化学反应既是氧化还原反应又是化合反应的是( )
A.2NaOH+H2SO4═2H2O+Na2SO4
B.H2CO3═CO2↑+H2O
C.3Fe+2O2 Fe3O4
D.Mg+2HCl═MgCl2+H2↑
钛(Ti)和钛合金是二十一世纪重要的金属材料,享有“未来金属”的美称,可用于制造航天飞机、船舶等。钛的冶炼方法很多,方法之一是利用二氧化钛和金属铝在高温条件下发生置换反应制得,该反应的化学方程式为 ,该反应中化合价升高的元素是 ,该反应中发生还原反应的物质是 。
工业炼铁中会发生一氧化碳与氧化铁的反应,该反应中发生还原反应的物质是( )
A.COB.Fe2O3C.CO2D.Fe
化学反应C+H 2O H 2+CO中的还原剂是( )
| A. |
C |
B. |
H 2O |
C. |
H 2 |
D. |
CO |
电脑芯片的制作要用到高纯度的硅。目前广泛采用石英砂(主要成分是SiO 2)为原料制取,其中一步反应为:SiO 2+2C  Si+2CO↑.对该反应分析正确的是( )
Si+2CO↑.对该反应分析正确的是( )
| A. |
该反应属于置换反应 |
B. |
碳发生了还原反应 |
| C. |
碳元素化合价由0价变为+4价 |
D. |
该反应利用了CO的还原性 |
地壳中的元素分布(质量分数)如图,请回答下列问题。
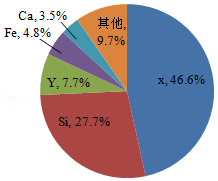
(1)元素X是 ,由X与Y组成的化合物的化学式是 。
(2)地壳中的赤铁矿(Fe2O3)与CO高温反应可炼铁,其中Fe2O3发生了 反应(填“氧化”或“还原”)。
(3)如图是Si与Cl2反应生成SiCl4的图示,请在方框内补充所缺反应物的图示。

某化学兴趣小组探究常温下碳酸钠饱和溶液的酸碱度.
[猜想与假设]溶液的pH可能是(填入你的猜想与假设):
①pH>7;②pH ;③pH .
[设计与实验]小方、小钟、小陈三位同学进行了如下实验:
小方:取pH试纸于玻璃片上,用玻璃棒蘸取碳酸钠溶液沾在pH试纸上,测得pH>7.
小钟:取pH试纸于玻璃片上,先用蒸馏水润湿pH试纸,然后用玻璃棒蘸取碳酸钠溶液沾在pH试纸上,测得pH>7.
小陈:取pH试直接浸入碳酸钠溶液中,测得pH>7.
[评价]以上三位同学中操作规范的是 同学,其余两位同学操作上的错误是
; .
根据下列实验现象可以判断某溶液一定呈碱性的是( )
| A.常温下,测得溶液的pH<7 | B.溶液中滴入酚酞显红色 |
| C.溶液中滴入石蕊显红色 | D.溶液中滴入酚酞不显色 |
将pH=10的氢氧化钠溶液加水稀释后,所得溶液的pH可能是( )
| A.6 | B.8 | C.11 | D.14 |
向稀盐酸中逐渐加入试剂X后,溶液的pH变化情况如图所示.试剂X是下列物质中的( )

| A.Mg | B.H2O | C.NaOH | D.CaCO3 |
下列反应中属于中和反应的是( )
| A.Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
| B.2NaOH+H2SO4═Na2SO4+2H2O |
| C.CO2+2NaOH═Na2CO3+H2O |
| D.Fe+CuSO4═Cu+FeSO4 |
U形管中是滴有酚酞试液的蒸馏水,向左、右两管中同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示).
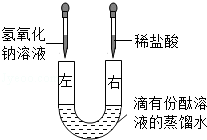
(1)开始时 管溶液呈红色.
(2)充分反应后U形管中溶液全部呈无色,除酚酞外,此时溶液中一定含有的溶质的名称为 ,可能含有的溶质的化学式为 ,写出上述反应的化学方程式 .
在氢氧化钠溶液中加入一定量的稀盐酸后,下列实验能证明两者恰好完全中和的是
| A.滴入适量FeCl3溶液,溶液变黄,但无沉淀生成 |
| B.滴入几滴酚酞试液,酚酞试液不变色 |
| C.测得反应后溶液中Na+与Cl﹣的个数比为1:1 |
| D.滴入适量AgNO3溶液和稀硝酸,观察到有白色沉淀 |
鱼胆弄破后,会使鱼肉粘上一种难以溶于水的胆汁酸(一种酸),使鱼肉变苦.下列物质中最适宜用来冲洗鱼肉,以消除这种苦味的是
| A.食盐水 | B.醋酸 | C.纯碱溶液 | D.氢氧化钠溶液 |