下列对有关实验操作或现象的描述中,错误的是()
| A. | 用玻璃棒蘸取少量待测液滴在湿润的pH试纸上,与标准比色卡对照并读出 |
| B. | 收集二氧化碳时,将燃着的木条伸到集气瓶口,如果木条立即熄灭,证明瓶内已集满二氧化碳 |
| C. | 向鸡蛋清中滴加几滴浓硝酸,微热,出现黄色 |
| D. | 将碘水滴加在馒头片上,出现蓝色 |
逻辑推理是化学学习常用的思维方法。下列推理正确的是( )
| A.酸性溶液的pH都小于7,所以酸溶液pH一定小于7 |
| B.氧化物都含氧元素,所以含氧元素的化合物都是氧化物 |
| C.水是纯净物,所以海水也是纯净物 |
| D.中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 |
下列实际应用中,利用中和反应原理的是
①用氢氧化钠溶液洗去石油产品中的残余硫酸;②用稀硫酸除铁锈;③用熟石灰改良酸性土壤;④用碳酸氢钠治疗胃酸过多
| A.①③ | B.③④ | C.①②④ | D.①③④ |
常温下,一些物质的pH如下,其中显酸性的物质是( )
| A.柠檬汁 pH=2 | B.鸡蛋清 pH=8 |
| C.蒸馏水 pH=7 | D.肥皂水 pH=10 |
下列离子组能在PH=1的无色溶液中大量共存的
| A.NO3- Fe3+ Na+ OH- | B.K+ SO42- Na+ NO3- |
| C.C1- K+ SO42- Ba2+ | D.Ca2+ Cl- CO32- Na+ |
下列除去杂质(在括号内)选用的试剂(在箭头右侧)不正确的是
| A.CO2(CO)→CuO | B.CaCl2溶液(HCl)→碳酸钙 |
| C.NaCl(泥沙)→水 | D.NaOH溶液(Na2CO3)→稀盐酸 |
(1)配制10%的盐酸的步骤有:①稀释 ②计算 ③装瓶并贴标签 ④量取浓盐酸和水.其正确的顺序为 (填序号).
(2)配制氢氧化钠溶液时,需要的玻璃仪器有量筒、烧杯、滴管及 。
(3)用配得的氢氧化钠溶液与待测的硫酸溶液反应,实验过程中
溶液的pH变化曲线如图所示:
a点对应的溶液呈 (填“酸性”、“碱性”或“中性”);
b点对应的溶液中的溶质为 (写化学式).
根据下列实验现象可以判断某溶液一定呈碱性的是( )
| A.常温下,测得溶液的pH<7 |
| B.溶液中滴入酚酞显红色 |
| C.溶液中滴入石蕊显红色 |
| D.溶液中滴入酚酞不显色 |
课本上有8个"基础实验",以提升同学们的实验能力,以下叙述正确的是()
| A. | "粗盐的初步提纯"实验中,持续加热食盐溶液直至水分蒸干 |
| B. | "氧气的制取与性质"实验中,做铁丝燃烧实验的集气瓶内要预留少量的水 |
| C. | "溶液的酸碱度"实验中,将pH试纸伸入溶液中测定酸碱度 |
| D. | "酸与碱的化学性质"实验中,将实验废液直接倒入下水道 |
根据你的经验,下列家庭小实验不能成功的是( )
| A.用自制净水器把浑浊的河水变为澄清的水 |
| B.用加热的方法修补电木插座 |
| C.用电池上的“锌皮”与食醋反应制氢气 |
| D.用小苏打和柠檬酸自制汽水 |
下列化学实验中能达到预期实验结果的是
| A.借助托盘天平和其他手段测定铜锌合金中锌的质量分数为36.25% |
| B.用pH试纸测定某未知溶液的pH为5.5 |
| C.20℃时,配制2%的氢氧化钙溶液 |
| D.将100g 10%的稀盐酸加热蒸发掉50g水,使得稀盐酸溶质质量分数变成20% |
小方同学在学习酸碱指示剂与常见酸、碱溶液的作用时,归纳出如图所示的关系,图中A、B、C、D是两圆相交的部分,表示指示剂与酸、碱溶液作用时所显示的颜色,则其中表示不正确的是
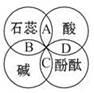
A. 紫色 B.蓝色 C.红色 D.无色
人体一些液体的正常pH范围如下,其中酸性最强的是
| A.胃液0.9 ~1.5 | B.胆汁7.1~7.3 |
| C.血浆7.35~7.45 | D.尿液4.7~8.4 |
为了维持人体正常的生命活动,人体不同器官内的体液具有不同的酸碱性,根据下表可知,在正常情况下()
| 体液 |
唾液 |
胆汁 |
胰液 |
| 6.6﹣7.1 |
7.1﹣7.3 |
7.5﹣8.0 |
| A. |
人体的唾液一定呈酸性 |
B. |
人体的胆汁一定呈碱性 |
C. |
人体的胰液能使紫色石蕊试液变红色 |
D. |
酚酞试液可精确测得以上体液的 |
pH是水质检验的重要指标之一。下列水样中,酸性最强的是
| A.pH = 1.3的工业废水 | B.pH = 4.5的雨水 |
| C.pH = 7.0的蒸馏水 | D.pH = 7.3的矿泉水 |