(1)根据图文回答下列问题。

①金刚石的(填"硬度"或"密度")大
②钠元素是人体必需的(填"常量"或"微量")元素。
③面包中淀粉属于(填字母序号)。
A、糖类 B、蛋白质 C、油脂
④100
该硫酸溶液中溶质质量为
.
(2)自行车是绿色出行的交通工具,根据图文回答下列问题。
①锰属于(填"金属"或"非金属"元素)。
②制造钢质轮圈利用了金属的延展性,这属于(填"物理"或"化学")性质。
③材质属于有机合成材料的是(填字母序号)
④在(填"潮湿"或"干燥")的空气中,自行车的铁质部件更易生锈。
金属材料在生活生产中应用十分广泛,请你用所学的知识回答下列问题:
(1)自行车钢架通常会喷上一层油漆,目的是: ;
(2)自行车中也会用到金属铜,湿法炼铜时,将金属铁放入硫酸铜溶液中,把铜置换出来,请写出化学反应方程式: .
世博同学在探究铝、铜、银三种金属活动性顺序时做了如下实验,并由此得出了正确结论。
(1)请指出上述实验操作中的错误________________________________________;
(2)乙中发生的化学反应方程式为______________________________。
钠是一种非常活泼的金属,它可以和冷水直接反应生成氢气和一种碱,但它不与煤油反应.把一小块银白色的金属钠投入盛有蒸馏水的烧杯中(如图a),可以看到钠浮在水面上,与水发生剧烈反应,反应放出的热量使钠熔成小球,甚至会使钠和生成的氢气都发生燃烧.如果在上述盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,可以看到金属钠悬浮在煤油和水的界面上(如图b),同样与水发生剧烈的反应,但是不发生燃烧.则:
(1)写出钠和水反应的化学方程式 反应类型是
(2)在第二个实验中,钠也与水发生反应,但不发生燃烧,这是因为
(3)第一个实验中,钠浮在水面上;在第二个实验中,钠悬浮在煤油和水的界面上.
这两个现象说明了金属钠具有的物理性质是
(1)《淮南万毕术》:“曾青得铁,则化为铜,外化而内不变”,有人据此说,早在西汉时候(公元前),中国已经知到了下面的反应。请写出相关的化学方程式:
(2)“遥知不是雪,为有暗香来”,产生这一现象的原因是因为分子具有 的性质。
(3)“釜底抽薪”的灭火原理是 。
甲、乙、丙、丁均为常见物质,由氢、碳、氧、氯、铁、钙6种元素中的1-3种组成。在一定条件下,四种物质存在如下转化关系:甲 + 乙 → 丙 + 丁。
(1)若甲的固体俗称干冰,其化学式是 。写出符合上述转化关系的一个化学方程式 。
(2)若甲、丙均为单质,反应后溶液为浅绿色。则符合上述转化关系的反应物是 。
(3)如图所示。关闭止水夹,将装置A注射器中的液体推入瓶中,与集气瓶中收集的气体发生上述(1)的反应,待恰好反应完全后,将装置B分液漏斗中过量的液体放入瓶中(使液面没过导管下端),与瓶中适量固体接触,发生上述(2)的反应,立即关闭开关,打开止水夹,可以看到的现象有:B中的液体进入A中、 ,分析B中液体进入A中的原因是 。

金属铝在金属活动性顺序中的具体位置是.铝比铁活泼。但铝比铁的抗腐蚀性能强,其原因是。铝既能与盐酸反应: ,也能与氢氧化钠溶液反应生成偏铝酸钠( )和氢气。铝与氢氡化钠溶液反应(提示:水也参加反应)的化学方程式为。将铝分别与足量的盐酸和氢氧化钠溶液反应,当产生相同质量的氢气时,所消耗的 和 的质量比为。
某校小组同学利用下图装置完成了有关铁和金属X的兴趣实验。实验前检查装置气密性良好,K1、K2、K3均已关闭。

(1)打开K1,用注射器向Ⅰ中注入稀硫酸,直至液面浸没下端导管口,此时发生反应的化学方程式为 。
(2)打开 ,关闭 ,一段时间后,Ⅰ中的液体转移到Ⅱ中,其原因是 。
(3)依据实验现象,所得结论正确的是 (填字母序号)。
A. 若金属X表面无明显现象,说明X一定是铜
B. 若金属X表面有无色气泡产生,说明X是氢前金属
C. 若金属X表面有无色气泡产生,且表面逐渐变黑,说明X的金属活动性比铁强
金属材料已得到越来越广泛的应用,请依据所学知识回答下列问题.

(1)钢铁是最常用的金属材料.
①钢属于 (填“纯净物”或“混合物”);
②将钢片和纯铁片相互刻画,纯铁片上留下划痕,说明 .
③以赤铁矿(主要成分为氧化铁)为例,写出工业上高炉炼铁的化学方程式: ;
(2)铝制品比铁制品抗腐蚀性更好的原因是 .
(3)向硝酸镁和硝酸铜的混合溶液中加入一定量锌粉,充分反应后过滤,观察到滤液为无色,则该滤液中的溶质一定有 ,滤渣中一定有 .
化学就在我们身边,它与我们的生活息息相关.
(1)"健康饮食、均衡营养"是青少年健康成长的重要保证,日常生活中食用的蔬菜和水果富含的营养素的。
(2)酒精灯的火焰太小时,将灯芯拨得松一些,可使火焰更旺.其原理是。
(3)下列电动自行车的各组件中,属于合成材料的是.
| A. |
橡胶轮胎 |
B. |
钢质车轮 |
C. |
塑料灯罩 |
(4)向一定量的AgNO3和Mg(NO3)2混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,向固体乙中加稀盐酸有气泡产生,则溶液甲中含有溶质的离子是(用离子符号表示)。
2015年5月21日至25日,第三届中国国际矿物宝石博览会在湖南举行,邵阳地区蕴藏着丰富的矿产资源。
(1)下列矿石的主要成分属于氧化物的是(填序号).

(2)铁是应用最广泛的金属.生活中用铁锅做饮具,主要利用铁的性;防止铁锅生锈,常用的方法有.
(3)有
三种金属,它们具有如下性质:
①
均不与稀盐酸反应 ②
↑ ③
则 三种金属活动性由强到弱的顺序是.
某学习小组用相同的光亮铁钉探究铁生锈与哪些因素有关,设计的实验如图所示:
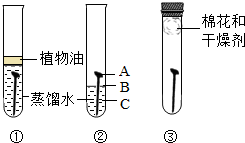
(1)一周后观察:试管①和③中的铁钉无明显变化,试管②中的铁钉明显生锈.探究发现铁生锈的主要条件是铁与_____________直接接触,其中铁钉中的A、B、C三处中________ __处锈蚀最严重.
(2)试管①中加入的蒸馏水要事先煮沸,其目的是___ _.
(3)沙漠地区的铁制品锈蚀较慢的原因是____________.
(1)中国的青铜举世闻名,青铜属于 材料;
(2)中国的铁锅源远流长,受到联合国卫生组织的推崇,原因之一是由于铁锅能为人体补充铁元素。若人体缺乏铁元素,容易引起 症;
(3)被发掘出的宋代铜钱已经锈迹斑斑,这是因为铜能与空气中的 、 以及二氧化碳发生化合反应生成铜绿[Cu2(OH)2CO3],请写出该反应的化学方程式: ;若要除去铜钱表面的铜绿,可选用的试剂为 (填化学式)。
金属材料与我们的生活息息相关。
(1)下列用品所使用的主要材料,属于金属材料的是 ;

A.紫砂锅 B.陶瓷碗 C.不锈钢水瓢 D.塑料盆
(2)人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度 (填“大”或“小”)。
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是 。
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈.
(4)铜与另一种金属M的混合物(M可能是Al、Fe或Ag),在该混合物中加入足量的稀硫酸有气泡产生,则M不可能是 ,待反应完成后 (填实验操作方法),得到铜和滤液,在滤液中加入锌片,其表面有一层黑色物质,则M是 。取一定量的原混合物投入到一定量的AgNO3溶液中,充分反应后,对反应所得溶液和固体推断正确的是 。
A.溶液中一定有M的离子 B.固体中一定有Ag和Cu
C.固体中一定有Ag D.溶液中一定有Ag+