通常情况下,氨气(NH3)是有刺激性气味的无色气体,密度比空气小,极易溶于水,水溶液叫氨水(NH3•H2O)呈碱性,氨气与氯化氢气体相遇产生白烟,生成氯化铵。氨气在化学工业中有着广泛的用途,如制造化肥、纯碱等。根据有关信息,回答下列问题:
(1)写出氨气的物理性质(任写一点) 。
(2)“氨气与氯化氢气体相遇产生白烟”的化学方程式为 。
(3)化工厂发生大量氨气泄漏,可用洒水的方法来吸收,原因是 。
(4)某研究性学习小组用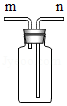 装置来收集氨气,判断氨气已收集满的方法是 。
装置来收集氨气,判断氨气已收集满的方法是 。
金属是重要的资源,在日常生活中已得到越来越广泛的应用.

(1)铜常用于制作导线,因为其具有良好的。
(2)将纯铝和铝合金相互刻画,纯铝上留下明显划痕,说明。
(3)对汽车部分钢铁部件进行喷漆可以防止其生锈,原因是。
(4)如图,向一定量
溶液中加入铜和锌的混合粉末,充分反应后过滤,的溶液甲和固体乙。
①若乙中含有锌、铜、银三种固体,则溶液甲中所含的金属离子符号为,此时向固体乙中加入稀盐酸,发生反应的化学方程式为,该反应类型为反应。
②若溶液甲显蓝色,是因为(用化学反应方程式表示),此时固体乙中一定含有的物质是。
金属及金属材料具有广泛的应用。
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是 。
(2)铁制品在潮湿的环境中容易生锈。某同学进行了如上图1所示实验。一周以后发现铁钉表面锈蚀。图中a、b、c三处锈蚀情况最严重的是 (填字母),产生该现象的原因是 。
(3)如上图2所示的某“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,使用过程中发热是由 能转化为热能。
(4)如图3是教材中炼铁高炉及炉内化学变化过程示意图,根据图示回答下列问题。
①若图中采用的铁矿石的主要成分为氧化铁,请写出A区生成生铁的化学反应方程式 。
②取出铁口的样品少量冷却粉碎放入试管中,加入足量的稀盐酸充分反应后过滤,滤渣主要成分是 。
(5)某小组同学在探究Mg、Cu、Fe三种金属的性质时进行了如图所示实验。
【实验一】发生反应的化学方程式为 。
【实验二】将实验一反应后的物质倒入烧杯中,发现烧杯内的红色固体明显增多,充分反应后过滤。
①下列对滤液中溶质可能成分的判断正确的是 。
| A.MgSO4 | B.MgSO4、FeSO4 |
| C.CuSO4、FeSO4 | D.MgSO4、FeSO4、CuSO4 |
②确定滤渣中所含物质成分的实验方案是 (写出步骤、现象和结论)。
(9分)金属在工农业生产和日常生活中有着很重要的作用。
(1)不锈钢属于 (填“纯净物”、“混合物”)。
(2)铝制品具有很好的抗腐蚀性能,现在世界上铝的年产量已超过了铜。请将方框内横线上的正确答案填写在答题纸上。
(3)某同学实验结束时,为了回收含有CuSO4、ZnSO4、FeSO4废液中的有关金属和盐,设计了如下实验方案:
试回答:
Ⅰ.步骤①中锌粉必须过量的原因是 。
Ⅱ.写出步骤①中任一反应的化学方程式 。
Ⅲ.要检验步骤④中加入的稀硫酸是否足量的方法 。
Ⅳ.若实验过程中的物质损失可以忽略,最终所得硫酸锌的质量 (填“>”、“<”或“=”)原废液中硫酸锌的质量。要计算该废液中硫酸铜质量,必须要称量 的质量。
如图所示,将一个塑料小球放入盛有硫酸铜溶液的烧杯中,小球漂浮于液面,将足量的铁粉投入到烧杯中,充分反应后,观察到铁粉表面有红色物质析出,写出有关反应的化学方程式 ;若溶液体积变化忽略不计,则塑料小球浸入液体中的体积跟原来相比 .

金属活动性顺序在生产和科学研究中有重要应用。请回答下列问题:
(1)法国佳士得拍卖行2009年3月26日拍卖圆明园流失文物鼠首和兔首铜像,拍卖圆明园兽首伤害了中国人民的感情,遭到全中国人民的强烈反对。用化学知识解释鼠首和兔首铜像经历150多年,保存相当完好而没有严重锈蚀的原因是_______________________。
(2)北京2008奥运会金牌为金镶玉,直径为70 mm、厚6mm。实验中学化学兴趣小组对金牌中金属的成分提出猜想:甲认为该金属是由金银合金制成;乙认为该金属是由黄铜(铜锌合金)制成。为了验证他们的猜想,建议取制造这种金牌的材质粉末少量进行实验,下列试剂不能证明甲、乙猜想正误是______。
| A.硫酸铜溶液 | B.盐酸 | C.硫酸锌 | D.硝酸银溶液 |
(3)实验中学研究小组拟用定量的方法测量Al和Fe 分别与稀盐酸反应的 快慢,来比较Al和Fe金属活动性的强弱。设计了甲图所示的装置(实验中采用表面积相同的铝丝和铁丝)。
①实验时,先用砂纸除去铝丝和铁丝表面的氧化物或污物。
②若要比较甲图中产生气体的快慢,可以测量相同时间内产生气体的体积,也可以测量_______________。
③实验测得铝丝产生气体的速率(V)与时间(t)的关系如图乙所示,则t1~t2时间内反应速率逐渐加快的主要原因是________________________________;
绝大多数金属都能与Cl2直接化合生成金属氯化物,如2Na+ Cl2=2NaCl、Cu+ Cl2  CuCl2等。已知A、B、C、D、E五种物质有如下图转化关系(个别反应条件已略去)。已知A是地壳中含量仅次于铝的金属元素的单质,C为紫红色金属单质,A 、C都能与Cl2直接化合生成相应的金属氯化物B、E。回答下列问题:
CuCl2等。已知A、B、C、D、E五种物质有如下图转化关系(个别反应条件已略去)。已知A是地壳中含量仅次于铝的金属元素的单质,C为紫红色金属单质,A 、C都能与Cl2直接化合生成相应的金属氯化物B、E。回答下列问题:
(1)A为 、B为 。
(2)D与Cl2化合生成E的化学方程式为 。
(3)A与E也可以化合生成D,请写出化学反应方程式 。
"铁、锌、铜、镁、铝"是生活中常见的金属。请根据所学知识回答下列问题:
(1)铝块能制成铝箔是利用了铝的性;
(2)黄铜是铜锌合金,其硬度比纯铜(填"大"或"小")。
(3)将一定质量的锌粒投入含有
和
的混合溶液中,充分反应后过滤,若滤液中只含一种溶质,则滤渣中一定含有;
(4)将等质量的镁、铁、锌三种金属分别放入三份溶质质量分数相等的稀盐酸 中。生成氢气的质量与反应时间的关系如图所示。金属
是(填化学式,下同),反应后可能已经反应完的金属是,一定有剩余的金属是。

(5分)金属,与我们生活息息相关。
(1)在空气中 制品(填“铝”或“铁”)更耐腐蚀。
(2)人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度 (填“大”或“小”)。
(3)用下列试剂验证铝、铁、铜这三种金属的活动性顺序,能达到目的是 (填序号)。
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
(4)将等质量的锌粉和铁粉分别于溶质质量分数相同且等质量的稀硫酸充分反应,产生氢气的质量与时间的关系如图所示。请回答下列问题:
(1)表示铁粉与稀硫酸反应的曲线是: (填 a 或 b)
(2)对于曲线a表示的反应, (填化学式)有剩余。
电子产品的迅速发展离不开化学的重要贡献。下图是一款便携卷轴式太阳能手机充电器,其外壳由铝合金制成,铝合金属于(1) 材料。
因其体积小巧轻便,适合户外运动携带,由此体现铝合金具有的一点物理性质是(2) 。该充电器在充电时的能量转化为(3) 。制造智能手机的关键材料有硅,工业上利用二氧化硅和碳在高温下制备单质硅,同时生成一种还原性气体,写出该反应的化学方程式(4) ,反应前后硅元素的化合价分别是(5) 。
铝、铜、铁是生活中常见的金属。
(1)铝在空气中具有很好的抗腐蚀性能的原因是 ;
(2)用铜制电线主要是利用铜具有良好的 性;
(3)铁制品锈蚀,实际上是铁跟空气中的 发生了化学反应;
(4)在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是 (填一种即可)。
A、B、C、D、E、X、Y、Z都是初中化学中的常见物质,其中A是天然气的主要成分,在A物质中碳元素与氢元素的质量比为3:1,X、Y、Z是单质,B、C、D、E是氧化物,常温下C是液体,Y是黑色固体,Z是红色粉末。它们之间有如下反应关系:
请根据以上信息回答下列问题:
(1)有关物质的化学式:A为 ,X为 ,C为 。
(2)B与Y反应的化学方程式为 ,该反应的基本类型为 。D与E反应的化学方程式为 。
化学就在我们身边。请你按要求回答下列问题:
(1)将50mL酒精和50mL水混合,得到溶液的体积小于100mL。试从微观的角度解释这一宏观现象:;
(2)在农村广泛使用沼气(主要成分是CH4),既可以改善人居环境,又使废弃物得到充分利用。请写出沼气充分燃烧的化学方程式:;
(3)在焊接钢管时,工人师傅通常用稀盐酸先将其表面的铁锈除去,反应的化学方程式是。
通过学习金属活动性后,我们知道铜与稀硫酸不能发生反应。某校化学兴趣小组对铜能否与浓硫酸发生反应产生了兴趣,并进行了如下探究:
实验Ⅰ:在一支试管中加入一小块铜片,再加入少量的浓硫酸,放置一段时间,无明显现象;
实验Ⅱ:对实验Ⅰ的试管加热,一段时间后有刺激性气味气体产生,待试管冷却后将其中的物质小心地倒入盛有少量水的烧杯中,得到蓝色溶液。
{查阅资料}
(1)反应生成的刺激性气味气体为二氧化硫。
(2)二氧化硫和二氧化碳化学性质相似,都能和石灰水反应。
{实验结论}
(1)在常温下,铜与浓硫酸 (填“能”或“不能”)发生反应。生成的二氧化硫中硫元素和氧元素的质量比是 。
(2)实验Ⅱ最后得到的蓝色溶液,说明反应生成了硫酸铜,已知该反应还生成了水,请写出铜与浓硫酸反应的化学方程式: 。
(3)铜与浓硫酸在加热的情况下可以发生反应,而铜与稀硫酸即使加热也不能反应,由此说明:物质的化学性质除了与物质的本身的性质有关外,还可能与 有关(填序号)。A、溶液的浓度 B、溶液的质量
(4)为了防止污染空气,兴趣小组可用 吸收生成的二氧化硫气体。
金属与我们密切相关。
(1)铝不易锈蚀的主要原因是________(填字母序号)。
A.铝不会与酸反应
B.铝不会与空气中的氧气反应
C.铝表面的氧化膜具有保护作用
(2)铁粉可用于食品保鲜的原理:铁生锈时能吸收________和_________,使食品保持干燥并防止氧化变质。颗粒大小达到纳米级的单质铁在空气中受撞击时,燃烧生成四氧化三铁,反应的化学方程式为_____________________________________。