阅读下面的科普短文,回答问题。
同学们一定见过晶莹剔透的水晶,你知道它的成分吗?其实水晶的主要成分是二氧化硅(SiO 2),二氧化硅是一种无色晶体,熔点很高,硬度很大,不溶于水,常温下二氧化硅能与强碱溶液缓慢反应。SiO 2在高温条件下能与CaO反应生成CaSiO 3,二氧化硅不与水反应,也不与一般的酸反应,却可以与氢氟酸反应。
二氧化硅用途十分广泛。玻璃中含有二氧化硅,此外,二氧化硅还用于制造光导纤维、电子部件等等。今后二氧化硅将更好地服务于我们的生产生活。
(1)写出二氧化硅的物理性质 (答出一点);
(2)用氢氟酸将精美的图案刻蚀在玻璃上,该过程属于 变化(填"物理"或"化学");
(3)二氧化硅与氢氧化钠反应的化学方程式为:SiO 2+2NaOH=X+H 2O,X的化学式是 ,因此实验室中储存氢氧化钠溶液的试剂瓶应用 (填"玻璃塞"或"橡胶塞")。
小明学习了金属活动性顺序后,欲进一步进行实验探究,他将一小块金属钠投入CuSO4溶液中,看到了下列现象:有大量气体产生,并出现了蓝色沉淀,但没有红色物质析出.小明通过查阅资料,发现钠能与水反应,于是又补做了另一个实验,并记录如下:
| 操作步骤 |
实验现象 |
| ①将一小块钠放入盛水的烧杯中 |
金属钠在水面四处游动,并逐渐溶解,有大量气体产生 |
| ②向反应后的溶液中滴加酚酞试液 |
溶液变红色 |
| ③将产生的气体收集并点燃 |
气体燃烧,并产生淡蓝色火焰 |
分析:由上述现象可知:金属钠与水反应后,生成物中呈碱性的物质是 (选填“NaOH”或“Na2CO3”),其理由是 .
结论:据上述现象,Na投入CuSO4溶液中产生的蓝色沉淀是 .
反思:按金属活动性顺序,一种活动性较强的金属 (选填“能”、“不能”、“不一定能”)把另一种活动性较弱的金属从它的盐溶液中置换出来.
废液中含有AgNO3和Cu(NO3)2,工厂设计生产方案如图所示:

(1)加入的X、Y物质分别是 .
(2)写出①、③两步反应的化学方程式:第①步: ;第③步: .
(3)你认为此方案的生产目的是 .
铝铁铜银是常见的金属。
(1)铝比铁活泼,但铝在空气中比铁稳定,原因是 。
A.铝的密度比铁小
B.铝在地壳中含量比铁高
C.在空气中铝的表面能够形成一层致密的氧化膜
(2)许多金属都与酸反应,可制得氢气。请您写出锌与稀盐酸反应的化学方程式
如图所示,将一个塑料小球放入盛有硫酸铜溶液的烧杯中,小球漂浮于液面,将足量的铁粉投入到烧杯中,充分反应后,观察到铁粉表面有红色物质析出,写出有关反应的化学方程式 ;若溶液体积变化忽略不计,则塑料小球浸入液体中的体积跟原来相比 .

铁是生产、生活中应用很广泛的一种金属。下列是与铁的性质有关的部分实验图,请回答下列问题。
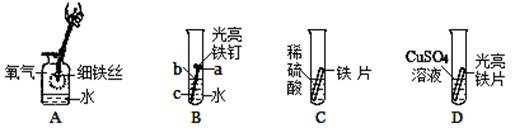
(1)A中发生反应的化学方程式是 ,集气瓶中水的作用是 。
(2)铁生锈的条件是 ,B中铁钉最易生锈的部位是 (填“a”、“b”或“c”)。
(3)C试管中刚好完全反应,得到溶液中溶质的化学式是 。
(4)D中反应一段时间后,现象是 ,试管内固体质量比反应前增大,据此推断,试管内溶液质量与反应前相比 (填“增大”、“不变”或“减小”)。
(1)下列三种金属被发现、使用的先后顺序为:铜、铁、铝。金属大规模被使用的先后顺序跟____________(选填字母)(A.地壳中金属元素的含量;B.金属的导电性;C.金属的活动性)关系最大。
(2)铁制品锈蚀的过程,实际上是铁与空气中的____________和____________等发生化学反应的过程。据有关资料报导,世界上每年因腐蚀而报废的金属设备或材料相当于年产量的20%~40%。保护金属资源,人人有责。请写出一条防止铁制品生锈的方法________________________________________________。目前世界上已有50%以上的废钢铁得到回收利用,其目的是____________(选填字母)。
A.节约金属资源;B.减少矿物开采,合理利用资源;C.防止钢铁生锈
(3)工人师傅切割铁板时,常用硫酸铜溶液在铁板上画线即可留下红色的印迹,此过程中发生的化学方程式为________________________________________________。
(4)某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案。结合如图实验方案回答下列问题:
步骤①中,金属X是____________;
步骤②中,加入过量稀硫酸的目的是__________,该反应的化学方程式为__________________________。
金属在生产和生活中具有广泛的应用。
(1)下列金属制品中,利用金属导热性的是_________(填字母)。

(2)为防止铁制品锈蚀,常在铁制品表面喷漆,防锈原理是使铁制品与 和 隔绝。铝的化学性质比铁活泼,但通常铝制品比铁制品更耐腐蚀的原因是(用化学方程式表示) 。
(3)某兴趣小组欲探究Fe、Cu、Ag、R四种金属的活动性顺序(R为未知金属),进行了如下实验(提供药品:四种金属、稀硫酸、硫酸铜溶液、硫酸亚铁溶液、硝酸银溶液):

①如图A所示,将四根金属丝同时插入烧杯中。甲烧杯中可观察到的现象是铁丝表面产生 ,溶液由无色变为浅绿色。乙烧杯中铁丝表面出现红色固体,银表面无明显现象,则乙中发生反应的化学方程式是 。
②一段时间后,将烧杯中铁丝替换为R进行实验,如图B所示。若甲中出现气泡,乙中无明显现象,则烧杯乙中的溶液是 (请选用提供药品填写),可得出Fe、Cu、Ag、R的活动性顺序由强到弱为 。
为了达到收旧利废节能减排的目的,从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料MgSO4和有关金属,实验过程如下:

请回答:
(1)操作①中被磁铁吸引的金属A是 ;金属B是 。
(2)操作a的名称是 ;在蒸发过程中需要使用玻璃棒,其作用是 。
(3)步骤②所涉及的化学方程 ,该反应基本类型是 。
(4)实验步骤②中除了加入稀硫酸外,还可以选用硫酸铜溶液,请写出反应的化学方程式 。
一段打磨光亮的铁丝在氧气中燃烧,火星四射,生成黑色固体,该反应的符号表达式为 ,基本反应类型为 反应;把另一段光亮铁丝放入蓝色硫酸铜溶液中,一段时间可以看到铁丝表面有红色物质生成,蓝色溶液变成浅绿色,写出该反应的符号表达式: 。
青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具。下图是一种照明用的台灯。

(1)灯管后面的反光片为铝箔。铝块能制成铝箔是利用了铝的 性。
(2)工业上用CO还原氧化铁来炼铁的反应化学方程式是 。
(3)铜、铁、铝是生活中广泛使用的三种金属。若想验证出这三种金属的活动性顺序,除了选用铜和铝两种金属单质外,还需选用 溶液。
(1)在“南海一号”打捞出来的文物中,“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜锈;铁器则锈迹斑斑,残存很少,这说明金、铜、铁这三种金属的活动顺序由强到弱的顺序是 ;
(2)生铁和钢是世界上用量最大的 (填“金属材料”或“合成材料”);炼铁的原理是利用一氧化碳与氧化铁反应,反应的化学方程式为 。写出防止铁生锈的一种方法是 。
若将一定量的铁粉投入到入一定量只含有Cu(NO3)2、AgNO3的工业废水中,充分反应后过滤,向所得滤渣中滴加稀盐酸,没有气泡产生,则滤渣中一定含有的金属是 ;一定不含有的金属是 。