新型高导热镁合金常用作电动汽车和消费电子产品的散热器。请根据如图回答有关问题。

(1)由图1可知,镁的相对原子质量为 。
(2)图2为镁离子的结构示意图,则x的数值为 ,表示镁离子的符号为 。
(3)以化合价为纵坐标、物质类别为横坐标所绘制的图叫价类二维图。图3为镁的价类二维图,B处的物质类别是 。MgO中镁元素与氧元素的质量比为 。价类二维图中的物质在一定条件下可以相互转化,例如金属镁和水发生反应可以生成A和一种单质,则该反应的化学方程式为 。
“嫦娥五号”月球采样返回,“天问一号”成功抵达火星,标志着我国航天事业取得突破性进展。
(1)月壤含CaAl2Si2O8以及可作为核聚变燃料的氦﹣3等物质。
①CaAl2Si2O8中,Si、O两种元素的质量比为 。
②如图为氦元素在元素周期表中的部分信息。氦﹣3原子的质子数与中子数之和为3,则其中子数为 ,核外电子数为 。
(2)着陆器上的仪器可探测水。若月球上存在大量的水,可利用光催化分解水技术得到氧气,对人类在月球上活动意义重大,该反应的化学方程式为 。
(3)火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分如下表。
气体成分 |
CO2 |
N2 |
Ar |
O2 |
其他 |
体积分数/% |
95.32 |
2.7 |
1.6 |
0.13 |
0.25 |
①为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是 。
②若为满足人类未来在火星上生活,下列研究设想不合理的是 。
A.将CO2转化为O2,提高O2含量
B.将CO2分解转化为N2,提高N2含量
C.寻找水的存在和开发水循环技术
D.利用火星上的金属矿物冶炼金属
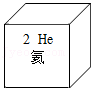
图甲为镁原子的结构示意图,图乙为镁元素在元素周期表中的部分信息。下列说法正确的是( )

| A. |
镁原子的质子数与核外电子数不相等 |
| B. |
镁原子在化学反应中易失去电子形成Mg 2+ |
| C. |
镁原子的质量为24.31g |
| D. |
镁是一种非金属元素 |
2020年6月23日我国的北斗导航"收官之星"在西昌发射成功,北斗导航卫星系统采用铷原子钟提供精确时间。铷元素在元素周期表中的相关信息与铷原子的原子结构示意图如图所示。下列说法不正确的是( )
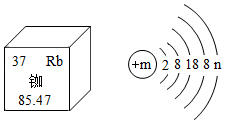
| A. |
铷单质具有导电性 |
B. |
m的值是37,n的值是1 |
| C. |
铷的相对原子质量为85.47 |
D. |
氯化铷的化学式为RbCl 2 |
根据图中提供的信息判断,下列说法不正确的是( )

| A. |
①③属于同种元素 |
| B. |
②表示的元素常见化合价为+1价 |
| C. |
硒元素的相对原子质量是34 |
| D. |
③④为稳定结构 |
几种元素在元素周期表中的部分信息如图所示。请回答下列问题:

(1)下列说法不正确的是 (填写字母标号)。
A.氯原子的质子数为17,最外层电子数为7
B.磷的相对原子质量为30.97g
C.X元素的原子序数为16,元素名称为硫,元素符号为S
D.X元素与磷、氯元素位于同周期,与氧元素位于同一族
(2)一种碳原子叫做碳12,是含有6个质子和6个中子的碳原子,一个碳12原子的质量为ag,则一个氧原子的质量为 (用含a的代数式表示)。
(3)图2所示粒子共表示 种元素。X元素的化学性质与图2中 的化学性质相似(填写字母标号)。
2019年诺贝尔化学奖颁给了约翰•古迪纳夫、斯坦利•威廷汉和吉野彰三位科学家,以表彰他们在锂离子电池领域的卓越贡献。如图是锂元素在周期表中的部分信息及原子结构示意图。下列说法正确的是( )
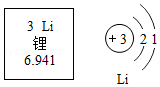
| A. |
锂原子的核电荷数为 1 |
| B. |
锂原子在化学反应中容易失去一个电子 |
| C. |
锂元素的相对原子质量为6.941g |
| D. |
氯化锂的化学式为LiCl 2 |
观察如图粒子结构示意图和元素周期表(部分)。

(1)图甲中,具有相对稳定结构的原子是 (填元素符号)。
(2)图甲中,属于金属阳离子的是 (填离子符号)。
(3)图乙中,X的值为 。
(4)C和D两种元素形成化合物的化学式是 。
硒元素有防癌和抗癌作用。如图,甲是硒的原子结构示意图,乙是硒元素在元素周期表中的信息,下列说法正确的是( )
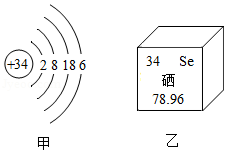
| A. |
硒原子核内中子数为34 |
| B. |
硒原子在化学反应中易得到电子 |
| C. |
硒元素的元素符号为Se,是一种金属元素 |
| D. |
硒的相对原子质量为78.96g |
图一是锶元素在周期表中的信息,图二是几种粒子的结构示意图。请回答:
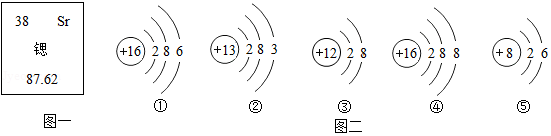
(1)图一中锶原子的核外电子数为 。图二中的粒子共表示 种元素,其中表示阳离子的是 (填序号)。已知原子的核外电子层数与元素所在周期表中周期的序数相同,则④表示的元素在周期表中排在第 周期。
(2)“宏现、微观、符号”相结合,是化学学科的特点。如图三是两种物质反应的微观示意图,该反应的化学方程式 。用实际参加反应的离子符号来表示反应的式子,叫做离子方程式。请写出该反应的离子方程式 。
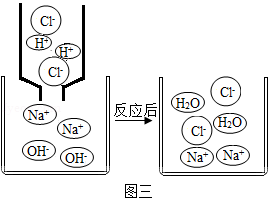
金属材料与人类生活息息相关,请回答下列问题。
(1)钛元素在元素周期表中的信息如图所示,则钛的相对原子质量是 。
(2)家用台灯通常采用铜质插头,是利用金属铜的 性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是 。
(4)将一定质量的Zn片加入AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是 ;若滤液蓝色,则滤液中溶质一定有 。
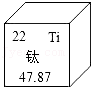
如图是元素周期表的一部分。
(1)写出空气中含量最多元素的符号 。
(2)如图是A、B、C三种粒子的结构示意图,其中属于同种元素的是 (填序号),A粒子与第二周期 元素的原子化学性质相似。
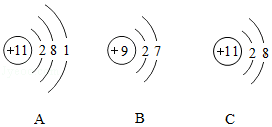
(3)第8号元素的原子在化学反应中易 (填“得到”或“失去”)电子,则第8号元素和第13号元素形成的化合物的化学式是 。
(4)我国科学家张青莲教授主持测定的铟等多种元素的相对原子质量已成为国际标准。关于相对原子质量,下列叙述错误的是 (填序号)。
A.相对原子质量与原子质量没有什么差别
B.由于原子的质量太小,使用不方便,所以采用相对原子质量
C.两种原子的质量之比等于它们的相对原子质量之比
D.采用相对原子质量后,就增大了原子的质量
小倩同学了解到:外国人把中国称为"China",在英文中与瓷器是同一个单词。"青花瓷"又是在中国瓷器中最具代表性的。绘制青花瓷纹饰的原料中主要含有氧化钴(CoO)。
她查阅元素周期表发现钴[读音:gǔ]元素符号为Co,在周期表中与铁元素同位于第4周期、第Ⅷ族。

【提出问题】
小倩同学产生疑问:为什么钴和铁都在第Ⅷ族呢?
【寻求帮助】
(1)[咨询老师]得知:因为铁与钴两种元素原子的结构具有相同点(见图2),使得二者的化学性质相似。因此把这两种元素放在一起。
请你帮助小倩完成下列问题:
①钴元素在元素周期表中的原子序数为 ;一个钴原子比一个铁原子多一个 (填序号)。
A.中子 B.电子 C.质子 D.电子层
②铁原子与钴原子具有相同的 (填序号,下同)。元素的化学性质主要与原子的 有关,因此二者的化学性质相似。
A.核电荷数 B.核外电子数 C.电子层数 D.最外层电子数
③在化学反应中,金属钴和铁一样,也能与稀盐酸发生反应放出氢气,反应的化学方程式为 ;钴在氧气中燃烧生成Co 3O 4,化学方程式为 。
(2)[查阅资料]钴元素有着广泛的用途:钴及其化合物在材料生产、化工生产、医疗中都有着广泛的应用。钴在电池制造中需求量增长很快,钴酸锂(已知:化学式为LiCoO 2,锂元素化合价为+1)常用作手机电池的正极材料,其中钴元素的化合价为 。
【深入探讨】
[产生问题]既然钴与铁的单质具有相似的性质,那么两种元素的化合物是否也有相似的化学性质?
[设计并实验验证]
(1)根据所学知识,同学们已知下列反应可以进行,并进行实验:
FeO FeCl 2 Fe(OH) 2
观察记录实验现象:氧化亚铁为黑色固体;实验a中,随着稀盐酸的加入,黑色固体逐渐溶解,溶液呈现浅绿色;实验b中,加入氢氧化钠溶液后出现白色沉淀,静置在空气中,沉淀物颜色发生变化,最后变为红褐色。[查阅资料得知:原因是溶液中的Fe(OH) 2遇空气中的氧气生成Fe(OH) 3]
(2)同学们欲探究钴元素化合物的性质。设计并进行了如下实验:
CoO CoCl 2 Co(OH) 2
请你依据实验现象,完成下列问题:
Ⅰ.实验①中,取少量灰黑色的氧化钴放入试管中,加入稀盐酸,固体被溶解,溶液呈红色,写出反应的化学方程式 。另取一支试管加入少量氧化钴,滴入浓盐酸,固体被溶解,溶液呈绿色。说明反应后钴离子在溶液中呈现的颜色与加入酸的 有关。
Ⅱ.实验②中,加入氢氧化钠溶液,出现青蓝色沉淀。将试管静置在空气中,沉淀物颜色发生变化,最终变为棕色,试推测沉淀物颜色变化可能与空气中的 有关。
通过实验探究,同学们得出结论:铁和钴两种元素的化合物化学性质相似。
某些元素的相关信息如图所示,请认真分析并回答问题。

(1)原子序数为7的元素位于元素周期表中第 周期,它属于 (填“金属”或“非金属”)元素;
(2)在化学反应中,原子序数为11的元素的原子容易 (填“得”或“失”)电子,形成离子的符号是 ;
(3)根据上表中原子结构示意图分析,氧元素与 (填元素符号)的化学性质相似。