菱镁矿中主要含MgCO3、FeCO3和SiO2.以菱镁矿为原料制取镁的工艺流程如图。
回答下列问题:
(1)菱镁矿属于 (选填“纯净物”或“混合物”)。
(2)流程中滤渣a主要成分是 。
(3)写出菱镁矿中MgCO3与稀HCl反应的化学方程式 。
(4)溶液b→溶液c反应的化学方程式为:4FeCl2+ +4HCl=4FeCl3+2H2O(补充完方程式)
(5)溶液c调pH使Fe3+完全沉淀为Fe(OH)3从而与Mg2+分离,则调pH的范围应为2.8﹣ 。
已知:物质沉淀的pH见下表:
物质 |
Mg(OH)2 |
Fe(OH)3 |
开始沉淀的pH |
8.9 |
1.5 |
完全沉淀的pH |
10.9 |
2.8 |
(6)结合流程中的数据计算。
①菱铁矿中镁元素的质量分数为 (不考虑整个流程转化中的损失)。
②MgCl2通电制得的气体的质量(写出计算过程)。
高纯硅可用于制备硅半导体材料.制备高纯硅的主要生产流程如图所示.
信息:石英砂的主要成分是SiO2,反应①化学方程式SiO2+2C Si+2CO↑
Si+2CO↑
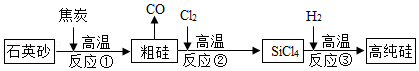
(1)石英砂属于 (填“纯净物”或“混合物”);SiCl4中硅元素的化合价为 ;写出合理处理中间产物CO的一种方法 .
(2)反应③反应除生成高纯硅外,同时还生成一种化合物.请写出此过程的化学方程式 ;
(3)反应③如果H2中混入O2,从安全角度考虑,可能引起的后果是 .
(4)若杂质不参加反应,利用反应①生产含硅质量分数为90%的粗硅2.8吨,计算至少需要焦炭多少吨?