将粗盐溶解、过滤,除去泥沙后,溶液中仍含有少量的CaCl2、MgCl2、Na2SO4,为除去这些杂质,需用到①BaCl2溶液 ②Na2CO3溶液 ③NaOH溶液三种试剂(为将杂质除尽,所加试剂均稍过量,且过量物质须在后续操作中被除去),充分反应后,过滤,再向滤液中加入适量的稀盐酸,加热蒸发,即可获得较为纯净的NaC1固体。以上三种试剂的加入顺序不正确的是( )
A.①②③B.①③②C.②③①D.③①②
结合下图仪器,完成粗盐提纯实验中的有关问题。
(1)仪器①的名称是 。
(2)在过滤粗盐水时,除用到⑤⑥⑦⑧,还需要用到图中的一种玻璃仪器是 (填名称)。
(3)蒸发结晶食盐,除用到①②⑧⑨,还需用到图中的仪器有 (填序号)。
(4)下列有关蒸发结晶操作描述正确的是 。
A.当加热至有晶体析出时,即停止加热
B.当蒸发皿中出现较多固体时,即停止加热
C.当水分完全蒸干时,即停止加热
D.蒸发皿应放在石棉网上加热,防止破损
以下是初中化学一些基本实验,请根据实验内容回答下列问题:
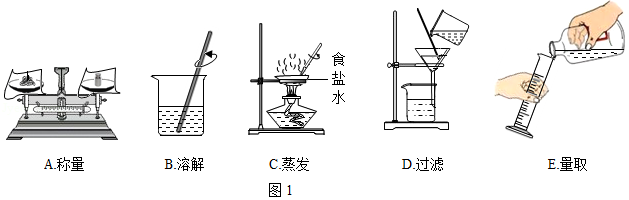
(1)利用如图1进行粗盐中难溶性杂质去除和配制一定质量分数氯化钠溶液的实验。
①粗盐中难溶性杂质去除的主要操作顺序是 (填字母序号);
②配制11%的氯化钠溶液100g。如按如图进行称量和量取,其它操作均规范无误,最终导致配制的氯化钠溶液的溶质质量分数 (填“大于”、小于”或“不能确定”)11%。
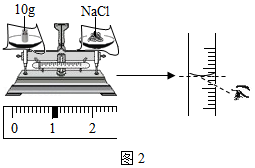
(2)如图为某小组探究金属化学性质的两组实验。
实验I |
实验Ⅱ |
|
|
①实验I中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是 ;
②写出实验Ⅱ中C试管内反应的化学方程式 ;
③实验Ⅱ中要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是 (填字母序号)。
某兴趣小组的同学进行“粗盐中难溶性杂质的去除”实验。下图是实验过程中的部分操作,其中正确的是( )
A. 取一定量粗盐B.
取一定量粗盐B. 溶解
溶解
C. 过滤D.
过滤D. 蒸发结晶
蒸发结晶
海水晒制粗盐的主要成分为NaCl,还含有少量的MgCl2、CaCl2、MgSO4、泥沙等杂质。下面是由粗盐获取较纯净精盐的一种方法:
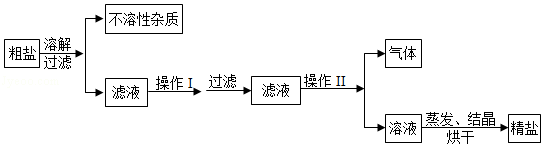
请分析上面流程图示,回答:
(1)为除去MgCl2、CaCl2、MgSO4可溶性杂质,操作I中依次加入的物质(过量)和顺序,合理的是 ;
A.NaOH、BaCl2、Na2CO3
B.Ba(NO3)2、Na2CO3、NaOH
C.Na2CO3、BaCl2、NaOH
D.BaCl2、NaOH、Na2CO3
(2)操作I过量加入各物质的目的是 ;
(3)为获取较纯净精盐,操作Ⅱ的具体方法是 。
在"粗盐中难溶性杂质的去除"实验中,玻璃棒的用途不正确的是( )
| A. |
称取粗盐后,把粗盐研磨细 |
| B. |
溶解时搅拌,加速粗盐溶解 |
| C. |
称量精盐前,把精盐固体转移到纸上 |
| D. |
蒸发时搅拌,防止因局部温度过高,造成液滴飞溅 |
在粗盐的提纯实验中
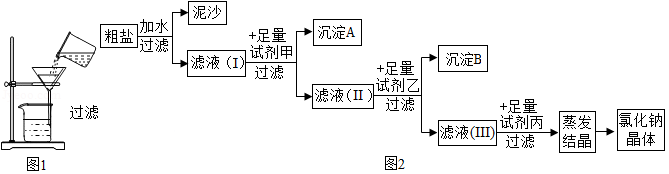
(1)其主要操作步骤顺序是
①过滤 ②溶解 ③蒸发 ④计算产率
(2)图1是某同学过滤的操作图,指出图中明显错误 ;过滤后,如果滤液仍然浑浊,其原因可能是 。(填一种)
(3)蒸发时,蒸发皿内出现 时应停止加热。
(4)通过以上操作只能除去粗盐中难溶性杂质,欲除去可溶性杂质MgCl 2、CaCl 2得到纯净的NaCl,可采用如图2所示流程
①图中所用甲、乙、丙三种试剂依次是
A.NaOH溶液、Na 2CO 3溶液、稀盐酸
B.Na 2CO 3溶液、KOH溶液、稀盐酸
C.NaOH溶液、Na 2CO 3溶液、稀硫酸
②反思交流:通过以上规范操作,制得氯化钠的质量比原粗盐样品中含氯化钠的质量 (填"增多"、"减少"、"不变")。
学会物质的分离提纯和准确配制一定质量分数的溶液在实际应用中有重要意义。
实验一:粗盐提纯

(1)操作①中玻璃棒的作用是 ,操作③的名称为 ;
实验二:溶液配制
(2)用氯化钠固体配制100g质量分数为5%的氯化钠溶液,需要氯化钠 g;
(3)生理盐水可用于补充人体所需电解质,生理盐水中的溶质为 。
提纯含少量泥沙的粗盐样品,实验过程和氯化钠的溶解度数据如下:

温度 (℃) |
溶解度 (g/100g水) |
20 |
36.0 |
40 |
36.6 |
60 |
37.3 |
①20℃时氯化钠的溶解度是 g/100g水。
②该实验是利用泥沙难溶于水而氯化钠 的性质进行提纯,操作Ⅲ的名称是 。
③关于蒸发叙述正确的是 (选填编号)。
a、蒸发是通过加热的方法将水汽化除去
b、所需仪器为酒精灯、蒸发皿、温度计
c、搅拌可以防止蒸发过程中食盐飞溅
d、加热过程中用试管夹夹住蒸发皿移动,使其均匀受热
④溶解时,加入水的合适的量约为 (选填“15”、“30”或“60”)mL,理由是 。
为除去粗盐中含有的氯化镁、硫酸钠、氯化钙等杂质,应加入过量的氢氧化钠、氯化钡、碳酸钠等物质,将杂质转化为沉淀。过滤去除沉淀后,再向滤液中加入适量的盐酸得到精盐水。实验操作过程如图所示:

下列说法错误的是( )
A.实验操作步骤也可以是①③④②⑤⑥
B.操作⑥中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7
C.在实验操作过程中,氯化钡和碳酸钠溶液的添加顺序可以颠倒
D.操作⑤得到的沉淀中共有四种物质
海水中蕴藏着丰富的资源,海水“晒盐”过程中可得到粗盐和卤水.粗盐中常含有多种杂质,必须对其分离和提纯,才能用于生产和生活;卤水经常用作工业制镁的原料.
(1)实验室除去粗盐中不溶性杂质的实验步骤为:溶解、过滤、蒸发结晶.在三步中都要用到的一种玻璃仪器是 .
2杂质,得到较为纯净的食盐晶体.请简述实验操作步骤: .
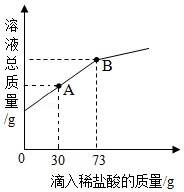
22的混合粉末6g,向其中加入20g水,经充分溶解后,再逐滴加入溶质质量分数为10%的稀盐酸.烧杯中溶液的溶液的总质量与加入稀盐酸的质量关系如图所示,请回答下列问题:
①当滴入稀盐酸30g时(即图中A点时),烧杯内溶液中的溶质是 (填写化学式).
②当滴入稀盐酸73g时(即图中B点时),试通过计算,求此温度时所得不饱和溶液中溶质的质量(计算结果精确至0.1g).
欲将粗盐提纯并用所得精盐配制一定溶质质量分数的氯化钠溶液,说法正确的是( )
A.过滤时,用玻璃棒搅拌加快过滤速度
B.蒸发时,待蒸发皿中晶体全部析出后停止加热
C.配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等
D.配制溶液需要经过计算、称量、溶解、装瓶存放等步骤
在“粗盐难溶性杂质的去除”实验中,操作步骤为:溶解、过滤、蒸发、计算产率。下列各步骤的一些做法正确的是( )
A.溶解:用玻璃棒搅拌以加速溶解
B.过滤:直接将粗盐水倒入漏斗中
C.蒸发:等蒸发皿中水分蒸干便停止加热
D.计算产率:将精盐直接转移到天平的托盘上称量
实验小组的同学欲对一粗盐样品进行初步提纯.
(1)提纯的步骤是:①溶解 ②过滤 ③ ④计算产率;
(2)过滤操作的要点可概括为“一贴、二低、三靠”,写出“三靠”中的任“一靠”操作
(3)在第③步骤中使用了玻璃棒,玻璃棒的作用:
(4)实验小组通过计算发现,实验测得的结果比实际偏低.请分析可能的原因: .