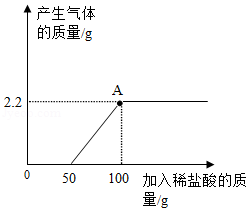
向部分变质的NaOH溶液中逐滴滴加稀盐酸,产生气体质量与所加稀盐酸质量关系如图所示:
(1)完全反应后,产生气体的质量是 g。
(2)当滴加稀盐酸至图中A点时,溶液中含有的溶质是 。
(3)计算所加稀盐酸中溶质的质量分数。(写出规范的计算过程)。
将木炭与氧化铜的粉末均匀混合,放入试管中高温加热至质量不再变化,冷却后粉末质量为16.8克。把该粉末全部倒入烧杯中,加入足量的稀硫酸搅拌,得到蓝色溶液和红色不溶物,经过滤、洗涤、干燥,所得红色不溶物的质量为12.8克。固体物质与所加稀硫酸之间的关系如图所示,则:

(1)反应生成铜的质量是 克;
(2)所加稀硫酸的溶质质量分数是 ;
(3)加热前氧化铜的质量是多少克?(写出计算过程)
电解法是工业上制铜的主要方法:控制一定条件,电解硫酸铜溶液,析出的铜附着在阴极板上,化学方程式为:2CuSO 4+2H 2O  2Cu↓+O 2↑+2H 2SO 4.取一定质量的硫酸铜溶液,在实验室中模拟工业条件进行电解,当硫酸铜恰好完全反应时,得到488.0g溶液和9.6gCu.(注:本题不考虑气体在溶液中的溶解)
2Cu↓+O 2↑+2H 2SO 4.取一定质量的硫酸铜溶液,在实验室中模拟工业条件进行电解,当硫酸铜恰好完全反应时,得到488.0g溶液和9.6gCu.(注:本题不考虑气体在溶液中的溶解)
回答下列问题:
(1)原硫酸铜溶液中溶质的质量分数是多少?(写出解题过程)
(2)向电解后得到的488.0g溶液中加入一定量的某种物质,充分反应后,所得溶液的质量、溶质质量分数均与原硫酸铜溶液相同。则这种物质可能是下列物质中的 (填选项编号)
A.Cu B.CuO C.Cu(OH) 2D.CuCO 3
现有含氯化钠杂质的碳酸钠样品,取6.95g样品溶于水,配制成52.2g溶液。此溶液与50g某溶质质量分数的盐酸恰好完全反应,得到100g溶液。请分析计算:
(1)生成二氧化碳的质量是 。
(2)所得溶液中溶质的质量分数(写出计算过程)。
用光卤石为原料提取的氯化钾产品中含有氯化镁杂质,产品等级中氯化钾指标为:
|
指标名称 |
优良品 |
一级品 |
二级品 |
|
氯化钾质量分数(≥) |
93.00% |
90.00% |
87.00% |
为确定某氯化钾产品等级进行了以下实验:
步骤一(溶解):取40.0g氯化钾产品溶于水,配制成溶液。
步骤二(沉淀):向步骤一所得溶液中加入过量的质量分数为10%的氢氧化钾溶液112.0g,充分反应后过滤,得2.9g沉淀和一定质量的滤液。
步骤三(回收):向步骤二所得滤液中加入盐酸至溶液呈中性,得到400.0g溶液,将所得溶液蒸发结晶,回收氯化钾固体。
回答下列问题:(提示:KCl溶液呈中性;不考虑实验过程中的损失)
(1)通过计算判断该产品的等级。(写出解题过程)
(2)步骤三所得溶液中氯化钾的质量分数为 。
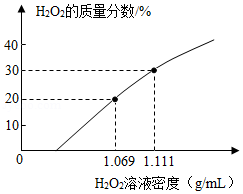
在新冠肺炎的疫情防控中,过氧化氢(H2O2)广泛用于环境消毒,在放置过程中会缓慢分解。某单位有一桶未曾使用过的久置的H2O2溶液,观测得其溶液密度为1.069g/mL,该温度下溶液的密度和溶质质量分数的对应关系如图。桶上标签提供的信息:①H2O2的质量分数为30%;②内装溶液质量50kg,完成下列问题:
(1)该久置的H2O2溶液的溶质质量分数为 。
(2)若用此久置的H2O2溶液来配制质量分数为3%的环境消毒液200kg,需用这种H2O2溶液 kg。
(3)若这桶H2O2溶液放置至完全分解,桶中剩下的液体质量是多少?(假设液体不挥发,通过计算回答,结果精确到0.1)
某化肥厂生产的一种化肥包装袋上的说明如图所示,化学兴趣小组为测定其纯度,取样品5.6克,完全溶于水,向所得溶液中加入100克一定溶质质量分数的硝酸银溶液,恰好完全反应生成14.35克沉淀(杂质不与硝酸银溶液反应)。通过计算回答。
(1)所用硝酸银溶液的溶质质量分数;
(2)该化肥是否合格(结果精确到0.1%)。

铜粉中混有少量的铁粉,为了除去铁粉,某校兴趣小组同学,取该铜粉20g于烧杯中,然后等量分5次加入未知质量分数的某强酸(W)溶液,充分反应后所得数据如下表,请根据相关知识和图表信息回答下列问题。
|
项目 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
加入W溶液的质量/g |
5 |
5 |
5 |
5 |
5 |
|
每次产生气体的质量/g |
0.01 |
0.01 |
0.01 |
0.005 |
0 |
(1)写出你所选择酸(W)的化学式 。
(2)铜粉中混有铁粉的质量是 。
(3)计算你选择酸(W)的质量分数(写出计算过程)。
将14g不纯的氢氧化钾样品(所含杂质既不溶于水,也不参与反应)放入烧杯中,向其中加入90.8g水,充分溶解后,继续加入一定质量的稀硫酸恰好完全反应。过滤,得到溶质质量分数为8.7%的硫酸钾溶液200g。
求:
(1)样品中氢氧化钾的质量;
(2)稀硫酸中溶质的质量分数。
小明同学在完成实验室制取CO2后,对回收的盐酸和CaCl2混合溶液(不考虑其它杂质)进行以下实验:取200g该溶液于烧杯中,向其中滴加溶质质量分数为10.6%的Na2CO3溶液,滴入Na2CO3溶液与生成沉淀的质量关系如图所示。
(1)生成沉淀的质量为 g?
(2)回收液中HCl的质量分数是多少?
(3)当Na2CO3溶液与CaCl2溶液恰好完全反应时,溶液中溶质的质量是多少?

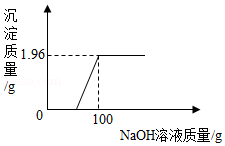
某化工厂排放的废水中含有H2SO4和CuSO4两种污染物。为测定废水中两种污染物的含量,给该化工厂提供污水处理的参考,某化学小组进行了以下实验:取该废水100g,向其中加入溶质质量分数为10%的NaOH溶液,测得生成沉淀的质量与加入NaOH溶液的质量关系如图所示,回答下列问题(写出计算过程):
(1)100g废水中含CuSO4的质量为多少?
(2)废水中H2SO4的质量分数为多少?
用久的热水瓶内胆有一层水垢【主要成分是CaCO3和Mg(OH)2】。兴趣小组为了解具体成分进行了实验。他们取样品25克放入质量为100克的锥形瓶中,置于电子天平上,往瓶内加入150克稀盐酸时,恰好完全反应(样品中的杂质不与稀盐酸反应),此时天平示数如图。对所得混合物进行过滤、洗涤、干燥、称量,得到固体4.2克。请回答下列问题:
(1)恰好完全反应时,溶液中的溶质为 (填化学式)。
(2)样品中CaCO 3的质量分数是多少?
(3)反应结束时溶液中MgCl 2的质量分数是多少?(精确到0.1%)。

某实验小组验证“Fe+Ag2SO4═FeSO4+2Ag”反应并进行了如下探究。已知银粉为黑色,22℃时Ag2SO4的溶解度为0.8g。
①22℃时,向盛有硫酸银饱和溶液的烧杯中加入过量铁粉,搅拌静置,观察到溶液变为黄色并逐渐加深。
②静置3小时后观察,烧杯底部仍有黑色粉末,溶液黄色几乎消失。
③用pH试纸检测Ag2SO4、FeSO4溶液,测得pH均小于7。
回答下列问题:
(1)22℃时,硫酸银饱和溶液显 性(填“酸”“碱”或“中”),其溶质质量分数为 。(列出计算式即可)
(2)取步骤①上层的黄色溶液少许滴加盐酸,观察到白色沉淀,该沉淀的化学式为 。
(3)某同学由步骤②中“仍有黑色粉末”得出Fe比Ag活泼的结论。小组同学讨论后认为思维不严密,因为黑色粉末不一定含Ag,还可能是 ,需要进一步实验才能得出结论,该实验方案是:取黑色粉末少许, 。(补充完实验方案)
(4)溶液呈黄色是因为含有Fe3+离子。小组对Fe3+产生的原因作出如下假设:
a.可能是铁粉表面有氧化物,可产生Fe3+;
b.空气中的O2能与Fe2+反应,可产生Fe3+;
c.溶液中存在 离子能与Fe2+反应,可产生Fe3+。
请设计实验证明假设a、b不是产生Fe3+的主要原因。实验方案是:向同样的铁粉中加入FeSO4溶液,振荡静置,观察到 时即可证明。
为测定某盐酸的溶质质量分数,取200g样品于烧杯中,将50g碳酸钠溶液分为5等份,分5次加入盛有样品的烧杯中。测出每次反应后溶液的总质量,实验数据如下表:
|
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
|
|
加入Na2CO3溶液的质量 |
10g |
10g |
10g |
10g |
10g |
|
反应后溶液的质量 |
208.9g |
217.8g |
226.7g |
235.6g |
245.6g |
请根据实验数据计算盐酸的溶质质量分数。