某工厂利用废硫酸与废铁屑反应制取硫酸亚铁,现取废硫酸4.9t与足量的废铁屑反应,得到硫酸亚铁FeSO 4 1.52t。计算废硫酸中H 2SO 4的质量分数。
将木炭与氧化铜的粉末均匀混合,放入试管中高温加热至质量不再变化,冷却后粉末质量为16.8克。把该粉末全部倒入烧杯中,加入足量的稀硫酸搅拌,得到蓝色溶液和红色不溶物,经过滤、洗涤、干燥,所得红色不溶物的质量为12.8克。固体物质与所加稀硫酸之间的关系如图所示,则:

(1)反应生成铜的质量是 克;
(2)所加稀硫酸的溶质质量分数是 ;
(3)加热前氧化铜的质量是多少克?(写出计算过程)
小华有一只银手镯(银锌合金),她想用实验探究手镯中银的含量。先用电子秤称得手镯的质量是25.00克,再用稀盐酸分多次与此手镯充分反应。实验数据如下表:
|
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
|
加入稀盐酸的质量(克) |
10.00 |
10.00 |
10.00 |
10.00 |
10.00 |
|
充分反应后剩余固体的质量(克) |
24.35 |
23.70 |
23.05 |
23.00 |
23.00 |
根据上表中数据分析,完成下列问题:
(1)手镯中银的质量是 克。
(2)所用稀盐酸中溶质的质量分数是多少?
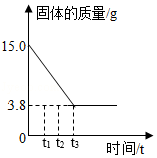
取15g某铁样品(杂质不溶于水也不与酸反应)放入烧杯中,逐渐加入一定质量的稀盐酸至不再产生气泡,烧杯中固体的质量随反应时间的关系如图所示。过滤后向所得滤液中加入143.2g水,测得溶液的溶质质量分数为10%,计算:
(1)该样品中铁的质量。
(2)所用稀盐酸的溶质质量分数。
某热水壶中水垢的成分是Mg(OH)2和CaCO3,某同学通过实验测定水垢中CaCO3的量:向20.8g该水垢中逐滴缓慢加入稀盐酸,将产生的气体通入足量NaOH溶液中,当加入182.5g稀盐酸时,水垢恰好完全反应,此时NaOH溶液的质量增加6.6g。(不考虑盐酸挥发)
(1)CO2与足量NaOH溶液反应的反应方程式 。
(2)水垢与稀盐酸反应生成CO2的质量是 g。
(3)水垢中CaCO3的质量是 g。
(4)计算稀盐酸的溶质质量分数。(写出计算过程)
在82.8克碳酸钠溶液中,逐滴加入盐酸,所加盐酸的质量与产生气体的质量关系如图所示(滴加过程中先发生化学反应:Na2CO3+HCl═NaHCO3+NaCl)。试计算(不考虑气体的溶解和盐酸的挥发):

(1)m的值为 。
(2)刚好不再产生气体时,溶液中溶质的质量分数(写出化学方程式及计算过程)。
NaCl和Na2CO3的固体混合物与一定质量的稀盐酸恰好完全反应,得到4.4gCO2和100g21.1%的NaCl溶液,求:
(1)稀盐酸中溶质的质量为 g。
(2)原混合物中NaCl的质量分数(写出计算过程)。
钙是人体中的常量元素,因缺钙而导致骨质疏松、佝偻病等的患者应在医生的指导下服用钙片。某补钙药剂说明书的部分信息如图1所示。现将100g盐酸分成五等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与关系图如图2.请根据有关信息回答问题。
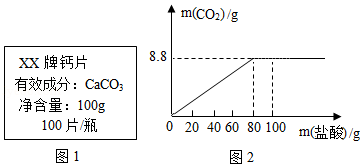
|
实验次数 |
第一次 |
第三次 |
第四次 |
|
加入盐酸的质量(g) |
20 |
20 |
20 |
|
剩余固体的质量(g) |
35 |
a |
20 |
(1)该品牌补钙药剂中CaCO 3的质量分数是 ,a的数值为 。
(2)该盐酸中溶质的质量分数是多少?(写出计算过程,计算结果精确至0.1%)
小华同学为测定某稀盐酸中溶质的质量分数,在烧杯里放入一定质量的大理石,然后分次加入该稀盐酸,充分反应后测得生成二氧化碳的质量如下表所示(大理石中的杂质不参与反应)。
|
加盐酸的次数 |
第一次 |
第二次 |
|
加盐酸的质量/g |
25 |
25 |
|
生成二氧化碳的质量/g |
2.2 |
1.1 |
(1)两次加稀盐酸后,生成二氧化碳的总质量是 g。
(2)该稀盐酸中溶质的质量分数。
某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数,先将10g样品放入烧杯中,再把100g稀盐酸分5次加入该样品中(该实验条件下,杂质不与酸反应,也不溶解于水,忽略稀盐酸挥发),得实验数据如表格。
|
稀盐酸的质量 |
充分反应后剩固体的质量 |
|
第一次加入20g |
8g |
|
第二次加入20g |
6g |
|
第三次加入20g |
4g |
|
第四次加入20g |
2g |
|
第五次加入20g |
2g |
请计算;
(1)10g石灰石样品中碳酸钙的质量分数是 。
(2)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
某补钙片的主要成分为CaCO3,每片钙片重0.5g(假设钙片中其他成分不含钙元素,不溶于水且不与任何物质发生反应)。化学兴趣小组为测定钙片中钙元素的含量,进行了如图实验:
根据图示信息,完成下列各题:
(1)钙片中钙元素的质量分数为 。
(2)求恰好完全反应时所得溶液的溶质质量分数?(要求写出计算过程)
氯可形成多种含氯酸盐,广泛应用于杀菌、消毒及化工领域。实验室中制备KClO3的化学反应方程式为3Cl2+6KOH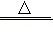 5KCl+KClO3+3H2O。若用Cl2与200g的KOH溶液恰好完全反应,反应后溶液质量为221.3g。计算:
5KCl+KClO3+3H2O。若用Cl2与200g的KOH溶液恰好完全反应,反应后溶液质量为221.3g。计算:
(1)参加反应的氯气的质量为 g。
(2)所用KOH溶液中溶质的质量分数是多少?
欲测定一瓶标签破损的稀硫酸的溶质质量分数,现取30g稀硫酸样品于烧杯中,将15%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示。回答下列问题:
(1)a点溶液中的溶质是 (填化学式)。
(2)计算该稀硫酸的溶质质量分数。(写出计算过程,结果精确到0.1%)

某化学兴趣小组的同学在社会实践中,对废品回收站中废弃电器零部件黄铜(铜、锌合金)中铜的含量产生了兴趣,为了测定该黄铜中铜的含量,小组同学将黄铜带入化学实验室,称取该黄铜样品50克放入指定容器中,然后分四次加入稀硫酸,实验数据记录如表:
|
加入次数 |
第1次 |
第2次 |
第3次 |
第4次 |
|
加入稀硫酸质量(g) |
100 |
100 |
100 |
100 |
|
充分反应后剩余固体质量(g) |
43.5 |
37 |
35 |
n |
请回答下列问题:
(1)根据实验数据分析,n的数值应该为 ;
(2)黄铜样品中铜的质量分数为 ;
(3)所用稀硫酸溶质的质量分数。(写出计算过程)