溶液与人们的生产生活密切相关。
(1)下列常见物质不属于溶液的是 (填序号)。
A.生理盐水
B.糖水
C.医用酒精
D.牛奶
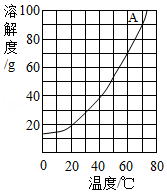
(2)如图是A物质的溶解度曲线,下表是B物质在不同温度时的溶解度。
| 温度/℃ |
B物质溶解度/g |
| 0 |
32 |
| 20 |
35 |
| 40 |
40 |
| 60 |
45 |
| 80 |
55 |
①60℃时,A物质的溶解度是 g。
②50℃时,向100g水中加入40g B物质,充分溶解后得到的是 (填"饱和"或"不饱和")溶液,此时溶液的溶质质量分数是 (结果保留两位小数)。
③请根据表格数据,在A物质溶解度曲线图上绘出B物质的溶解度曲线。
④A、B两种物质溶解度相同时的温度是 ℃。
(3)生活中常用75%酒精消毒液对手和皮肤进行消毒。请分析酒精浓度与杀死细菌的时间对比表(如下)中的数据,酒精消毒液的最合适浓度应为 。根据酒精的物理性质,你认为两者浓度差异的主要原因是 。
| 酒精浓度(%) |
大肠杆菌 |
金黄色葡萄球菌 |
溶血性链球菌 |
| 90 |
15小时 |
30分钟 |
5分钟 |
| 80 |
1小时 |
30分钟 |
5分钟 |
| 70 |
30秒 |
5分钟 |
10秒 |
| 60 |
20秒 |
30分钟 |
10秒 |
| 50 |
20秒 |
2小时 |
20秒 |
| 40 |
22分钟 |
4小时 |
2分钟 |
设计实验、动手操作、观察现象、记录信息、提炼证据、进行推理、形成结论是化学学习的重要方法。
(1)学习化学概念“饱和溶液”﹣﹣﹣实验“KNO3溶于水”
[实验用品]KNO3(研磨处理)、水、玻璃棒、三脚架、石棉网、酒精灯、烧杯等。
[实驰探究]在室温20℃下。向小烧杯中加入20mL水,按下表中设计的操作步骤进行实验。
实验序号 |
实验步骤 |
实验现象 |
实验推理 |
实验结论 |
Ⅰ |
加入2g KNO3,搅拌 |
全部溶解 |
不一定形成饱和溶液 |
在一定温度下,一定量水中不能无限制地溶解溶质 |
Ⅱ |
再加入5g KNO3,搅拌 |
部分溶解 |
|
|
Ⅲ |
加热,搅拌 |
解 |
不一定形成饱和溶液 |
KNO3的溶解度随温度的升高而 。 |
Ⅳ |
再加入5g KNO3,搅拌 |
全部溶解 |
不一定形成饱和溶液 |
|
Ⅴ |
放在冷水的大烧杯中冷却 |
析出晶体 |
一定形成饱和溶液 |
KNO3可用 的方法结晶 增加溶剂的质量,可将饱和溶液转化为不饱和溶液 |
Ⅵ |
,搅拌 |
全部溶解 |
一定形成不饱和溶液 |
[实验反思]
①KNO3预先研磨处理的目的是 。
②实验步骤 (填实验序号,下同)中KNO3的溶质质量分数最大。
③比较实验步骤 中观察到的实验现象,经分析推理。可得出将KNO3饱和溶液转化为不饱和溶液的另一种方法,即升高饱和溶液的温度。
(2)应用化学知识“身边的化学”﹣﹣﹣体验“家庭燃料的变迁”
[文献资料]
①天然气和煤都是 (选填“可再生”或“不可再生”)能源;天然气的主要成分是 (填化学式)。
②我国近50年来家庭燃料变迁:煤或木柴→液化石油气或管道煤气→天然气。
③CO2能产生 效应,SO2易导致酸雨。
④充分燃烧天然气和煤各lkg产生CO2和SO2的质量如图所示。
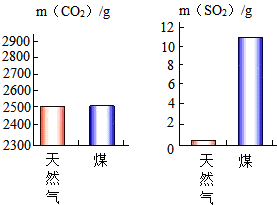
[证据推理]各级政府推广“利用天然气代替煤作家庭燃料,分析文献资料可知实施该项举措的科学依据是 。
[联系实际]为防止燃气泄漏造成危险,使用天然气的家庭“将报警器安装位置确定在燃气灶附近墙壁的上方”,这是基于天然气具有 的性质。
[反思拓展]保护生态环境是建设“人类命运共同体”的重要组成部分,我国科学家正在利用和开发H2等新能源,在一定程度上减少对环境的污染。请再列举一例可利用的新能源: 。
某同学进行硫酸铜晶体(化学式为CuSO 4•5H 2O)的制备和生长实验,配制了某温度时的硫酸铜热饱和溶液,静置、冷却到室温,观察晶体的生长,如图。
(1)能判断原硫酸铜溶液已饱和的方法是 。
A.观察颜色,溶液蓝色较深
B.溶液冷却,有蓝色晶体析出
C.蒸发少量水,有蓝色晶体析出
D.加入硫酸铜晶体,晶体质量不变
(2)现称取49克无水硫酸铜溶于水,配成150克某温度时的热饱和溶液,再冷却到室温,共析出50克硫酸铜晶体,请计算该室温时硫酸铜饱和溶液的溶质质量分数。

根据下表回答问题:
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解度 /g |
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
NH4Cl |
33.5 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
|
(1)海水中含有大量的氯化钠,海水晒盐的原理是 ,氨碱法制纯碱先向饱和食盐水中通入氨气,通入氨气的作用是 ,可向滤出晶体后的NaHCO3溶液中加入 以回收氨,使之循环使用。
(2)氯化钠和氯化铵具有相同溶解度的温度范围在 ℃之间。
(3)图中,A是60℃时含有120g水的NH4Cl溶液,经过如下操作后,得到固体。

I.C中溶液的质量是 g.A溶液为NH4Cl的 (选填“饱和”或“不饱和”)溶液,该溶液中溶质的质量分数为 (结果精确到0.1%)。
II.对以上过程的分析,正确的是 (选填编号)。
①A到B的过程中,溶质质量没有改变
②B中溶质与溶剂的质量比为55.2:100
③由B到C开始析出NH4Cl固体的温度在40℃至50℃之间。
根据下表回答问题:
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解度 /g |
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
NH4Cl |
33.5 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
|
(1)海水中含有大量的氯化钠,海水晒盐的原理是 ,氨碱法制纯碱先向饱和食盐水中通入氨气,通入氨气的作用是 ,可向滤出晶体后的NaHCO3溶液中加入 以回收氨,使之循环使用。
(2)氯化钠和氯化铵具有相同溶解度的温度范围在 ℃之间。
(3)图中,A是60℃时含有120g水的NH4Cl溶液,经过如下操作后,得到固体。

I.C中溶液的质量是 g.A溶液为NH4Cl的 (选填“饱和”或“不饱和”)溶液,该溶液中溶质的质量分数为 (结果精确到0.1%)。
II.对以上过程的分析,正确的是 (选填编号)。
①A到B的过程中,溶质质量没有改变
②B中溶质与溶剂的质量比为55.2:100
③由B到C开始析出NH4Cl固体的温度在40℃至50℃之间。
硝酸钾是实验室常见的一种试剂。
(1)硝酸钾是由 和 构成的(填写微粒符号)。
(2)硝酸钾中钾元素的质量分数是 (结果用百分数表示,保留到0.1%)。
(3)如图是硝酸钾的溶解度曲线,由图可以总结出硝酸钾的溶解度随温度变化的趋势是 。60℃时110g硝酸钾溶于100g水中形成的溶液是 ( 选填“饱和“或“不饱和”)溶液,将此时配得的溶液降温至20℃,析出硝酸钾晶体的质量是 g。
(4)列式计算:用100g 10%的硝酸钾溶液配制5%的硝酸钾溶液。需要加水多少亳升?(水的密度为1.0g•mL﹣1)

根据下表回答问题:
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解度 /g |
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
4Cl |
33.5 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
|
(1)海水中含有大量的氯化钠,海水晒盐的原理是 ,氨碱法制纯碱先向饱和食盐水中通入氨气,通入氨气的作用是 3溶液中加入 以回收氨,使之循环使用。
(2)氯化钠和氯化铵具有相同溶解度的温度范围在 ℃之间。
4Cl溶液,经过如下操作后,得到固体。
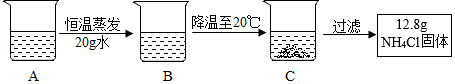
I.C中溶液的质量是 4Cl的 (选填“饱和”或“不饱和”)溶液,该溶液中溶质的质量分数为 (结果精确到0.1%)。
II.对以上过程的分析,正确的是 (选填编号)。
①A到B的过程中,溶质质量没有改变
②B中溶质与溶剂的质量比为55.2:100
4Cl固体的温度在40℃至50℃之间。
20℃时,将等质量的甲、乙两种固体分别加入盛有100g水的烧杯中,充分搅拌后现象如图1所示,甲、乙两物质的溶解度曲线如图2所示。请回答下列问题:

(1)图l中一定为饱和溶液的是 溶液(填“甲”或“乙”)
(2)图2中P点表示的意义 。
(3)图2中表示乙物质溶解度曲线的是 (填“M”或“N”)
控制变量法是科学探究中常用的方法之一。
(1)在探究固体物质的溶解度时,需要考虑的因素有:①溶质的种类;②溶剂的种类;③溶质最多被溶解的质量;④溶剂的质量;⑤温度。
如测定“某物质在不同温度下的溶解度”,研究的是 (填序号)受温度的影响,这就需要控制其他因素保持不变。
(2)右表是利用控制变量法测得的氯化钠、硝酸钾在不同温度时的溶解度,请根据表格内容及实验现象回答下列问题。
温度(℃) |
20 |
40 |
50 |
|
溶解度/g |
NaCl |
36.0 |
36.6 |
37.0 |
KNO3 |
31.6 |
63.9 |
85.5 |
|
①从上表可知,两种物质的溶解度受温度变化影响较大的是 ;
②20℃时,将等质量的NaCl、KNO3分别放入盛有100g水的两个烧杯中,充分溶解后如图1所示,升温到50℃时如图2所示。试判断:50℃时甲烧杯中的溶液一定是 (填“饱和溶液”、“不饱和溶液”或“不能确定”)。

20℃时,将不同质量的NaCl晶体分别加入100g水中,充分溶解后所得溶液质量与加入NaCl晶体质量的对应关系如表:
| 组别 物质质量 |
A |
B |
C |
D |
E |
| NaCl晶体质量/g |
5 |
15 |
20 |
30 |
40 |
| 所得溶液质量/g |
105 |
115 |
X |
130 |
136 |
请回答下列问题:
(1)A组的溶液为 (填"饱和"或"不饱和")溶液。
(2)C组X的值为 。
(3)如图为NaCl的溶解度曲线图,图上a点纵坐标的值为 。Ca(OH) 2的溶解度温度变化的趋势与NaCl相反,则室温时,向饱和石灰水加入少量生石灰,并恢复到室温,此时溶液中溶质的质量 (填">"、"<"或"=")原溶液中溶质的质量。

硝酸钾常用于配制无土栽培的营养液,如图是KNO 3的溶解度曲线,请回答相关问题:
(1)T 1℃时,称量6.0g KNO 3,加入20g水,固体全部溶解,所得溶液的溶质质量分数为 ,该溶液为 (填"饱和"或"不饱和")溶液.
(2) 将上述溶液由T 1℃加热至T 2℃(忽略水的蒸发),有关溶液的变化描述正确的是 (填序号).
a.变为饱和溶液 b.变为不饱和溶液
c.溶质质量分数增大 d.溶质质量分数不变
(3)某同学在T 1℃时,称量6.0gKNO 3,加入20g水,搅拌却发现烧杯中仍有少量固体不溶,该现象可能是下列哪些操作引起的 (填序号).
a.用量筒量取20mL水时俯视读数 b.用量筒量取20mL水时仰视读数
c.称量KNO 3时将砝码放在左盘(1g以下用游码) d.向烧杯中倾倒水时,有水溅出
(4)请写出一种能使(3)中固体全部溶解的措施 .
