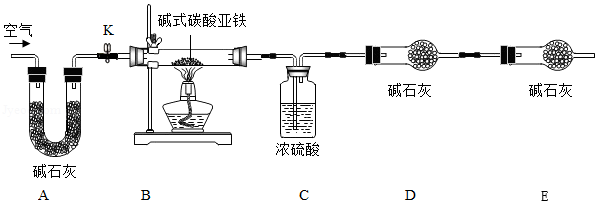
菱铁矿和赤铁矿一样,也是工业上冶炼铁的一种矿物。某种菱铁矿中铁元素的主要存在形式是碱式碳酸亚铁,为测定碱式碳酸亚铁[xFeCO3•yFe(OH)2•zH2O]的组成,华雪同学在老师的指导下设计了如图实验装置:
【查阅资料】
a.碱式碳酸亚铁受热会完全分解生成FeO、CO2和H2O。
b.FeO是一种黑色粉末,它不稳定,在空气中加热,可被氧化成四氧化三铁。
c.石灰是NaOH及CaO的混合物,可以吸收CO2和H2O
【实验步骤】
(1)检查装置的 后,准备称取3.40g碱式碳酸亚铁粉末放在装置B中,连接仪器。
(2) ,鼓入一段时间空气,准确称量装置C、D、E的质量。
(3)关闭弹簧夹K,加热装置B至装置C中导管末端无气泡冒出,再打开弹簧夹K,缓缓通空气一段时间,这样操作的目的是 。
(4)再次准确称量装置C、D、E的质量,所得数据如下
装置C/g |
装置D/g |
装置E/g |
|
加热前 |
200.00 |
180.00 |
180.00 |
加热后 |
200.36 |
180.88 |
180.00 |
(5)图,分析表中数据可知:3.40g碱式碳酸亚铁受热分解过程中生成H2O的质量为 g,CO2的质量为 g,装置E的作用是 。
【实验结论】
在xFeCO3•yFe(OH)2•zH2O中,氢原子与氧原子的个数之比为 。
【实验反思】
(1)装置A的作用是 。
(2)实验结束后,装置B中的残留固体可能全部是FeO.也可能全部是Fe3O4.还可能是 。
(3)为了得到装置B中残留固体的组成,华雪同学称得装置B中残留固体质量为2.24g后,通过计算可知:残留固体的组成及各成分的质量为 。
矿物资源的综合利用,可以节约资源与能源.黄铁矿的主要成分为二硫化亚铁(FeS 2),黄铁矿煅烧的化学方程式:4FeS 2+11O 2═2Fe 2O 3+8SO 2.产生的SO 2用于生产硫酸,矿渣(含有少量的硫元素)用于冶铁.
查阅资料:SO 2气体能使品红溶液褪色,能使澄清石灰水变浑浊,反应的化学方程式为SO 2+Ca(OH) 2═CaSO 3↓+H 2O.
(1)FeS 2中硫元素的化合价为 .矿渣在炼铁高炉内反应产生的高炉气含CO、CO 2、SO 2等气体,其中 是形成酸雨的气体.
(2)某化学兴趣小组为检验高炉气中的CO、CO 2、SO 2,设计了如图所示装置(不考虑其他气体对该实验的影响).
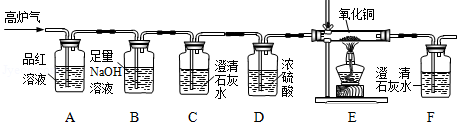
①该装置不能检验出的气体是 .
②装置B的作用是 .
③装置E中发生反应的化学方程式为 .
④确认高炉气中含CO的依据是 (填小写字母).
a.装置C中澄清石灰水变浑浊 b.装置C中澄清石灰水不变浑浊
c.装置E中黑色粉末变成红色 d.装置F中澄清石灰水变浑浊
(3)请指出该装置存在的一处明显缺陷 .