某同学为测定空气里氧气的含量,设计了如图所示的实验装置。该同学在“金属梯”的每一步的凹处放置一颗用滤纸吸干水后的白磷,用放大镜会聚6V手电筒光于靠近水面的一步“金属梯”处的白磷上。
(1)一段时间后,可观察到的主要现象是____________________________________。根据现象你能得出的结论__________________________。
(2)“金属梯”的每一步上都放置一小颗白磷与只靠近水面 的一步“金属梯”处放一大颗白磷相比,优点是___________________。
(3)写出你所学过的产生该实验现象的反应的化学方程式:__________________。
(4)做完此实验:该同学得到启示:要使一个密闭容器中气体压强变小方法_____________________。
请根据下图实验内容回答下列问题。

A B C D
(1)A实验结束待集气瓶冷却后,进入集气瓶中水的体积小于集气瓶容积的五分之一,可能的原因是__________________(填一条即可)。该实验不能用蜡烛代替红磷,理由是___________________。
(2)B实验产生氧气与氢气的体积比约为___________。
(3)C实验观察到的现象是_______________________。
(4)D实验资料信息:白磷和红磷的着火点分别是40℃、240℃。铜片上的红磷不燃烧,是因为_______________。水中的白磷不燃烧,是因为_______________。如果要让水中的白磷在水下燃烧,应采取的措施是____________________。通过以上实验事实证明,燃烧一般需要同时具备下列条件:①物质具有可燃性;②可燃物与氧气接触;③_________________________。
已知空气的主要成分是氮气和氧气,某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:

(1)实验中红磷需稍过量,其目的是 ,待红磷燃烧停止,白烟消失并冷却后,打开弹簧夹,观察到 ,由此可知氧气约占空气总体积的 .下列氮气的性质中,与本实验无关的是: .
.下列氮气的性质中,与本实验无关的是: .
| A.无色无味 | B.难溶于水 |
| C.不能燃烧也不支持燃烧 | D.不与红磷反应 |
(2)如果实验中,打开弹簧夹后,几乎没有水进入集气瓶中,其原因可能是 .
(3)若将红磷换成蜡烛,该实验能否获得成功? ,理由是 .
甲、乙、丙是探究氧气化学性质时三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题.

(1)所发生的三个反应有多个共同的特点,分别是:① ;② ;③ .
(2)丙实验进行时,发生反应的文字表达式为 ,甲瓶底为什么要放少量的水? .
某同学对蜡烛的性质及其燃烧进行了如下探究.请填写下列空格:
(1)取一只蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上.结论 、 .
(2)点燃蜡烛,观察到蜡烛火焰分为三层,分别叫外焰、内焰和 .
把一根火柴梗放在蜡烛的火焰中(如图)约1s后取出可以看到火柴梗的 (填字母)处最先碳化.结论:蜡烛火焰的 温度最高.

某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究。
(1)取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上。
结论:石蜡的密度比水___________(填“大”或“小”)。
(2)将一只干冷的烧杯罩在蜡烛火焰上方,烧杯内壁出现水雾;片刻后取下烧杯,迅速向烧杯内倒入少量澄清的石灰水,振荡,澄清的石灰水变浑浊。据此,写出石蜡燃烧的文字表达式:__________________。
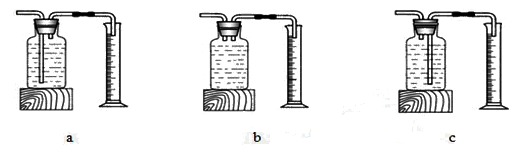
某兴趣小组探究了影响双氧水分解速度的某种因素。实验数据记录如下:
| |
双氧水的质量 |
双氧水的浓度 |
MnO2的质量 |
相同时间内产生O2体积 |
| Ⅰ |
50.0g |
1% |
0.1g |
9 mL |
| Ⅱ |
50.0g |
2% |
0.1g |
16 mL |
| Ⅲ |
50.0g |
4% |
0.1g |
31 mL |
(1)本实验中,测量O2体积的装置是_________________(填编号)。
(2)实验结论:在相同条件下,_____________,双氧水分解得越快。
(3)用右图装置进行实验,通过比较___________________也能达到实验目的。
空气中的氧气摸不着、看不见,但可以利用磷在密封容器中燃烧,消耗氧气,使瓶内气压减小,通过进入水的体积量测定氧气的含量,以下是三种测定空气中氧气含量的方法:
请回答下列问题:
①图3中白磷燃烧时(40℃时白磷就能在空气中自动燃烧)观察到的现象是白磷燃烧产生大量的白烟;活塞先向________(填“左”或“右”)移动,后向_________移动;最后停留在刻度_________处。
②用图2和图3的方法测定空气中氧气的含量比用图1测氧气含量具有的优点是_________________。
为测定空气中氧气的含量,小华同学打算设计如下图所示的实验方案:
在一个隔热效果良好的容器上方安装一个可自由上下移动的活塞(活塞质量忽略不计,起始位置在5刻度处)。加热容器,使容器温度达到80℃(已知白磷燃烧所需的最低温度为40℃)。请回答:

(1)实验过程中,可以观察到:白磷剧烈燃烧,产生大量白烟,活塞先向 __移动,再向 移动,最后停在刻度 处。
(2)发生反应的表达式为________ __。
(3)有位同学做此实验时活塞最终停在4.5处,请你分析造成这一现象的原因是____________ 。
某小组同学进行了有关蜡烛成分测定的实验
| 实验步骤 |
现象 |
结论 |
|
 |
在蜡烛火焰上方罩一个冷而干燥的烧杯 |
烧杯内壁有小液滴 |
产物中有 |
| 将内壁涂有 的烧杯罩在火焰上方 |
|
产物中有二氧化碳 |
由此可知:蜡烛的成分主要由 元素组成,可能还含有 。
如右图所示,在小烧杯A中装入30ml蒸馏水,再滴入3滴酚酞,在小烧杯B中装入300ml浓氨水,用一大烧杯把A、B两个烧杯罩在一起,过一段时间看到的现象是 ,该实验说明 。

一些同学对上述结论有不同看法,主要有以下两种猜测:
第一种:B烧杯中的蒸馏水使酚酞试液变红
第二种:B烧杯中的浓氨水挥发出氨气,扩散到A烧杯中的溶液中使酚酞试液变红。
①你认为 猜测正确。
②为证明这两种猜测,现设计如下实验:(请完成下空)
| 实验内容、方法 |
现象 |
结论 |
| 用洁净的水烧杯取30ml水,滴入2-3滴酚酞试液,观察现象 |
不变色 |
水 使酚酞变色(填“能”或“不能”,下同) |
| 取一张滤纸,滴上酚酞试液,待晾干后,放在装有浓氨水的试剂瓶上方 |
酚酞不变色 |
氨气 使酚酞变色 |
| 将少量氨气通入含有酚酞试液的蒸馏水中 |
溶液变 色 |
氨气溶解水中形成的氨水能使酚酞变色 |
图Ⅰ是小红按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味.于是小明对原实验装置进行了改进装置如图Ⅱ.

【实验操作】
a.向B、C、E三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色
b.在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟.
【分析讨论】:
(1)E试管放有酚酞溶液的目的是 ;
(2)进行操作b时观察到的现象是 ;
(3)由此可以得到的实验结论是:① ;② ;
(4)对比改进前的实验,改进后实验的优点是 。
(12分)“对比实验”是化学学习中行之有效的思维方法。某化学学习小组的同学在学完相关的化学知识后,走进实验室做了如下实验,请你参与并回答下列问题。

| A.燃烧的条件 | B.铁钉生锈的条件 | C.证明CO2与NaOH反应 | D.分子运动的现象 |
(1)通过实验A,可以说明燃烧的条件之一是 ,实验中使用铜片,是利用了铜的 性(填一条物理性质)
(2)对于实验B,一段时间后观察到试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是铁与水和 直接接触。欲除去铁锈可用 洗的方法,铁制品除锈时 (填“能”或“不能”)长时间浸在酸溶液中。
(3)实验C是利用体积相同并充满CO2的软塑料瓶、等量的水(瓶①)和NaOH溶液(瓶②)进行实验,根据塑料瓶变瘪的程度证明CO2与NaOH溶液中的溶质确实发生了反应,这一反应的化学方程式为 。
(4)实验D的烧杯②中呈现的现象能说明分子是不断运动的。当烧杯①中液体是浓氨水时烧杯②中的酚酞溶液由无色变为 色;当烧杯①中液体换成浓盐酸,且烧杯②中液体换成滴有酚酞的NaOH溶液时,一段时间后,溶液颜色的变化是 。其中盐酸与NaOH反应的化学方程式为 ,属于 反应
某同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如图。经过一周观察:试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀。
(1)通过探究发现:铁生锈是铁与 和 共同存在时发生化学反应的过程。
(2)A中加入的蒸馏水要事先煮沸,其目的是 ;
(3)通过探究,请你写出防止铁制品生锈的一种措施 。
图Ⅰ是小明按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小刚对原实验装置进行了改进,装置如图Ⅱ。

【实验操作】
a.向B、C、E三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色 。
b.在A、D试管中分别加入2 mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】:
(1)E试管放有酚酞溶液的目的是: 。
(2)进行操作b时观察到的现象是: ,
(3)由此可以得到的实验结论是① ,
② 。
(4)对比改进前的实验,改进后实验的优点是(只答一点即可): 。