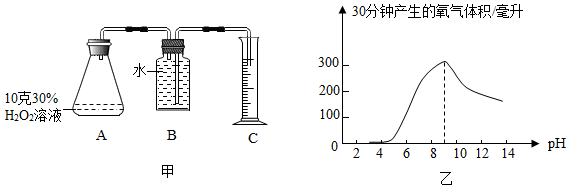
过氧化氢溶液保存时,因缓慢分解导致质量分数变小(化学方程式为2H2O2═2H2O+O2↑)。为探究酸碱性对过氧化氢分解快慢的影响,小明利用图甲装置,每次实验往锥形瓶中加10克30%过氧化氢溶液,再滴加调节剂,使其pH分别从3依次调至13,在60℃反应温度下进行实验,获得数据如图乙。
(1)氧气能用排水法收集,是因为 。
(2)根据本实验结果,对实验室常温保存过氧化氢溶液提出合理的建议: 。
(3)某次实验中,当10克溶质质量分数为30%的过氧化氢溶液分解产生0.32克氧气时,剩余过氧化氢溶液的溶质质量分数为多少?(滴加的试剂对溶液质量的影响忽略不计,计算结果精确到1%)
某实验小组探究了溶质的质量分数对H 2O 2分解速率的影响。实验装置如图1所示,用注射器加入不同浓度的H 2O 2溶液(见下表),实验中使用传感器装置测算生成O 2的质量(圆底烧瓶内气压变化在安全范围),绘制氧气质量随时间变化的曲线,如图2所示。

| 实验编号 | H 2O 2的质量分数(%) | H 2O 2溶液的体积(mL) | 对应曲线 |
| Ⅰ | 3.4 | 10.0 | a |
| Ⅱ | 2.4 | 10.0 | b |
| Ⅲ | 1.7 | 10.0 | c(待绘制) |
(1)实验前需准备不同浓度的H 2O 2溶液,若要配制100.0g质量分数为2.4%的H 2O 2溶液,需质量分数为30%的H 2O 2溶液 g。
(2)根据实验探究目的,从曲线a、b中,可得出的结论是 。
(3)计算实验Ⅰ条件下H 2O 2完全分解所得氧气的质量,并写出具体计算过程(1.5﹣5.0% H2O2溶液的密度取值1.0g/mL)。
(4)在如图2中画出曲线c的大致位置及趋势。