维生素C又称抗坏血酸,广泛存在于水果、蔬菜中,属于外源性维生素,人体不能自身合成,必须从食物中摄取。其化学式为C6H8O6,相对分子量为176.1,由于分子中的烯二醇基具有还原性,能被I2定量地氧化成二酮基,半反应为:
C6H8O6=C6H6O6+2H++2e jy=0.18V
因此,可以采用碘量法测定维生素C药片中抗坏血酸的含量。具体实验步骤及结果如下:
(1)准确移取0.01667mol/L的K2Cr2O7标准溶液10.00mL于碘量瓶中,加3mol/L H2SO4溶液10mL,10% KI溶液10mL,塞上瓶塞,暗处放置反应5min,加入100mL水稀释,用Na2S2O3标准溶液滴定至淡黄色时,加入2mL淀粉溶液,继续滴定至溶液由蓝色变为亮绿色。平行三次实验,消耗Na2S2O3标准溶液平均体积为19.76mL。
(2)准确移取上述Na2S2O3标准溶液10.00mL于锥瓶中,加水50mL,淀粉溶液2mL,用I2标准溶液滴定至蓝色且30s不褪。平行三次实验,消耗I2标准溶液平均体积为10.15mL。
(3)准确称取0.2205g的维生素C粉末(维生素C药片研细所得)于锥瓶中,加新煮沸过并冷却的蒸馏水100mL,2 mol/L HAc溶液10mL,淀粉溶液2mL,立即用I2标准溶液滴定至蓝色且30s不褪,消耗12.50mL。
(4)重复操作步骤(3),称取维生素C粉末0.2176g,消耗I2标准溶液为12.36mL;称取维生素C粉末0.2332g,消耗I2标准溶液为13.21mL。
根据以上实验结果计算出该维生素C药片中所含抗坏血酸的质量分数。
(混合物平均摩尔质量通常可表示为: ,利用此概念可以讨论许多化学问题:
,利用此概念可以讨论许多化学问题:
(1)相同条件下,潮湿空气的密度____(选填“>”、“<”或“=”)干燥空气的密度,理由是___________________________________________________________________;
(2)在一定条件下的密闭容器中,以碳和水蒸气为反应物,发生反应:
C(s)+H2O(g) CO(g)+H2(g);达到平衡后保持温度不变并加压,则
CO(g)+H2(g);达到平衡后保持温度不变并加压,则 (混合气)将 (填写“变大”、“变小”或“不变”);
(混合气)将 (填写“变大”、“变小”或“不变”);
(3)以物质的量之比为1:2相混合的Na2SO3和K2SO3的混合物共a g,与足量盐酸反应生成的SO2物质的量n(SO2)=____________mol(用含a的代数式表示)。
把四氧化三铁与焦炭混合后隔绝空气加热,生成物分别可能为FeO、Fe,CO、CO2。
(1)写出四氧化三碳与碳反应生成物都是低价氧化物的化学反应式: 。
若按此反应进行还原1mol四氧化三铁,固体物质的质量减少 g.
(2)分别取116g四氧化三铁,加入足量的碳粉加热反应后产物分别如下表ABCD所列:
| 编号 |
产物 |
| A |
FeO CO2 |
| B |
FeO CO |
| C |
Fe CO2 |
| D |
Fe CO |
反应中生成气体在标准状况下的最大体积为 L,固体减少的质量最小为 g。
(3)与1mol四氧化三铁作用,从反应开始至反应结束消耗碳的质量mC的可能的范围为 。
(4)如果反应中产生的气体只有CO2,反应作用掉的碳的质量为Xg,则反应生成的固体产物m的取值范围为(用含X的函数表示) 。
(5)如果反应中生成的都是铁,测得反应产生的气体的密度折算到标准状况下为1.429g/L,反应中固体质量减小256g,则反应中生成铁的质量为多少?
为测定某工厂烟道气中SO2的含量,使16.00L烟道气缓慢通过1L水,设SO2完全被吸收,且溶液体积不改变。取出其中20.00mL溶液,加入2—3滴淀粉溶液后,用1.18×10-3mol/L的饱和碘水(密度为1g/cm3)滴定,耗去19.07mL达到终点。(反应为SO2+I2+2H2O→H2SO4+2HI)求
(1)实验条件下碘的溶解度;
(2)该厂烟道气中SO2的含量(mg/L);
(3)为简便计算,在其余操作都不变的情况下,要使滴定时每水泵5mL碘水相当于烟道气中含SO21mg./L,则所配制的碘水的物质的量浓度为多少?
NO2-是一种常见配体,在八面体配离子[MR2(NO2)4]-中,中心离子M含量为21.27%,氮元素的含量为30.33%,只检测到一种N-O键长,请回答下列问题
⑴ 给出自由状态下的NO2-的结构,NO2-在该配合物中配位方式
⑵ 通过计算,给出配离子的化学式和名称
⑶ 画出该配离子的结构
某温度下,测得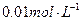 氢氧化钠的PH=11水的离子积常数KW是多少?
氢氧化钠的PH=11水的离子积常数KW是多少?
(1)该温度下,水的离子积常数KW是多少?
(2)在此温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合。
①若所得混合溶液为中性,且a=12,b=2,则Va : Vb为多少?
②若所得混合溶液为中性,且a+b=12,则Va : Vb为多少?
25℃时,若体积为Va、pH=a的某一元强酸与体积Vb、pH=b的某一元强碱混合,恰好中和,且已知Va<Vb和a=0.5b,请填写下列空白;a值可否等于3(填“可”或“否”)_________,其理由是___________________
a值可否等于5(填“可”或“否”)________,其理由是____________________
a的取值范围是_______________________________________。
25℃时,若体积为Va、pH=a的某一元强酸与体积Vb、pH=b的某一元强碱混合,恰好中和,且已知Va<Vb和a=0.5b,请填写下列空白;a值可否等于3(填“可”或“否”)_________,其理由是___________________
a值可否等于5(填“可”或“否”)________,其理由是____________________
a的取值范围是_______________________________________。
有硫酸与硝酸的混合液,取出其中10ml,加入足量的BaCl2溶液,将生成的沉淀过滤洗涤,干燥称得质量为9.32g.另取这种溶液10ml与4mol/L的NaOH溶液25ml恰好中和。求混合液中H2SO4与HNO3的物质的量浓度是多少?
另取10ml的混合液与0.96g铜粉共热时,有多少ml气体产生?
有一瓶白色固体,取少量置于试管中加热,固体逐渐消失,放出水蒸气和其他两种气体,试管内除管口有少量水珠外,没有任何残留物。取0.350g这种固体跟过量的碱液反应,生成一种能使湿润红色石蕊试纸变蓝的气体,这些气体正好能和30.0mL、0.100mol/L H2SO4完全反应;另取0.350g该固体跟足量的盐酸反应,放出一种无色、无溴的气体,将这些气体通入过量的澄清石灰水中,得到0.400g白色沉淀。计算0.350g固体中含有的阴离子和阳离子的物质的量。
根据实验及计算结果确定白色固体是什么?写出判断依据。
(6分)在隔绝空气的条件下,某同学将一块被氧化钠覆盖的钠块用一张无保护膜并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待反应完全后,在容器中收集到1.12L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27g,水槽和容器内溶液的总体积为2.0L,溶液中NaOH的浓度为0.050mol·L-1(忽略溶解的氢气的量)。试通过计算确定该钠块中钠元素的质量分数。
(4分)将一定质量铜与100 mL一定浓度的硝酸反应,铜完全溶解时产生的NO和NO2混合气体在标准状况下的体积为11.2 L。待产生的气体全部释放后,向溶液加入140mL 5 mol·L-1的NaOH溶液,恰好使溶液中的Cu2+ 全部转化成沉淀,求原硝酸溶液的物质的量浓度是多少。
(8分) Fe是人体不可缺少的微量元素,摄入含铁化合物可补充铁。
⑴正常人每天应补充14mg左右的铁。其中绝大部分来自于食物。如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用含 mg FeSO4·7H2O的片剂。
⑵“速力菲”是市场上一种常见的补铁药物,其中Fe2+的含量为35.0%。该药品中Fe2+会缓慢氧化。国家规定该药物中Fe2+的氧化率超过10%即不能再服用。为检验某药店出售的“速力菲”是否失效,取10.00g该药品全部溶于稀硫酸,配制成1000mL溶液。取其中20.00mL,用0.01000 mol/L KMnO4溶液滴定,用去KMnO4溶液24.00mL。通过计算说明该药物是否能服用?(MnO4-在酸性条件下的还原产物为Mn2+,药品中除Fe元素外其他成分不与KMnO4反应)
在室温下,向200mL Cu(IO3)2饱和溶液中加入一定浓度100 mL(经酸化)的KI溶液,发生如下反应:
5I-+IO3-+6H+=3I2+3H2O
2Cu2++4I-=2CuI↓+I2
充分反应后,再加入25.0mL 0.234 mol/L KIO3溶液恰好将过量的KI反应掉。再从上述所得混合液中取出25.0 mL,用0.110 mol/L Na2S2O3溶液滴定,发生反应
I2+2S2O32-=2I-+S4O62-
消耗了30.0mL Na2S2O3溶液。溶液体积改变忽略不计。计算:
(1)原饱和溶液中Cu(IO3)2的物质的量浓度;
(2)若Cu(IO3)2饱和溶液的的密度为1.00g/cm3,Cu(IO3)2的溶解度是多少?
接触法制硫酸,最后的产品是质量分数为98%的硫酸或20%的发烟硫酸(H2SO4和SO3的混合物,其中含20%的SO3)。若98%的硫到可表示为SO3·aH2O,20%的发烟硫酸可表示为SO3·bH2O,
则a,b的值(a、b可用分数表示)分别是:a=_________,b=____________;用
 分别表示SO3转化成上述两种硫酸时,用水的质量与SO3物质的量的关系式分别是:
分别表示SO3转化成上述两种硫酸时,用水的质量与SO3物质的量的关系式分别是: =______
=______ ,
, =______
=______ ;
;若工厂同时生产上述两种硫酸,则两种产品的质量比x(
 ,
, 的硫酸的质量,
的硫酸的质量, 的发烟硫酸的质量)与
的发烟硫酸的质量)与 用量之比的关系是:
用量之比的关系是: ___________x;
___________x;实际生产时,总
 的物质的量一定,x随市场需求而有改变,则用水总量
的物质的量一定,x随市场需求而有改变,则用水总量 、x、
、x、 的关系式是_________________。
的关系式是_________________。