某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测 溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖 嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是
(5)如图,是某次滴定时的滴定管中的液面,其读数为 mL
(6)根据下列数据:
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
25.00 |
0.50 |
20.40 |
| 第二次 |
25.00 |
4.00 |
24.10 |
请计算待测烧碱溶液的浓度: mol/L
下列有关实验原理、方法和结论都正确的是
| A.将蘸有浓氨水的玻璃棒置于某无机酸浓溶液的试剂瓶口,有大量白烟,该无机酸一定为盐酸 |
| B.向含少量苯酚的苯中加入适量溴水后过滤,可除去苯酚 |
| C.向KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去,说明SO2具有还原性 |
| D.某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,该溶液中一定含有SO42- |
下列实验事实不能证明醋酸是弱酸的是
| A.常温下,测得醋酸钠溶液的pH>7 |
| B.常温下,测的0.1 mol·L-1醋酸溶液的pH=4 |
| C.常温下,pH=1的醋酸溶液稀释1000倍,测得pH<4 |
D.常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和 |
如图所示装置实验,若X 轴表示流入阴极的电子的物质的量,则Y 轴可表示
①c(Ag+) ②a棒的质量 ③c(NO-3) ④b棒的质量 ⑤溶液的pH
A ①③ B ③④ C ①②④ D ①③⑤
某同学设计了以下流程来检验碳酸钠粉末中可能含有少量氯化钠和氢氧化钠中的一种或两种杂质。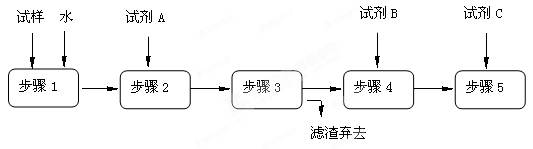
(1)步骤1所需玻璃仪器是 ;步骤3的操作名称是
(2)对检验碳酸钠粉末中可能含有的杂质提出合理假设:
假设1: 只含有氯化钠
假设2: 只含有
假设3: 氯化钠和氢氧化钠都含有
(3)设计实验方案,对假设3进行检验。
限选以 下试剂:氯化钡溶液、硝酸钡溶液、酚酞试液、稀硝酸、稀盐酸、稀硫酸、硝酸银溶液。回答下列问题:
下试剂:氯化钡溶液、硝酸钡溶液、酚酞试液、稀硝酸、稀盐酸、稀硫酸、硝酸银溶液。回答下列问题:
② 入过量试剂A的名称是_______________________。
②填写下表:
| 实验步骤 |
预期现象和结论 |
| 步骤4: |
|
| 步骤5: |
|
某同学在实验报告中记录下列数据,其中正确的是
| A.用25 mL量筒量取12.36 mL盐酸 | B.托盘天平称取8.75克食盐 |
| C.用酸式滴定管量取4.90mL硫酸 | D.用广泛pH试纸测得某溶液pH为3.5 |
用硫酸和铁屑制备硫酸亚铁,反应结束后,需将反应液进行过滤,但过滤时常出现漏斗颈下端管口堵塞的现象 ,可采取的措施是 ( )
,可采取的措施是 ( )
| A.将普通漏斗改为分液漏斗 | B.将漏斗预热,进行热过滤 |
| C.增加滤纸层数 | D.向溶液中加一些稀硫酸 |
用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是44.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s)+ H2SO4(85%)=Na2SO4 + SO2↑+ H2O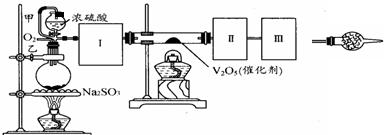
根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合Ⅰ、Ⅱ、Ⅲ处连接的装置分别是 、 、 。
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是 。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(写2点)。
①原因 ,验证方法
②原因 ,验证方法
(4)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式
(5)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为 %(用含a、b的代数式填写)
水蒸气通过灼热的焦炭后,流出气体一的主要成分是和
,还有
和水蒸气等。请用下图中提供的仪器,选择必要的试剂,设计一个实验,证明上述混合气中有
和
。(加热装置和导管等在图中略去)

回答下列问题:
(1)盛浓的装置用途是。
盛溶液的装置用途是。(2)仪器B中需加入试剂的名称(或化学式)是:。
所发生反应的化学方程式是:。
(3)仪器C中需加入试剂的名称(或化学式)是:。
其目的是。
(4)按气流方向连接各仪器,用字母表示接口的连接顺序: 。
(5)能证明混合气体中含的依据是。能证明混合气体中含
的依据是。
下列说法正确的是
| A.可用碘水鉴别苯、四氯化碳、乙醇三种无色液体 |
| B.取11.7 g NaCl固体于烧杯中,加入200 mL蒸馏水(r=1g/cm3)充分搅拌可配成1mol/L的NaCl溶液 |
| C.测定溶液的酸碱性时,应先将pH试纸润湿,然后进行检测 |
| D.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应相等 |
下列实验中,所加物质的浓度不会影响实验现象的是 ( )
( )
A.向Fe(OH)3胶体中滴加HCl,先出现沉淀,后沉淀溶解 |
B.向少量苯酚溶液中滴入溴水,有白色沉淀产生 |
C.向盛有少量MnO2的烧瓶中加入盐酸,加热,有黄绿色气体产生 |
D.向盛有少量铜片的试管中加入H2SO4,加热,有气体放出 |
反应①②是重要的化工反应,D、E、F、G、M为单质,D、E、G、H为气体,且只有E为有色气体,G是空气中主要成分之一,F、M是生活中常见的金属,K是白色沉淀,C的焰色反应为黄色,P是M和紫黑色固体单质化合的产物,P、J、L、M含有同种元素,其物质间转化关系如下,虚框内是需设计的内容,反应物只能用A~N中的物质。请回答下列问题:
(1)用电子式表示H物质的形成过程
(2)电解池①中的阴极产物的名称
(3)足量的E与P溶液反应生成J,离子方程式为
(4)N溶液呈碱性,用离子方程式解释原因
(5)请模仿上述物质转化关系图设计F→K的最佳途径:(用A~N中的物质的化学式表示)
 |
F — →K
按设计得到1molK,至少需要另加的试剂及其物质的量是
n( )=" " mol;n( )=" " mol。
用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是44.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s) + H2SO4(85%)==Na2SO4 + H2O + SO2↑
 |
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中。
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是 _______ 、 _____ 、 _______ 。
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作是 。若用大火加热烧瓶时,SO2的转化率会 (填“升高”、“不变”或“降低”)
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(可以不填满)。
①原因 ,验证方法
②原因 ,验证方法
③原因 ,验证方法
(4)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式
(5)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为 %(用含a、b的代数式填写)