欲除去混在苯中的少量苯酚,下列实验方法正确的是
| A.分液 | B.加入氢氧化钠溶液后, 充分振荡,静置后分液 充分振荡,静置后分液 |
| C.加入过量溴水,过滤 | D.萃取 |
下列有关实验的操作正确的是
| A.若不小心将苯酚沾到皮肤上,应立即用氢氧化钠稀溶液冲洗 |
| B.在石油的分馏实验中,温度计应该伸入到液面下方 |
| C.实验室制备乙烯时,应加入碎瓷片防止爆沸 |
| D.利用电石制备电石气时,用饱和食盐水来进行除杂 |
除去下列括号中的少量杂质的实验操作,能够达到目的的是
| A.甘油(水):直接分液 |
| B.苯(苯酚):加入NaOH溶液充分反应后,再分液 |
| C.甲烷(乙烯):通过盛有酸性高锰酸钾溶液的洗气瓶 |
| D.乙酸乙酯(乙酸):加入NaOH溶液后,再分液 |
能一次性鉴别(NH4)2SO4、NH4Cl 、NaCl 、Na2SO4四种无色溶液的试剂是
| A.Na OH | B.Ba(OH)2 |
| C.AgNO3 | D.BaCl2 |
对于某些离子的检验及结论一定正确的是
| A.SO2通入酸性高锰酸钾溶液中,溶液褪色,说明SO2具有漂白性 |
| B.加入NaOH溶液,生成的白色沉淀在空气中迅速变为灰绿色,最终变为红褐色,则原溶液中一定含有Fe2+ |
| C.加入Ba(NO3)2溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液一定有SO42- |
| D.用洁净的铂丝蘸取溶液在火焰上灼烧,产生黄色的火焰,则原溶液中一定不含有K+ |
在铜催化和加热的条件下,用苯甲醇制得了苯甲醛,同时还有氢气生成。分离出铜后,检验该苯甲醛是否是纯净物可用的方法是
| A.定量分析--测熔点 | B.定性分析--酸性高锰酸钾溶液 |
| C.定量分析--银氨溶液 | D.定性分析--新制氢氧化铜 |
以下物质的分离方法错误的是
| A.将碘和四氯化碳分离:蒸馏、 |
| B.除去苯中混有的苯酚:加入浓溴水,过滤 |
| C.煤焦油和粗氨水的分离:分液、 |
| D.分离溶液中微量的Fe3+ 和Cu2+:纸上层析 |
在括号内离子可能存在情况下,下列对指定离子的检验合理的是
| A.SO42-(SO32-): 加入HNO3酸化的Ba(NO3)2,看能否产生白色沉淀 |
| B.Fe2+ (Fe3+): 先滴加KSCN溶液,再滴加氯水,看溶液是否变红 |
| C.NH4+( HCO3-):与足量NaOH溶液共热,看能否生成使湿润红色石蕊试纸变蓝的气体 |
| D.CO32- (SO32-): 加入足量盐酸,看能否产生使澄清石灰水变浑浊的气体 |
既可用于鉴别乙烷与乙烯,又可用于除去乙烷中的乙烯以得到乙烷的方法是
| A.通过氢氧化钠溶液 | B.通过溴水 |
| C.通过酸性高锰酸钾溶液 | D.通过浓盐酸 |
下列有关实验的操作、原理和现象,正确的是( )
| A.吸滤操作可加快过滤速度,若吸滤完毕,则应先关闭水龙头,然后拆下连接抽气泵和吸滤液的橡皮管 | |
| B.某无色溶液中滴加硝酸银溶液,有白色沉淀生成, 加稀硝酸后沉淀溶解;若另取该溶液加稀硫酸后,微热后有气泡产生;可确定该溶液中一定含NO2- |
C.在纸层析法分离Fe3+和Cu2+的实验中,层析后,经氨熏,滤纸中无色带出现,一定是误将试样点浸没在展开试中 |
| D.结晶时,若沉淀的结晶颗粒较大,静置后容易沉降到容器底部,此时,进行分离的操作方法是倾析 |
某同学为监察溶液中是否含有常见的四种 无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使红色石蕊试纸变蓝。由该实验能得到的正确结论是
无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使红色石蕊试纸变蓝。由该实验能得到的正确结论是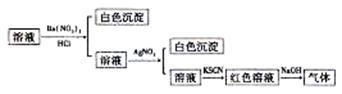
| A.原溶液中一定含有SO42—离子 | B.原溶液中一定含有NH4+离子 |
C.原溶液中一定含有Cl—离子 | D.原溶液中一定含有Fe3+离子 |
下列哪一种试剂可以鉴别乙醇、乙醛、乙酸、甲酸四种无色溶液
| A.银氨溶液 | B.浓溴水 | C.FeCl3溶液 | D.新制Cu(OH)2浊液 |
化学实验中常将某些溶液或试剂进行酸化或碱化。下列处理中正确的是
| A.检验C2H5Br中的Br元素时,将C2H5Br和NaOH溶液混合加热后,加硫酸酸化 |
| B.为提高KMnO4 溶液的氧化能力,用浓盐酸将KMnO4溶液酸化 |
C.检验蔗糖在稀硫酸中水解产生的葡萄糖,应先用NaOH溶解碱化后才 能进一步检验 能进一步检验 |
D.检验溶 液中是否含有SO42-时,先加氯化钡溶液后,再加稀盐酸酸化 液中是否含有SO42-时,先加氯化钡溶液后,再加稀盐酸酸化 |