3名同学在用氯酸钾和二氧化锰混合加热制取氧气的过程中,发现生成的气体有刺激性气味,针对这一“异常现象”进行了实验探究及分析。
(1)甲用湿润的KI-淀粉试纸检验上述生成的气体,观察到试纸变蓝,据此判断氧气中混有Cl2。用离子方程式解释甲判断试纸变蓝的原因 。
(2)乙认为上述现象只能说明混合气体具有 性,实验中使试纸变蓝的气体单质还可能是 。为了进一步验证甲的推测,乙补充了一个实验:将上述生成的气体冷却后通入盛有 溶液的洗气瓶中,若现象为 ,则甲的推测合理。
(3)丙查阅文献获知,这种方法制取氧气的过程中确有Cl2产生,并且查到了以下反应历程:
①2KClO3 + 2MnO2 → 2KMnO4 + Cl2 + O2↑
② 反应②
③K2MnO4 + Cl2 → 2KCl + MnO2 + O2↑
总反应 2KClO3→2KCl + 3O2↑
丙设计实验,通过观察MnO4-的特征颜色来验证反应历程中①的发生,具体实验操作为:将一定量的KClO3和MnO2混合于试管中,加热, 。写出历程中反应②的化学方程式 。
(4)另据文献记载:此法制取的氧气中除了含有Cl2,还混有化合物ClO2。ClO2具有强氧化性,可以将污水中的S2-氧化成SO42-,反应的离子方程式为 。
草酸晶体的组成可表示为H2C2O4·xH2O。实验室常用其加热分解制取CO气体,反应方程式为:H2C2O4·xH2O  CO+CO2+(x+1)H2O。下图为分解草酸晶体,用干燥纯净的CO还原CuO制取Cu,并收集CO的实验装置(略去铁架台、铁夹等支撑加持装置),回答下列问题。
CO+CO2+(x+1)H2O。下图为分解草酸晶体,用干燥纯净的CO还原CuO制取Cu,并收集CO的实验装置(略去铁架台、铁夹等支撑加持装置),回答下列问题。
(1)A装置为加热分解草酸的装置,该装置错误是_________________,C装置中盛放的试剂是_______ (填化学式),E装置的作用是__________。
(2)实验过程中涉及到如下操作:
①点燃A处的酒精灯
②熄灭A处的酒精灯
③点燃D处的酒精灯
④熄灭D处的酒精灯。
这4步操作由先到后的顺序为_______(填序号)。点燃D处酒精灯前必须要进行的操作名称是__________。
(3)用酸性高锰酸钾溶液滴定草酸晶体,求x的值。
实验步骤:准确称取1.17g 草酸晶体,配成100mL溶液;取出20.00mL于锥形瓶中,再向瓶中加入足量稀H2SO4;用0.0500mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液16.00mL。滴定时,所发生的反应为:2MnO4-+5H2C2O4+6H+ = 10CO2+2Mn2++8H2O。
①配制草酸溶液除需要玻璃棒、烧杯,还一定需要的玻璃仪器有_____________。
②x=________。
(4)为探究催化剂对化学反应速率的影响,在甲乙试管中分别加入下列物质
| 试管 |
0.01mol/L KMnO4 |
0.1mol/L H2C2O4 |
0.1mol/L H2SO4 |
MnSO4固体 |
| 甲 |
4 mL |
x mL |
1 mL |
无 |
| 乙 |
y mL |
2mL |
1 mL |
有 |
则x=_______,y=________。能够得出催化剂对该反应有影响结论的实验现象是___________________。
某同学设计如图所示装置(夹持装置已略去,量气管可上下移动)可分别进行下列实验探究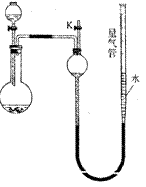
| 实验 |
药品 |
制取气体 |
量气管中液体 |
| Ⅰ |
铜片,浓HNO3(过量) |
NO2 |
CCl4 |
| Ⅱ |
|
NH3 |
煤油 |
| Ⅲ |
MnO2,HCl(浓) |
Cl2 |
|
| Ⅳ |
硅铁合金,NaOH溶液 |
H2 |
H2O |
请回答下列问题:
(1)实验前,某同学检查装置气密性的操作方法是:将活塞K关闭,再将量气管向上提高,其判断装置漏气或不漏气的现象分别是_____
(2)另一同学欲通过实验Ⅰ收集并测量NO2气体的体积来探究铜片的纯度,所测得的结果比真实值偏小(不考虑操作误差),你认为可能的原因是____。
(3)若进行实验II制NH3,则烧瓶和分液漏斗中应分别盛装适量的____。
(4)若进行实验III,该装置缺少的玻璃仪器是____;该反应的离子方程式是_________ 量气管中最好装的液体是_____(选填字母代号)。
a.NaOH溶液 b.水 c.饱和NaCl溶液 d.苯乙烯
(5)实验IV时,应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②_________,③读数时,视线与凹液面最低处水平相切。经多次重复实验,获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 |
某硅铁合金质量 |
量气管第一次读数 |
量气管第二次读数 |
| ① |
1.0g |
10.0 mL |
346.3mL |
| ② |
1.0g |
10.0mL |
336.0mL |
| ③ |
1.0g |
10.0mL |
345.7mL |
根据上述数据,可计算出硅铁合金中硅的质量分数为____。
(14分)某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题:
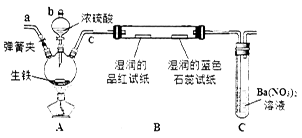
(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为________;实验过程中,装置B中观察的现象是_______________;装置C中有白色沉淀生成,该沉淀是______________(填化学式),原因是___________。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:______________________。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为 (填序号);装置②的作用是 ;③的作用是 ;然后再进行的操作是从a处多次鼓入N2,原因是_______________。
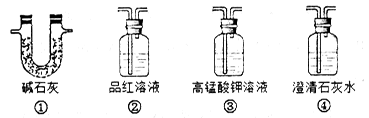
(4)某同学通过验证实验后期装置A中产生的气体中还含有H2,理由是________(用离子方程式表示)。
菠菜营养丰富,在营养价值上是一种高效的补铁剂。但因草酸含量高,因而吃起来有涩味。某学校化学兴趣小组的同学拟通过实验探究以下问题:
①菠菜是否含有丰富的铁;
②菠菜中草酸及草酸盐的含量(以C2O42-计);
通过上网查询,获得以下资料:草酸又名乙二酸,其酸性比乙酸稍强,草酸及其盐具有较强的还原性,其中草酸钙不溶于水。
他们设计的实验步骤如下:
Ⅰ.取菠菜样品,按如下步骤进行实验,观察实验现象。

Ⅱ.另取一份菠菜样品研磨成汁后,在少量开水中煮沸2~3 min,冷却后过滤得滤液。向滤液中加入足量Ca(OH)2溶液,然后再加入足量试剂X,观察现象。并过滤得CaC2O4固体。
Ⅲ.用稀HCl溶解CaC2O4,并加水配制成100mL溶液.每次准确移取25.00mL该溶液,用0.0100mol•L-1KMnO4标准溶液滴定,平均消耗标准溶液VmL。(不考虑Cl-被KMnO4氧化。)
请回答以下问题:
(1)操作①中使用的仪器除三脚架、泥三角、酒精灯、玻璃棒外,还需要的硅酸盐质仪器 ,操作②的名称是 。
(2)通过资料分析,菠菜中的Fe是+2价还是+3价? 。
步骤I中 (填现象)可以证明该结论?
(3)通过步骤Ⅱ可以确定菠菜中含有草酸类物质。由于滤液中含有CO32-,故需加入试剂X排除CO32-的干扰。
则X是 (写化学式),加入试剂X后可观察到沉淀部分溶解。
(4)步骤Ⅲ中用到的玻璃仪器除烧杯、锥形瓶、胶头滴管、玻璃棒外,还有 ,该步骤中滴定操作的终点如何判断________________;所涉及的离子反应方程式 。
(5)若样品的质量为W g,则菠菜中草酸及草酸盐(以C2O42-计)的质量分数为___ __。
(14分)已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验:
(1)装置的连接顺序为 。
(2)饱和食盐水的作用是 。
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
①淡黄色溶液中加入试剂X生成淡红色溶液的离子反应方程式为_______。
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是 。
(4)已知红色褪去的同时有气体生成,经检验为O2。该小组同学对红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀HCl和BaCl2溶液,产生白色沉淀。
②另取同浓度的FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
实验①说明 ;
实验②的目的是 ;
得出结论:溶液褪色的原因是 。
为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。
(1)该组同学为了制取Cl2,SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol/L)为原料制取Cl2。在此实验中,发生装置B应选择三种装置中的___________(选填序号),F的作用是_____________。
(2)D装置中主要反应的离子方程式为__________________________。
(3)为检验通入D装置中的Cl2是否过量,该组同学取适量D溶液滴加至盛有少量紫色石蕊的试管中,若出现___________现象,则Cl2过量,此时E中发生的离子反应方程式为______________________,若D中出现__________________实验现象,则氯气不过量。
某化学小组为了证明SO2和Cl2的漂白性,设计了如下图所示的实验装置:
它们制备SO2和Cl2所依据的原理分别是:
Na2SO3+H2SO4= Na2SO4+H2O+SO2↑ MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)用来制取Cl2的装置是 (填序号),反应中浓盐酸所表现出的化学性质是 和 。
(2)反应开始一段时间后, B、D试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,____ __ (填“B”或“D” )试管中无明显现象。
(3)装置C的作用是 ;
(4)若装置D中的品红溶液换成紫色的石蕊溶液,则出现的现象是 。
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是 。
某小组同学欲研究SO2的性质。
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是 。
| 第1组 |
第2组 |
第3组 |
| S(单质) |
SO2、X、Na2SO3、NaHSO3 |
SO3、H2SO4、Na2SO4、NaHSO4 |
(2)利用下图所示的装置研究SO2的性质:
(熔点:SO2-76.1℃,SO3 16.8℃;沸点:SO2-10℃,SO3 44.8℃)
①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是 。
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是 ;装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时溶液酸性增强,则该反应的离子方程式是 。
③乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,若装置Ⅳ中有40 mL 2.5mol/L NaOH溶液,反应后增重4.8 g,则装置Ⅳ中发生反应的化学方程式是 。
欲探究Na2CO3和NaHCO3稳定性的相对强弱,两同学分别设计了以下两组装置:
请回答:
(1)如甲图所示,分别用Na2CO3和NaHCO3做实验,试管②中的试剂是_______(填字母);
A.稀H2SO4 B.NaOH溶液 C.Ca(OH)2溶液
试管①中发生反应的化学方程式是_________________________。
(2)如乙图所示,试管④中装入的固体应该是_________(填化学式)。
(3)通过上述实验,得出的结论是:Na2CO3比NaHCO3的稳定性_____(填“强”或“弱”)。
Ⅰ、Na2O2与SO3(g)的反应类似于Na2O2与CO2(g)的反应,请写出Na2O2与SO3反应的化学方程式: 。每2molNa2O2参加反应,转移电子数为 。
Ⅱ、某学生课外活动小组模拟呼吸面具中的反应原理,设计用下图所示的仪器来制取氧气并测量氧气的体积。图中量气装置E由甲乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低。
实验可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。
请回答:
(1)图中各装置接口连接顺序是:(填各接口的编号,其中连接胶管及夹持装置均省略)
→ → →⑥ → ⑦ → → →
(2)装置C中放入的反应物是 和 (填化学式)。
(3)装置B的作用是 。
(4)为了较准确测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中,应注意 (填字母编号)。
a.视线与凹液面最低处相平
b.等待气体恢复常温才读数
c.读数时应上下移动乙管,使甲乙两管液面相平
d.读数时不一定使甲乙两管液面相平
(5)实验测收集的氧气在标准状况下体积为V L,则参与反应的Na2O2的物质的量为 mol。
用图示装置制备NO并验证其还原性。
(1)铜与稀硝酸反应的离子方程式是__________。
(2)滴入稀硝酸之前,应该关闭止水夹,点燃红磷并伸入瓶中,塞好胶塞。这样操作的目的是__________。
(3)滴入稀硝酸后,烧杯中的现象是__________。
(4)烧杯中的反应停止后,打开止水夹,通入__________可验证NO的还原性。
某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)装置F中发生反应的离子方程式:______________________________________。
(2)装置A中的烧瓶内固体可选用_________(选填以下选项的代号)。
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择,并将编号填入下列空格:B ,D_____________,E 。(均填编号)
(4)催化剂存在下,NH3可用来消除NO的污染,生成两种对环境无害的物质。写出该反应的化学方程式: ;该反应中每生成0.5molN2转移 mol电子。
研究性学习小组利用下列有关装置进行探究实验,回答相关问题。
(1)写出A中的反应化学方程式
(2)实验时,旋开装置A中分液漏斗的旋塞,发现液体流出缓慢,最终停止,其可能的原因是 。
(3)装置B中的溶液出现浑浊,该实验证明SO2具有 性 。
(4)实验后,测定装置C中溶液呈碱性。溶液为什么呈碱性呢?大家有不同意见:①是生成的Na2SO3水解;②是氢氧化钠剩余。请设计实验方案证明哪种意见成立。选用下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
| 实验步骤 |
实验操作 |
预期现象与结论 |
| |
|
|
(5)另一小组利用装置D进行实验:用注射器向装置D共注入v mL实验室制备SO2的空气,当溶液刚好褪色,停止实验。
该小组的实验目的是 。
Na2S2O3·5H2O在化学定量分析中常用作基准物质,实验室制备原理为
2Na2S+Na2CO3+4SO2 3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。
3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。
(1)A中发生的化学反应方程式为 。
(2)C中所盛试剂可能是 ;若要停止A中的化学反应,除取下酒精灯停止加热外,还可以采取的操作是 。
(3)学生乙在加热A后,发现液面下的铜丝变黑。对黑色生成物该学生提出如下假设:
①可能是CuO ②可能是Cu2O ③可能是CuS
学生丙提出假设②一定不成立,依据是 ;该生用如下实验进一步验证黑色物质的组成:

基于上述假设分析,黑色物质的组成为 (填化学式)。
(4)实验室用Na2S2O3标液测量废水Ba2+的浓度,过程如下:
(已知:2 S2O32一+I2=S4O62—+2 I-)
①写出BaCrO4沉淀与过量HI、HCl溶液反应的离子方程式 ;
②以淀粉为指示剂,则到达滴定终点的现象是 ;
③若标液Na2S2O3的浓度0.0030mol·L-1,消耗该Na2S2O3溶液体积如图,则废水Ba2+的浓度为 。