某化学小组在常温下测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
下列有关判断中不正确的是( )
A 溶液A和B均可以是盐酸或NaOH溶液
B 溶液A和B均可以选用稀硝酸
C 若溶液B选用浓硝酸,则测得铜的质量分数偏小
D 实验室方案II更便于实施
已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是
| A.上述实验证明氧化性:MnO4->Cl2>Fe3+>I2 |
| B.上述实验中,共有两个氧化还原反应 |
| C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝 |
| D.实验②证明Fe2+既有氧化性又有还原性 |
下列变化中,由加成反应引起的是
A.将乙醇蒸汽通过 灼热的氧 灼热的氧 化铜,固体颜色由黑色变为红色 化铜,固体颜色由黑色变为红色 |
| B.苯在一定温度、压强和催化剂的作用下和氢气反应,生成环己烷 |
| C.一定条件下,将苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成 |
| D.往溴水中加入四氯化碳溶液,水层褪色 |
右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是( )
①食盐水 ②KNO3溶液 ③适量稀硫酸铜溶液
④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
| A.①③⑤ | B.①②③ | C.④⑤⑥ | D.①②③⑤ |
某同学通过系列实验探究及其化合物的性质,操作正确且能达到目的的是
| A. |
将水加入浓硫酸中得到稀硫酸,置镁片于其中探究讨
|
| B. |
将
|
| C. |
将
|
| D. |
将
|
根据下列实验现象,所得结论不正确的是
| 实验 |
实验现象 |
结论 |
| A |
左边烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Al>Fe>Cu |
| B |
烧瓶内颜色深浅不同 |
说明:2NO2 N2O4(g) △H<0 |
| C |
白色固体先变为淡黄色,后变为黑色 |
溶度积(Ksp):AgCl>AgBr >Ag2S |
| D |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:Cl>C>Si |
学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上。另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图)。过一会儿,发现纸蝴蝶的颜色由白色转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是
| |
A |
B |
C |
D |
| 纸蝴蝶上的喷洒液 |
石蕊 |
酚酞 |
酚酞 |
石蕊 |
| 小烧坏中的溶液 |
浓盐酸 |
浓氨水 |
氢氧化钠溶液 |
浓硫酸 |
某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )


| A.甲装置:可用来证明碳的非金属性比硅强 |
| B.乙装置:橡皮管的作用是能使水顺利流下 |
| C.丙装置:用图示的方法不能检查此装置的气密性 |
| D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集一氧化氮 |
某研究性学习小组用如图所示装置研究不同能量之间的转化问题。下列说法正确的是( )
| A.断开开关S1,按下开关S2,化学能转化为电能,电能转化为光能等 |
| B.断开开关S1,按下开关S2,此时构成的装置属于电解池 |
| C.断开开关S2,按下开关S1,此时构成的装置属于原电池 |
| D.断开开关S2,按下开关S1,化学能转化为电能 |
易拉罐主要为铝合金,其中以铝铁合金和铝镁合金最为常见。现取几小块易拉罐碎片进行下列实验,其中实验方案与现象、结论正确的是
| 序号 |
实验方案 |
现象、结论 |
| A |
加入盐酸 |
产生无色气体,含铝、铁、镁三种元素 |
| B |
加入NaOH 溶液 |
有无色气体产生,含有铝元素 |
| C |
加入盐酸后,所得溶液中再加入少量NaOH溶液 |
产生白色沉淀,含有镁元素 |
| D |
加入KSCN 溶液 |
溶液呈血红色,含有铁元素 |
用下列装置及实验设计不能达到实验目的的是( )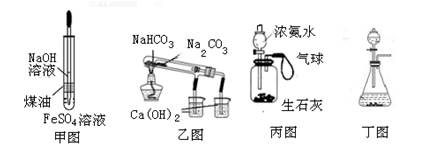
| A.用甲图装置制备少量的氢氧化亚铁 |
| B.用乙图装置验证NaHCO3和Na2CO3的热稳定性 |
| C.用丙图装置可以实现使气球膨胀 |
| D.用丁图装置可以用于实验室制取氧气 |
铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4·5H2O呈蓝色等。研究性学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O进行了认真的探究。 Ⅰ.查阅资料:①Cu2O属于碱性氧化物; ②在空气中灼烧Cu2O生成CuO;③Cu2O在酸性条件下能发生下列反应:Cu2O+2H+=Cu+Cu2++H2O。
Ⅰ.查阅资料:①Cu2O属于碱性氧化物; ②在空气中灼烧Cu2O生成CuO;③Cu2O在酸性条件下能发生下列反应:Cu2O+2H+=Cu+Cu2++H2O。
Ⅱ.设计实 验方案:
验方案:
方案1:取该红色试样溶于足量的稀硝酸中,观察溶液颜色变化
方案2:取该红色试样溶于足量的稀硫酸中,观察溶液是否呈蓝色
⑴请你评价方案1和方案2。如果你认为方案合理,请简述其化学原理;如果你认为该方
案不合理,请简述原因。
方案1 :
方案2 :
Ⅲ.研究性学习小组乙,设计了新的探究方案,拟通过干燥管中CuSO4是否变蓝判断红色固体中是否含有Cu2O,装置如图所示。
(2)为确保探究的科学、合理、安全,你认为实验中还应采取的措施有: (填序号)
A.在氢气发生器与硬质玻璃管之间加一个干燥装置
B.加热前先排尽装置中的空气
C.在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管
用下列装置及实验设计不能达到实验目的的是( )
| A.用甲图装置制备少量的氢氧化亚铁 |
| B.用乙图装置验证NaHCO3和Na2CO3的热稳定性 |
| C.用丙图装置可以实现使气球膨胀 |
| D.用丁图装置可以用于实验室制取氧气 |
用右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是

| A. |
上下移动①中铜丝可控制
|
| B. |
②中选用品红溶液验证
|
| C. |
③中选用
|
| D. |
为确认
|